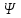2.4.2 Эволюция представлений о строении атома. Корпускулярно-волновой дуализм.
В 1911 году английский физик Э.Резерфорд предложил планетарную модель атома. Эта модель представляла атом как положительно заряженное ядро, состоящее из протонов и нейтронов, вокруг которого вращаются отрицательно заряженные электроны (см. приложение). Общий заряд атома равен нулю, поскольку заряды ядра и электронов равны между собой. В ядре атома сосредоточено 99,9 % массы атома. Ядро атома имеет размером 10 -15 — 10 -14 м, электроны находятся от ядра на расстоянии от 10 тыс. до 100 тыс. поперечников ядра, т.е. основную часть атома составляет пустое пространство.
Модель атома Резерфорда имеет сходство с строением Солнечной системы, поэтому она называется планетарной. Однако планетарная модель не может объяснить устойчивость атома, так как из-за ускоренного движения и притяжения к ядру электрон должен упасть на ядро. Датский физик Нильс Бор (1885-1962) в 1913 предложил новую теорию строения атома, в основу которой положил следующие постулаты:
- Постулат стационарных состояний: электроны в атоме могут двигаться только по определенным (разрешенным или стационарным) орбитам, на которых они не излучают и не поглощают энергию. Электрон на каждой орбите обладает определенной энергией Еn. Чем дальше орбита удалена от ядра атома, тем большей энергией обладает электрон, который на ней находится. Этот постулат позволил ответить на вопрос: почему электроны не падают при движении на ядро атома.
- Правило частот: при переходе с одной стационарной орбиты на другую электрон испускает или поглощает энергию. Поскольку энергии орбит электронов дискретны и постоянны, то и излучение или поглощение энергии происходит порциями (квантами). Второй постулат объяснил прерывность спектра излучения электрона.
Источник
22. Современное представление о строение атома: принцип неопределенности Гейзенберга, двойственная природа электрона.
где Δx — неопределенность (погрешность измерения) пространственной координаты микрочастицы, Δv — неопределенность скорости частицы, m — масса частицы, а h — постоянная Планка. Постоянная Планка равняется примерно 6,626 x 10–34 Дж·с, то есть содержит 33 нуля до первой значимой цифры после запятой.
Согласно принципунеопределённости у частицы не могут быть одновременно точно измерены положение и скорость (импульс). Принцип неопределённости уже в виде, первоначально предложенном Гейзенбергом, применим и в случае, когда не реализуется ни одна из двух крайних ситуаций (полностью определенный импульс и полностью неопределенная пространственная координата — или полностью неопределенный импульс и полностью определенная координата).
Пример: частица с определённым значением энергии, находящаяся в коробке с идеально отражающими стенками; она не характеризуется ни определённым значением импульса (учитывая его направление!), ни каким-либо определённым «положением» или пространственной координатой (волновая функция частицы делокализована в пределах всего пространства коробки, то есть её координаты не имеют определенного значения, локализация частицы осуществлена не точнее размеров коробки).
Двойственная природа электрона
В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, называемых фотонами. Из теории Эйнштейна следует, что свет имеет двойственную (корпускулярно-волновую) природу.
В 1924 г. Луи де Бройль (Франция) выдвинул предположение, что электрон также характеризуется корпускулярно-волновым дуализмом. Позднее это было подтверждено на опытах по дифракции на кристаллах. Де Бройль предложил уравнение, связывающее длину волны λ электрона или любой другой частицы с массой т и скоростью ν,
Волны частиц материи де Бройль назвал материальными волнами. Они свойственны всем частицам или телам. Однако, как следует из уравнения (5), для микротел длина волны настолько мала, что в настоящее время не может быть обнаружена. Так, для тела с массой 1000 кг, двигающегося со скоростью 108 км/ч (30 м/с)
В 1927 г. В. Гейзенберг (Германия) постулировал принцип неопределенности, согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств. Э. Шредингер (Австрия) в 1926 г. вывел математическое описание поведения электрона в атоме.
Работы Планка, Эйнштейна, Бора, де Бройля, Гейзенберга, а также Шредингера, предложившего волновое уравнение, заложили основу квантовой механики, изучающей движение и взаимодействие микрочастиц.
Периодический закон — свойства химических элементов, простых веществ, а также состав и свойства соединений находятся в периодической зависимости от значений зарядов ядер атомов.
В каждой ячейке, соответствующей элементу, представлены: химический символ, название, порядковый номер, соответствующий числу протонов в атоме, относительная атомная масса. Число электронов в атоме соответствует числу протонов. Количество нейтронов в атоме можно найти по разности между относительной атомной массой и количеством протонов, т. е. порядкового номера.
N(n 0 ) = Ar — Z
Количество относительная порядковый
нейтронов атомная масса номер элемента
Например, для изотопа хлора 35 Cl количество нейтронов равно: 35-17=18
Составными частями периодической системы являются группы и периоды.
Источник
Корпускулярно-волновые свойства частиц
Характеристика состояния электронов в атоме основана на положении квантовой механики о двойственной природе электрона, обладающего одновременно свойствами частицы и волны.
Впервые двойственная корпускулярно-волновая природа была установлена для света. Исследования ряда явлений (излучение раскаленных тел, фотоэффект, атомные спектры) привели к выводу, что энергия испускается и поглощается не непрерывно, а дискретно, отдельными порциями (квантами). Предположение о квантовании энергии впервые было высказано Максом Планком (1900 г.) и обосновано Альбертом Эйнштейном (1905 г.): энергия кванта (∆Е) зависит от частоты излучения (ν):
∆Е = hν, где h = 6,63·10 -34 Дж·с – постоянная Планка.
Приравнивая энергию фотона hν к полному запасу его энергии mс 2 и, учитывая, что ν=с/λ, получаем соотношение выражающее взаимосвязь волновых и корпускулярных свойств фотона:
(54)
В 1924 году Луи де Бройль предположил, что двойственная корпускулярно-волновая природа присуща не только излучению, но и любой материальной частице: каждой частице, имеющей массу(m) и движущейся со скоростью (υ) соответствует волновой процесс с длиной волны λ:
Чем меньше масса частицы, тем больше длина волны. Поэтому обнаружить волновые свойства у макрочастиц трудно.
В 1927 г. Американские ученые Девиссон и Джермер, англичанин Томсон и советский ученый Тартаковский независимо друг от друга обнаружили дифракцию электронов, что явилось экспериментальным подтверждением волновых свойств электронов. Позднее была открыта дифракция (интерференция) α-частиц, нейтронов, протонов, атомов и даже молекул. В настоящее время дифракция электронов используется для исследования строения вещества.
В волновых свойствах элементарных частиц заложен один из принципов волновой механики: принцип неопределенности (В. Гейзенберг 1925 г.): для малых тел атомного масштаба невозможно одновременно точно определить положение частицы в пространстве и ее скорость (импульс). Сем точнее определены координаты частицы, тем менее определенной становится ее скорость, и наоборот. Соотношение неопределенностей имеет вид:



где ∆х – неопределенность положения частицы, ∆Рх – неопределенность величины импульса или скорости в направлении х. Аналогичные соотношения записываются и для координат y и z. Величина ℏ, входящая в соотношение неопределенности, очень мала, поэтому для макрочастиц неопределенности в значениях координат и импульсов ничтожны.
Следовательно, нельзя рассчитать траекторию движения электрона в поле ядра, можно лишь оценить вероятность его нахождения в атоме с помощью волновой функции ψ, которая заменяет классическое понятие траектории. Волновая функция ψ характеризует амплитуду волны в зависимости от координат электрона, а ее квадрат ψ 2 определяет пространственное распределение электрона в атоме. В наиболее простом варианте волновая функция зависит от трех пространственных координат и дает возможность определить вероятность нахождения электрона в атомном пространстве или его орбиталь. Таким образом, атомная орбиталь (АО) – область атомного пространства, в котором вероятность нахождения электрона наибольшая.
Волновые функции получаются при решении основополагающего соотношения волновой механики – уравнения Шредингера (1926 г):
(57)
где h- постоянная Планка, — переменная величина, U – потенциальная энергия частицы, Е – полная энергия частицы, x, y,z, — координаты.
Таким образом, квантование энергии микросистемы вытекает непосредственно из решения волнового уравнения. Волновая функция полностью характеризует состояние электрона.
Волновая функция системы – это функция состояния системы, квадрат которой равен плотности вероятности нахождения электронов в каждой точке пространства. Она должна удовлетворять стандартным условиям: быть непрерывной, конечной, однозначной, обращаться в нуль там, где электрон отсутствует.
Точное решение получается для атома водорода или водородоподобных ионов, для многоэлектронных систем используются различные приближения. Поверхность, ограничивающая 90–95 % вероятности нахождения электрона или электронной плотности, называют граничной. Атомная орбиталь и плотность электронного облака имеют одинаковую граничную поверхность (форму) и одинаковую пространственную ориентацию. Атомные орбитали электрона, их энергия и направление в пространстве зависят от четырех параметров – квантовых чисел:главного, орбитального, магнитного и спинового. Первые три характеризуют движение электрона в пространстве, а четвертое – вокруг собственной оси.
Квантовое число n – главное. Оно определяет энергетический уровень электрона в атоме, удаленность уровня от ядра и размер электронного облака. Принимает целые значения от 1 до ∞ и соответствует номеру периода. Из периодической системы для любого элемента по номеру периода можно определить число энергетических уровней атома, и какой энергетический уровень является внешним. Чем больше n, тем больше энергия взаимодействия электрона с ядром. При n = 1 атом водорода находится в основном состоянии, при n> 1 – в возбужденном. Если n ∞, то электрон покинул атомный объем. Произошла ионизация атома.
Источник