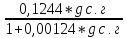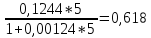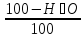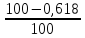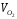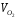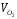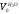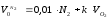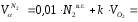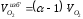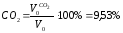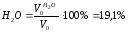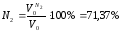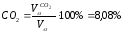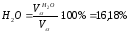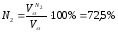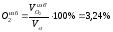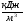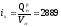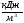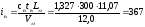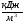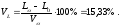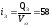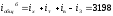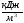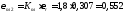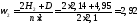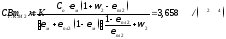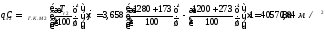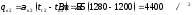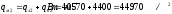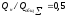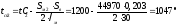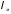- 1. Расчет горения топлива
- 1.5 Расчет теплоты сгорания природного газа
- 1.6 Расчет температур горения
- 2 Определение тепловых потоков и температур металла по длине печи
- 2.1. Определение теплового потока и температур металла в сечении 2
- § 1.4. Энтальпия продуктов сгорания и воздуха
- Энтальпия воздуха и продуктов сгорания котельного топлива. Теплоемкость уходящих дымовых газов.
1. Расчет горения топлива
Сжигается природный газ, элементарный состав которого на сухую массу, %:
Влагосодержание сухого газа составляет g с.г. =5 г ∕ м 3 .
Температура подогрева воздуха tв=300 ° С.
Коэффициент избытка воздуха α=1,2.
Влажность воздуха q св =14.
Механический недожог отсутствует.
1.2 Пересчет состава газа на рабочую (влажную) массу
Рассчитаем процентное содержание водяных паров в 1 м 3 природного газа:
H2O в . г = ;
H2O в.г =%
Пересчитаем состав газа на рабочую массу по формуле:
x в.г =x c .г % ;
CH4 в.г = 98,3*= 96,6%;
1.3 Расчет количества кислорода и воздуха для сжигания 1 м 3 газа
Найдем объем кислорода, необходимый для окисления горючих составляющих природного газа.
=0,01[(m+n∕ 4)∑CmHn в.г. ];
=0,01(2·96,6+3.5·0,129+5·0.009)=1,939 м 3 /м 3 .
Находим количество воздуха при α=1, необходимое для сжигания 1 м 3 природного газа, используя соотношение азота и кислорода в воздухе К=3,76:
L0 с.в =(1+K)
Практически введенное количество воздуха при α=1,2 составит:
1.4 Расчет объема и состава продуктов сгорания при сжигании 1 м 3 газа
Найдем объем продуктов сгорания при α=1
= 0,01[CH4 в. + 2C2H6 в.г +3C3H8 в.г +4C4H10 в.г ] =0,969 м 3 /м 3 ;
= 0,01[H2O в.г +2CH4 в.г +3C2H6 в.г +4С3H8 в.г +5C4H10 в.г ]=1,942 м 3 /м 3 ;
= 7,26 м 3 /м 3 ;
V0=0,969 +1,942 +7,26 =10,17м 3 /м 3 .
Выход продуктов сгорания при α=1,2 изменится только на величину содержания азота, внесенного с избытком воздуха, и на величину избыточного кислорода:
8,7 м 3 /м 3 ;
=0,386 м 3 /м 3 ;
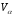
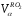
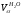
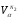
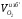
Состав продуктов сгорания при α=1:
Состав продуктов сгорания при α=1,2:
1.5 Расчет теплоты сгорания природного газа
В формулу для Qн р , подставим горючие составляющие, которые указаны в исходных данных и пересчитаны на рабочую массу:
Qн р =34666
1.6 Расчет температур горения
Определим химическую энтальпию топлива:
Физическая энтальпия подогретого воздуха, где св взята из прил. 2.
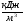
Общая энтальпия продуктов сгорания составит:
Используем приложение 1 — диаграмму itи вычисляем содержание избыточного воздуха в продуктах сгорания:
Теоретическая температура горения природного газа tα т =1950°С.
Энтальпия химического недожога
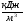
Общее балансовое теплосодержание продуктов сгорания:
Балансовая температура горения природного газа tα т =1970°С.
2 Определение тепловых потоков и температур металла по длине печи
2.1. Определение теплового потока и температур металла в сечении 2
Для расчета лучистого теплообмена необходимо знать эффективную толщину излучающего слоя печных газов вблизи сечение 2, м:
Высота рабочего пространства над заготовками найдена с использованием размеров, указанных на рис. 1.1:
H2 = Н— S=2,54-0,3= 2,24 м, а ширина печи D =2,6 м оставлена без изменения.
Задаем температуру газов в сечении 2 tг2 = 1280°С. Затем из расчета объема и состава продуктов сгоранияопределяем содержание Н20 и С02.
Получаем содержание излучающих газов, а печной атмосфере, а именно:
0,01 Sэф Н2О = 0,01∙ 2,21∙ 11,66= 0,25 атм∙м,
которые необходимы для определения степени черноты при с помощью прил. 6,7 и 8 заданной температуре газов tг2 = 1280°С: водяного пара εСО2 =0,096; εН2О=β∙ εН2О=1,05∙0,14=0,147
Затем определяем степени черноты: продуктов горения
Определяем степень развития кладки вблизи сечения 2:
Приведенный коэффициент излучения для системы «газ — кладка — металл» в сечении 2:
Удельный лучистый тепловой поток на металл в рассчитываемом сечении
При известном коэффициенте конвективного теплообмена ак2 определяем конвективную составляющую общего теплового потока:
Суммарный тепловой поток на металл в сечении 2 составит
Полагаем, что тепловая мощность низа печи составляет 50 % от общей, т.е. отношение этих мощностей равно
Используя это отношение, по прил. 9 находим = 0,58 и прогреваемые толщины слитка: сверху SB =0,580,35 = 0,203 м и снизу 5„ =0,35 -0,203 = 0,147 м.
Определяем минимальную температуру по сечению слитка перед его заходом на сплошной под
куда подставили из прил. 10 теплопроводность малоуглеродистой стали = 28 Вт/(м-К) при температуре на 100 °С ниже, чем конечная температура поверхности.
Определяем температуру массы верхней части слитка
Источник
§ 1.4. Энтальпия продуктов сгорания и воздуха
Энтальпия продуктов сгорания (кДж/кг, кДж/м 3 ) 1 кг твердого, жидкого или 1 м 3 газообразного топлива определяется как сумма энтальпий продуктов сгорания I
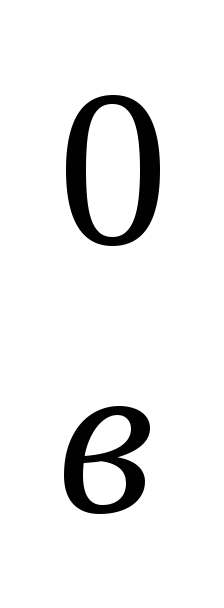
Iг=I

Энтальпия продуктов сгорания (кДж/кг, кДж/м 3 ) при αт=1 и температуре газов θ, °С определяется по формуле
I
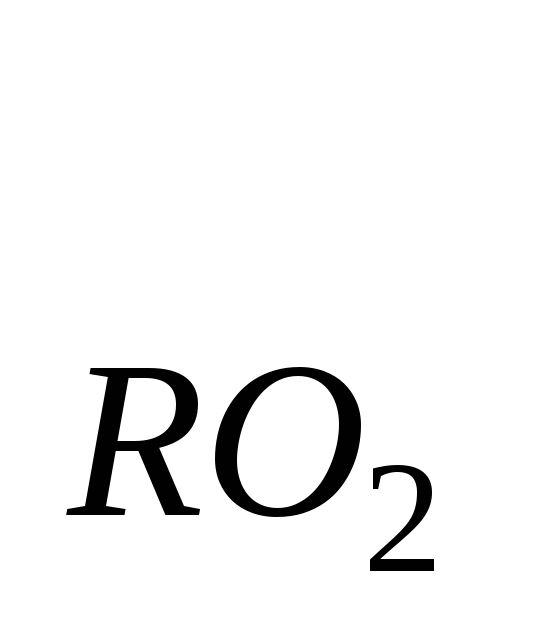




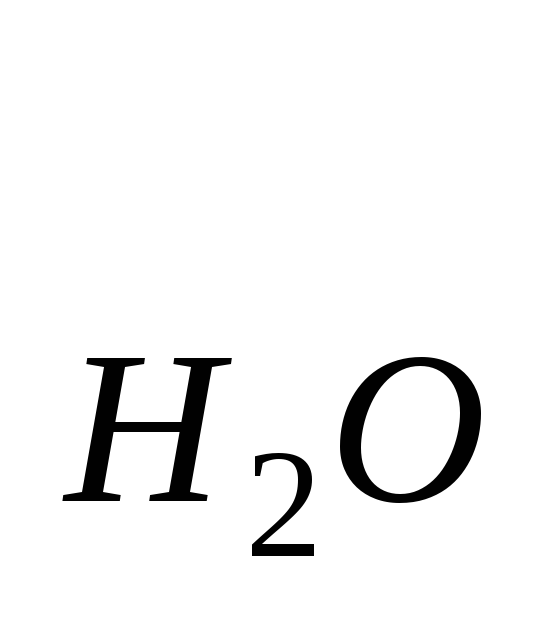
где V





Энтальпия воздуха (кДж/кг, кДж/м 3 ) при αт=1 и температуре θ, °С определяется I=V 0 (cθ)в, по формуле
I=V 0 (cθ)в, (1.62)
где V 0 — теоретический объем воздуха, м 3 /кг (м 3 /м 3 ); (cθ)в – энтальпия воздуха, кДж/м 3 .
, (1.63)
где aун — доля золы топлива, уносимой продуктами сгорания; (cθ)з — энтальпия золы, кДж/кг.
Значения энтальпий продуктов полного сгорания топлива, воздуха и золы приведены в табл. 1 (см. Приложение).
Iθ-диаграмма для продуктов сгорания. Iθ-диаграмму строят следующим образом: задают несколько значений температуры горения топлива θ и вычисляют для них энтальпии продуктов сгорания. Затем, выбрав масштабы температур и энтальпий в прямоугольной системе координат, по точкам проводят прямую I=f(θ) (рис. 1.1). По Iθ—диаграмме находят теоретическую температуру горения топлива в топке котла.
Задача 1.58. Определить энтальпию продуктов сгорания на выходе из топки, получаемых при полном сгорании 1 кг карагандинского угля марки К состава: С р =54,7%; Н р =3,3%; S=0,8%; N p =0,8%; O p =4,8%; A р =27,6%; W p =8,0%; если известно, что температура газов на выходе из топки равна θг=1000°С, доля золы топлива, уносимой продуктами сгорания, аун=0,85 и приведенная величина уноса золы сжигаемого топлива Апр.ун=4,6 кг·%/МДж. Коэффициент избытка воздуха в топке αт=1,3.
Решение: Теоретически необходимый объем воздуха определяем по формуле (1.27):
V 0 =0,089C p +0,266H p +0,033(S-O p )=0,089·54,7+0,266·3,3+0,033(0,8-4,8)=5,61 м 3 /кг.
Объем трехатомных газов, по формуле (1.33),
V

Теоретический объем азота, по формуле (1.32),
V=0,79V 0 +0,8N p /100 = 0,79·5,61+0,8·0,8/100=4,43 м 3 /кг.
Теоретический объем водяных паров, по формуле (1.35),
V=0,0124(9H p +W p )+0,0161V 0 =0,0124(9·3,3+8,0)+0,0161·5,61=0,56 м 3 /кг.
Энтальпию продуктов сгорания при αт=1 и температуре газов θг=1000°С определяем по формуле (1.61):
I
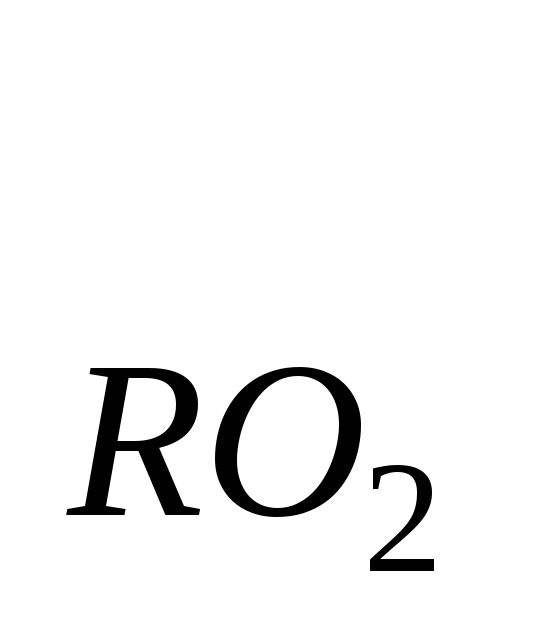



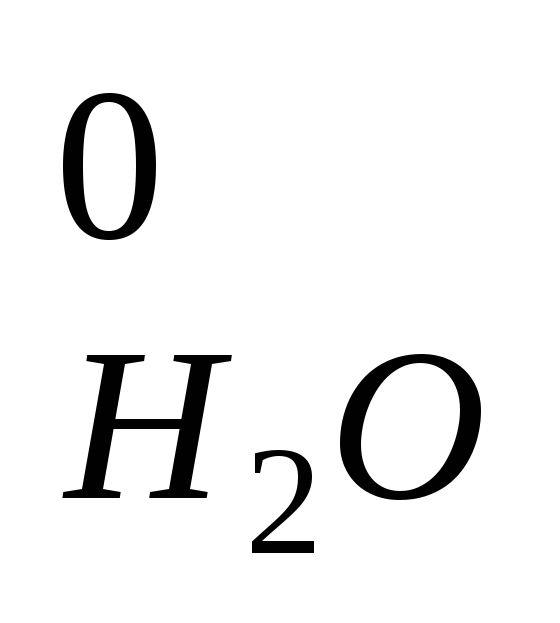

Значения (cθ)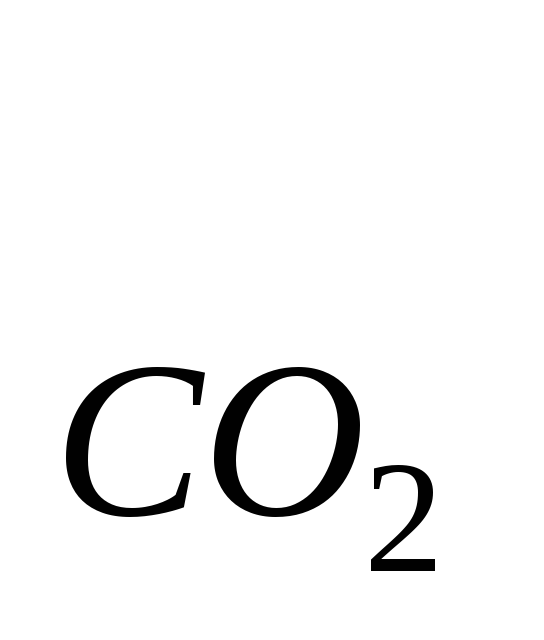
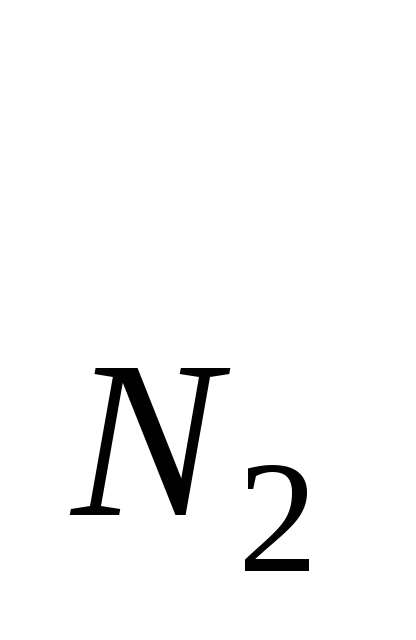
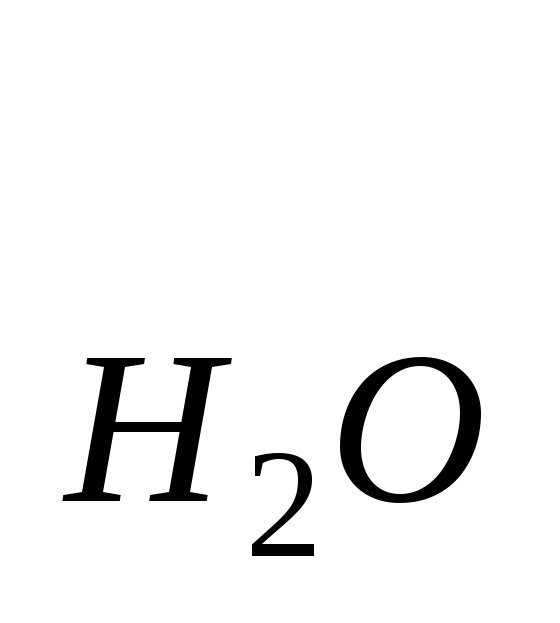
Энтальпию золы 1 кг угля при θг=1000°С определяем формуле (1.63):
=231 кДж/кг.
Значение (cθ)з при температуре газов θг=1000°С взято из табл. 1 (см. Приложение).
Энтальпию воздуха при αт=1 и температуре газов θг=1000°С находим по формуле (1.62):
I=V 0 (cθ)в=5,61·1436=8056 кДж/кг.
Значение (cθ)в при температуре газов θг=1000°С взято из табл. 1 (см. Приложение).
Энтальпию продуктов полного сгорания 1 кг угля при θг=1000°С определяем по формуле (1.60):
Iг=I

Задача 1.59. Определить энтальпию продуктов сгорания на выходе из топки, получаемых при полном сгорании 1 кг донецкого угля марки Т состава: С р =62,7%; Н р =3,1%; S=2,8%; N p =0,9%; О р =1,7%; А р =23,8%; W р =5,0%, если известно, что температура газов на выходе из топки θг=1100°С.
Ответ: I = 11 774 кДж/кг.
Задача 1.60. В топке котла сжигается 1 кг донецкого угля марки А состава: С р =63,8%; Н р =1,2%; S=l,7%; N р =0,6%; О р =1,3%; А р =22,9%; W p =8,5%. Определить энтальпию избыточного воздуха на выходе из топки при полном сгорании угля, если известно, что температура газов на выходе из топки θг=1000°С. Коэффициент избытка воздуха в топке αт=1,3.
Ответ: Iв =2604 кДж/кг.
Задача 1.61. Определить энтальпию продуктов сгорания на выходе из топки, получаемых при полном сгорании 1 м 3 природного газа Газлинского месторождения состава: СО2=0,4%; СН4=94,0%; С2Н6=2,8%; С3Н8=0,4%; С4Н10=0,3%; C5H12=0,l%; N2=2,0%, если известно, что температура газов на выходе из топки θг=1000°С. Коэффициент избытка воздуха в топке αт=1,1.
Ответ: Iг=18 034 кДж/м 3 .
Задача 1.62. Определить энтальпию избыточного воздуха на выходе из топки при полном сгорании 1 м3 природного газа Шебелинского месторождения состава: СО2=0,1%; СН4=92,8%; С2Н6=3,9%; С3Н8=1,0%; С4H10=0,4%; С5Н12=0,3%; N2=l,5%, если известно, что температура газов на выходе из топки θг=1000°С. Коэффициент избытка воздуха в топке αт=1,1.
Ответ: Iв=1431 кДж/м 3 .
Задача 1.63. Определить энтальпию продуктов сгорания на выходе из топки, получаемых при полном сгорании 1 кг высокосернистого мазута состава: С р =83,0%; Н р =10,4%; S=2,8%; О р =0,7%; А р =0,1%; W p =3,0%, если известно, что температура газов на выходе из топки θг=1100°С. Коэффициент избытка воздуха в топке αт=1,15.
Ответ: Iг=21 377 кДж/кг.
Задача 1.64. Определить энтальпию избыточного воздуха и золы на выходе из топки при полном сгорании 1 кг донецкого угля марки Г состава: C p =55,2%; Н р =3,8%; S=3,2%; N p =1,0%; О р =5,8%; А р =23,0%; W p =8,0%, если известно, что температура газов на выходе из топки θг=1100°С, доля золы топлива, уносимой продуктами сгорания, аун=0,85 и приведенная величина уноса золы сжигаемого топлива Апр.ун=3,72 кг·%/МДж. Коэффициент избытка воздуха в топке αт=1,3.
Ответ: Iв=2790 кДж/кг; Iз= 214 кДж/кг.
Задача 1.65. В топке котла сжигается 1 кг карагандинского угля марки К состава: С р =54,7%; Н р =3,3%; S=0,8%; N p =0,8%; О р =4,8%; А р =27,6%; W p =8,0%. Построить Iθ-диаграмму для продуктов сгорания в интервале температур горения топлива 600. 2000°С. Коэффициент избытка воздуха в топке αт=1,3.
Решение: Теоретически необходимый объем воздуха определяем по формуле (1.27):
V 0 =0,089C p +0,266H p +0,033(S-О р )=0,089·54,7+0,266·3,3+0,033(0,8-4,8)=5,61 м 3 /кг.
Объем трехатомных газов находим по формуле (1.33):
V

Теоретический объем азота определяем по формуле (1.32):
V
Теоретический объем водяных паров находим по формуле (1.35):
V=0,0124(9H p +W p )+0,0161V 0 =0,0124(9·3,3+8)+ +,0161·5,61=0,56 м 3 /кг.
Энтальпию продуктов сгорания 1 кг угля при θг=600°С определяем по формуле (1.60):
Iг=I




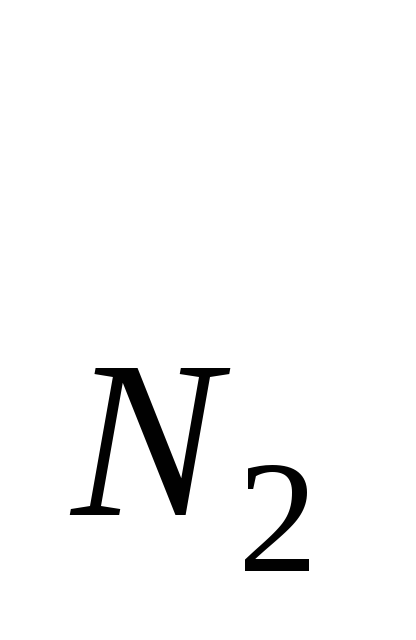



Значения (cθ)
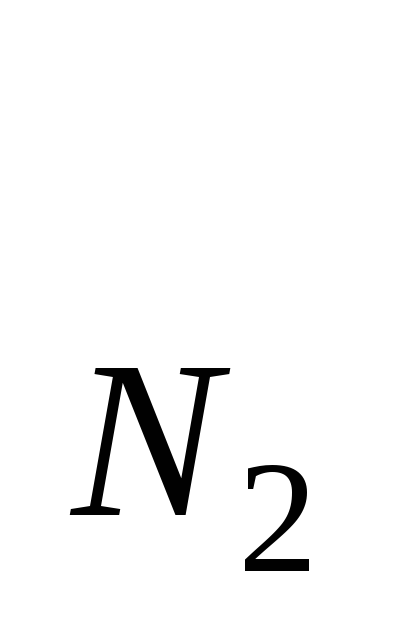

Iг=I
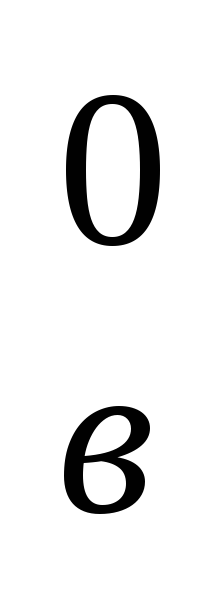


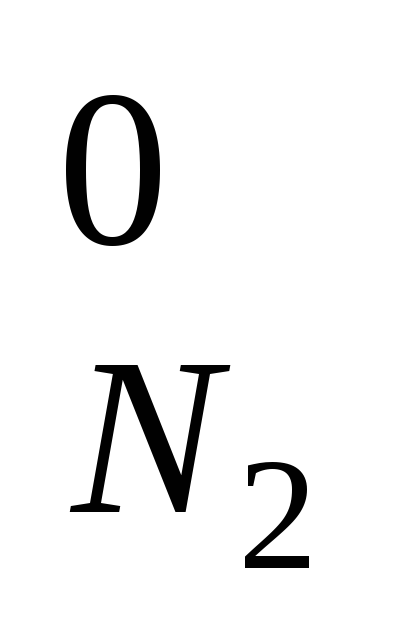



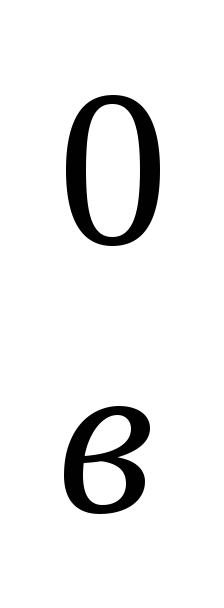
Значения (cθ)


Iг=I








По найденным значениям энтальпий продуктов сгорания строим Iθ-диаграмму (рис. 1.2).
Источник
Энтальпия воздуха и продуктов сгорания котельного топлива. Теплоемкость уходящих дымовых газов.
Энтальпия воздуха и продуктов сгорания 1 кг твердого, жидкого или 1 м 3 газообразного топлива определяется по сумме энтальпий газообразных продуктов сгорания, входящих в состав дымовых газов.
I в ° = α ּV в ° ּСв ּ t в , (1)
где Св — теплоемкость воздуха, м 3 • °С, при его температуре t в , ˚С.
Vв ° — теоретический объем воздуха,
a — коэффициент избытка воздуха ,
Энтальпия газообразных продуктов сгорания, кДж/м 3 (при α = 1),
Iг° = (V R о2 ּ Ссо2 + V N 2 ּ С N 2 + V н2оּСн2о) ּ tг (2)
где Ссо2, СN2 Сн2о — средние объемные теплоемкости двуокиси углерода, азота и водяных паров при постоянном давлении и температуре, кДж/(м 3 ּ°С).
Энтальпия дымовых газов, кДж/м 3 , при α > 1
Теплоемкость газов изменяется в зависимости от их температуры. Средние объемные значения теплоемкости для воздуха, водяного пара и дымовых газов приведены в таблице 14.
Таблица 14. Средняя объемная теплоемкость газов при постоянном давлении и нормальных условиях
Источник