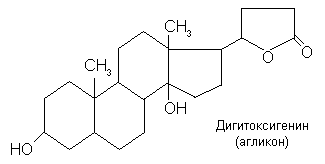
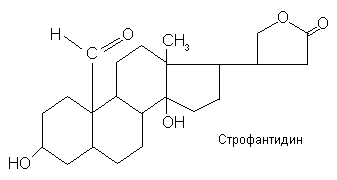
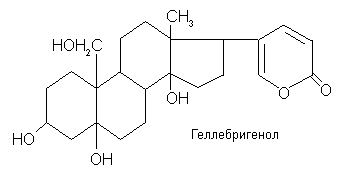
42. Сердечные гликозиды: классификация, строение, физико-химические свойства, способы выделения из лрс.
Определение. Кардиотоническими гликозидами называют вещества растительного, реже животного происхождения, агликоны которых являются стероидами – производными циклопентанпергидрофенантрена, имеющими у С17 ненасыщенное пяти- или шестичленное лактонное кольцо, и ооказывающими специфическое действие на сердечную мышцу. Классификация. Сердечные гликозиды по их молекулярной структуре классифицируют на подгруппы: карденолиды: а) наперстянковые,б) строфантовые, в) строфантидоловые;
Физико-химические свойства сердечных гликозидов. В чистом виде выделенные из ЛРС сердечные гликозиды представляют собой бесцветные или бело-кремовые кристаллические вещества без запаха и горького вкуса. Для них характерна определенная точка плавления (около 200ºС) и оптическая активность (обусловленная присутствием в молекуле гликозильной части), многие сердечные гликозиды флуоресцируют в ультрафиолетовом свете.
Сердечные гликозиды плохо растворимы в органических растворителях (хлороформе, эфире), но хорошо растворимы в воде, а еще лучше – в водных растворах этанола и метанола. Чем длиннее сахарная цепочка кардиогликозидов, тем их растворимость в воде лучше. Агликоны же, наоборот, лучше растворимы в неполярных растворителях и нерастворимы в воде.
Молекулы сердечных гликозидов легко гидролизуются ферментами и в кислых значениях рН, в результате чего их гликозильная цепочка ступенчато или полностью отщепляется от генина. Как правило, при ферментном гидролизе углеводный фрагмент расщепляется постепенно и мягко, одно звено за другим, а при кислотном – более резко, часто с отрывом больших кусков или даже всей сахаристой цепочки от агликона. Многие сердечные гликозиды достаточно быстро окисляются кислородом воздуха. К разрушению сердечных гликозидов приводит и нахождение их при повышенных значениях температуры. В щелочной среде, вследствие наступающего раскрытия лактонного кольца, сердечные гликозиды теряют свою кардиотоничекую активность и превращаются в биологически малоактивные изо-соединения. Таким образом, если кислая среда ведет к отделению сахаристой части от агликона, то щелочная приводит к утере сердечными гликозидами своих специфических кардиотонических свойств. Лучше всего эти свойства у сердечных гликозидов сохраняются при нейтральных показаниях рН. Эти обстоятельства следует учитывать при заготовке и сушке ЛРС и при технологии выделения из него кардиогликозидов.
Выделение сердечных гликозидов из ЛРС. На практике обычно используют упрощенный способ выделения этих веществ. Для этого навеску измельченного лекарственного растительного сырья (например, листьев ландыша) подвергают в течение суток экстракции 50% или 70% этанолом. Спирт одновременно препятствует ферментативному гидролизу сердечных гликозидов, отделению сахаристой части от агликона. В этих концентрациях спирта растворятся и гликозиды, и агликоны сердечных гликозидов. Полученный экстракт выпаривают под вакуумом при 50-60ºС (выпаривание при более высокой температуре ведет к инактивации сердечных гликозидов – потере ими качественных свойств). Густой экстракт разбавляют водой и многократно обрабатывают хлороформом или другим органическим растворителем. Очистку можно проводить методом фильтрации через колонку с окисью алюминия, которая при этом поглощает хлорофилл, флавоноиды, смолистые и другие липофильные балластные вещества, делая раствор более прозрачным. Затем проводят разделение суммы сердечных гликозидов на хроматографических колонках с Al2O3, селикагелем или другим сорбентом. Образующиеся на сорбенте нужные зоны затем берут и элюируют определенным растворителем.
Источник
2 Вопрос:
Гликозиды — природные соединения, производные циклических форм сахаров, которые в процессе гидролиза распадаются на продукты, среди которых всегда есть сахаристое вещество.
Слово «гликозиды» произошло от греческого слова «glycos» — сладкий. В состав гликозидов входят гексозы (моносахариды, содержащие 6 углеродных атомов) и пентозы (содержащие 5 углеродных атомов), а также их окисленные производные — уроновые кислоты. Циклические формы моносахаридов могут быть в пиранозной форме (в основе их структуры лежит пирановое кольцо) и фуранозной форме (в основе — фурановое кольцо). рме (называется глюкофуранозой).
Образование гликозидной связи происходит за счет полуацетальных гидроксильных групп моносахаридов, поэтому их называют гликозидными гидроксилами. В зависимости от конфигурации полуацетального гидроксила у C1 различают альфа— и бета-формы.
В зависимости от того, какая форма моносахаридов участвует в образовании гликозидов, различают альфа— и бета-гликозиды. В растениях бета-гликозиды встречаются чаще, они более устойчивы к гидролизу и фармакологически более активны.
Классификация гликозидов
Группа гликозидов очень разнородная. В зависимости от продуктов гидролиза гликозиды делятся на гомогликозиды (полисахариды) и гетерогликозиды (гетерозиды).
При гидролизе гомогликозидов среди продуктов гидролиза присутствуют только моносахариды и их производные. В свою очередь гомогликозиды по продуктам гидролиза делятся на гомополисахариды и гетерополисахариды.
Гомополисахариды при гидролизе дают один вид сахара. Например: крахмал гидролизуется до глюкозы. Гетерополисахариды при гидролизе дают различные моносахариды. Например: инулин гидролизуется до фруктозы и глюкозы.
При гидролизе гетерозидов среди продуктов гидролиза кроме сахаров присутствует органическое вещество неуглеводного характера. Это вещество называют агликоном, или генином. Сахаристую часть называют гликон, или гликозил. Таким образом, гетерозиды — это природные соединения, распадающиеся вследствие гидролиза на углеводную часть и агликон.
- по углеводной части молекулы;
- по характеру гликозидной связи;
- по структуре агликона.
Классификация гетерозидов по углеводной части молекулы.
В зависимости от количества моносахаридов в углеводной части молекулы различают:
1) монозиды — углеводный компонент содержит моносахарид;
2) биозиды — углеводный компонент содержит дисахарид;
3) триозиды — углеводный компонент содержит трисахарид;
4) тетразиды — углеводный компонент содержит тетрасахарид;
5) олигозиды — углеводный компонент содержит олигосахарид (5 и более моносахаридов).
Гликозиды, содержащиеся в живом растении, называются первичными, или нативными. Они, как правило, с медицинской точки зрения наиболее ценные. При ферментативном гидролизе происходит постепенное отщепление сахаров, т.е. ступенчатый гидролиз. Гликозиды, образующиеся в процессе гидролиза, называются вторичными, третичными и т.д.
При кислотном и щелочном гидролизе идет практически одновременное расщепление всех гликозидных связей.
Классификация гетерозидов по характеру гликозидной связи.
Соединение сахарной части и агликона происходит за счет полуацетального гидроксила циклической формы сахара и водорода гидроксильной группы или других функциональных групп агликона. В зависимости от природы связывающего атома выделяют несколько типов гликозидов:
1. О-гликозиды — присоединение агликона идет через атом кислорода.
Это наиболее многочисленная группа гликозидов, они легко подвергаются гидролизу.
2. S-гликозиды (тиогликозиды) – присоединение агликона идет через атом серы.
Тиогликозиды очень устойчивы к кислотному гидролизу, но легко подвергаются ферментативному и щелочному гидролизу. S-гликозиды обычно имеют сложный агликон, который при гидролизе распадается на компоненты, в числе которых всегда имеется серосодержащее эфирное масло.
3. N-гликозиды – присоединение агликона идет через атом азота. Образуются в основном плесневыми грибами.
4. C-гликозиды – присоединение агликона идет через атом углерода.
С-гликозиды отличаются большой устойчивостью к гидролизу. Они содержатся в растениях семейств розоцветных, бобовых, крестоцветных и др.
Классификация гетерозидов по характеру агликона.
Наиболее многочисленную группу О-гликозидов классифицируют по характеру агликона.
1. Алкилгликозиды – агликонами являются алифатические углеводороды и их производные.
2. Цианогенные гликозиды — агликон содержит цианогенную, или нитрильную группу (-C≡N). Наиболее характерны для растений семейства розоцветных, подсемейства сливовых. Локализуются в семенах. В медицинской практике применяется горькоминдальная вода, которую получают из жмыха семян горького миндаля перегонкой с водяным паром.
3. Терпеновые гликозиды:
4. Стероидные гликозиды — агликонами являются производные циклопентанпергидрофенантрена:
1) кардиотонические (сердечные) гликозиды;
3) стероидные алкалоиды (гликоалкалоиды).
5. Фенольные гликозиды:
1) группа простых фенольных соединений;
5) дубильные вещества гидролизуемой группы.
6. Гликозиды неустановленного строения.
Физические и химические свойства гликозидов
Гликозиды — это твердые кристаллические или аморфные вещества, чаще бесцветные, иногда окрашенные. Некоторые гликозиды имеют специфический вкус или запах. Гликозиды большей частью растворяются или набухают в воде, растворяются в этиловом спирте слабой концентрации, нерастворимы в органических растворителях. Обладают оптической активностью.
Гликозиды в растениях находятся в растворенном виде в клеточном соке. Химические свойства многообразны и обусловлены наличием гликозидной связи и строением составляющих гликозида, т.е. сахаров и агликона.
Под действием ферментов при наличии воды гликозиды гидролизуются на составные части. Возможен гидролиз не только ферментативный, но также кислотный и щелочной.
Гликозиды и ферменты находятся в живых растениях в динамическом равновесии. При заготовке лекарственного растительного сырья клеточные мембраны теряют барьерные свойства, и ферменты и гликозиды, находившиеся в разных клетках, вступают во взаимодействие.
Оптимальной для ферментативного гидролиза является температура 30-40 °С. При 25 °С активность ферментов снижается, при 50-60 ºС ферменты инактивируются. Все это учитывают при заготовке, сушке и хранении сырья.
Источник
Характеристика сахарного компонента.
Кроме обычных сахаров — глюкозы, фруктозы, рамнозы, в сердечных гликозидах встречаются специфические дезоксисахара (обедненные кислородом): дигитоксоза — С6Н12O4 и цимароза — С6Н11O4*СН3. Сахаристые вещества присоединяются к агликон за счет спиртового гидроксила в положении 3. Длина сахарной цепочки может быть от одной молекулы до 30 сахаров. О 
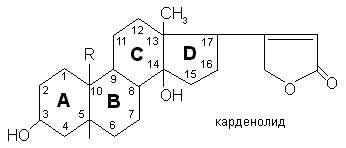
Биологическая активность сердечных гликозидов зависит от числа групп СН3 и особенно ОН у углеродных атомов «скелета». С увеличением числа гидроксильных групп повышается их растворимость в воде.
Классификация.
В зависимости от строения ненасыщенной: лактонного кольца все сердечные гликозиды делятся на две группы с пятичленным — карденолиды (гликозиды наперстянки, строфанта, ландыша, горицвета) и шестичленным — буфадиенолиды (гликозиды морозника) лактонным кольцом. В формуле карденолидов встречаются заместители: -СН3, -С-OH; в формуле буфадиенолидов заместителями могут быть -СН3, -С-OH, -СН2OН.
В зависимости от заместителя в положении C10 карденолиды подразделяются на три подгруппы.
1.Подгруппа наперстянки включает гликозиды, агликоны которых в положении С10 имеют метильную группу — СН3. Гликозиды этой подгруппы медленно всасываются и медленно выводятся из организма, обладают кумулятивным действием, например гликозид гитоксигенин.
2. Подгруппа строфанта — агликон имеет в положении 10 альдегидную группу -С-OH. Эти гликозиды быстро всасываются, быстро выводятся из организма и не обладают кумулятивным действием, например строфантидин.
3. Подгруппа объединяет сердечные гликозиды, имеющие в положении 10 спиртовую группу (-OН2OН):
Сердечные гликозиды, как и все другие гликозиды, по количеству остатков в углеводной части молекулы делят на монозиды, биозиды, триозиды и т. д.
Физико-химические свойства.
Сердечные гликозиды чаще кристаллические вещества, бесцветные или кремоватые, без запаха, горького вкуса; характеризуются определенной точкой плавления и углом вращения. Многие гликозиды обладают флюоресценцией в УФ-свете (ланатозиды наперстянки шерстистой). Сердечные гликозиды в основном мало растворимы в воде, хлороформе, но хорошо растворимы в водных растворах метанола и этанола. Агликоны сердечных гликозидов лучше растворимы в органических растворителях. Сердечные гликозиды легко подвергаются кислотному, щелочному и ферментативному гидролизу. При кислотном или щелочном гидролизе сразу происходит глубокое расщепление до агликона и cахаров.
Способы получения.
Для выделения сердечных гликозидов используют этанол и метанол, которые не вызывают гидролиза сердечных гликозидов. Качественные реакции. Проводятся с индивидуальными веществами или очищенным извлечением из растительного сырья: на углеводную часть молекулы (реакция Келлер-Килиани); на стероидное ядро; на лактонное ненасыщенное кольцо (реакция Балье) — с пикриновой кислотой в щелочной среде. В полевых условиях пользуются пикратной бумагой, в которую завертывают свежее растение и надавливают плоскогубцами; появление красного окрашивания на бумаге характеризует присутствие сердечных гликозидов.
Источник