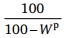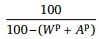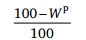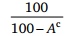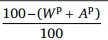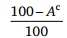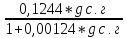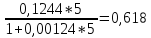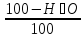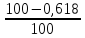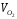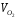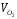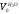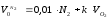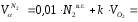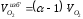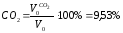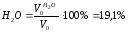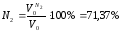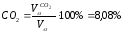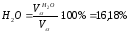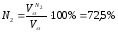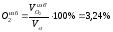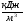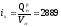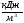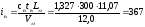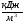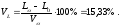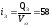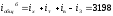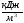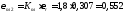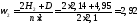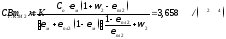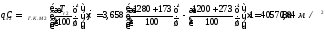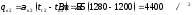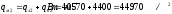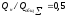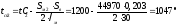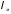- Топливо и его сжигание. Состав, расчет горения топлива.
- 1.1. Элементарный состав твердого, газообразного и жидкого топлива
- 1. Расчет горения топлива
- 1.5 Расчет теплоты сгорания природного газа
- 1.6 Расчет температур горения
- 2 Определение тепловых потоков и температур металла по длине печи
- 2.1. Определение теплового потока и температур металла в сечении 2
Топливо и его сжигание. Состав, расчет горения топлива.
1.1. Элементарный состав твердого, газообразного и жидкого топлива
В базовой и промышленной энергетике для получения электрической и тепловой энергии используется в основном топливо органического происхождения.
Все виды органического топлива (горючие) представляют собой углеводородные соединения, в которые входят небольшие количества других веществ.
К твердому топливу относят: антрацит, каменный и бурый уголь, торф, дрова, сланцы, отходы лесопильных заводов и деревообделочных цехов, а также растительные отходы сельскохозяйственного производства — солому, костру, лузгу и др.
К жидкому топливу относят нефть, а также различные продукты ее переработки: бензин, керосин, лигроин, разнообразные масла и остаточный продукт нефтепереработки нефти — мазут.
До 70 % и более видов жидкого топлива используется на транспорте — авиационном, автомобильном, специальном водном, железнодорожном (тепловозы), около 30 % сжигается в виде мазута на тепловых электростанциях и в промышленных котельных.
К газообразному топливу относят природный газ, добываемый из недр земли, попутный нефтяной газ, газообразные отходы металлургического производства (коксовый и доменный газ), крекинговый газ, а также генераторный газ, получаемый искусственным путем из твердого топлива в особых газогенераторных установках.
Топливо в том виде, в каком оно поступает для сжигания в топки котлов или в двигатели внутреннего сгорания, называется рабочим.
В общем случае в состав рабочего (твердого или жидкого) топлива входят углерод С, водород Н, кислород О, азот N и летучая сера S, а также негорючие минеральные примеси — зола А и влага W.
Для рабочей массы топлива имеет место равенство:
C p + H p + O p + N p + S p + A p + W p = 100 %, (1.1)
где С Р , Н Р , О Р и т. д. — элементы рабочего топлива, % общей массы топлива.
Влага, содержащаяся в топливе совместно с золой, называется балластом топлива.
В естественных видах ископаемого твердого топлива встречается сера трех разновидностей:
1) органическая S о , связанная с другими элементами топлива С, Н, N и О в виде сложных органических соединений;
2) колчеданная S к в виде пирита, колчедана FeS2;
3) сульфатная S сульф в виде солей серной кислоты (гипс, FeSО4и др.). Сульфаты представляют собой высокие окислы серы, поэтому находящаяся в них сера гореть не может. Присутствующие в топливе органическая и колчеданная серы сгорают, образуя токсичный сернистый ангидрид SO2и (в небольших количествах) еще более токсичный серный ангидрид SO3. Выброс их с продуктами сгорания вызывает загрязнение воздушного бассейна.
Органическая и колчеданная сера образуют вместе летучую горючую серу Sл. Общее содержание серы в топливе
Sобщ = S о + S к + S сульф = Sл + S сульф . (1.2)
В горючую часть топлива входит только летучая сера, остальная сера в горении участия не принимает и может быть отнесена к балласту топлива.
Для правильного представления тепловых свойств топлива вводится понятие горючей массы, для которой
С г + Н г + О г + N г + S г л= 100 %, (1.3)
где индекс вверху показывает, что процентный состав отдельных элементов отнесен к горючей массе.
Название «горючая масса» носит условный характер, так как действительно горючими ее элементами являются только углерод, водород и сера. Углерод — преобладающий компонент твердых и жидких топлив, в топливах его обычно содержится от 50 до 95 %, тогда как содержание водорода Н г колеблется в пределах от 1 до 11 %, а серы S г — от 0 до 8 %. Горючую массу можно характеризовать как топливо, не содержащее золы и в абсолютно сухом состоянии. Содержание азота в горючей массе твердых топлив обычно составляет 1—2 % по массе. Несмотря на столь малое количество, азот является весьма вредным компонентом, поскольку при сгорании азотсодержащих соединений в высокотемпературных топках образуются сильнотоксичные оксиды NО и NO2(они образуются также и из атмосферного азота, но в
Для топлива, содержащего большое количество влаги (бурый уголь, торф, дрова, некоторые растительные отходы), в некоторых случаях удобно использовать понятие сухой массы, т. е. характеризовать состав абсолютно сухого топлива суммой элементов С с , Н с , О с , N с , S с и А с . При этом
С с + Н с + О с + N с + S с + Ас = 100 %, (1.4)
где индекс показывает, что процентный состав отдельных элементов отнесен к сухой массе.
Для взаимного пересчета массы топлива в соответствии с понятием о массах топлива служат формулы, объединенные в табл. 1.1.
Таблица 1.1. Формулы для пересчета состава топлива с одной массы на другую
Зольность топлива. Золой называют твердый негорючий остаток, остающийся после сжигания топлива в атмосфере воздуха. Зола может быть в виде сыпучей массы с плотностью в среднем 600 кг/м 3 и в виде сплавленных пластин и кусков, называемых шлаками, с плотностью до 800 кг/м 3 .
В состав золы большинства видов твердого топлива входят: глинозем Al2O3, кремниевая кислота SiO2, известь СаО, магнезия MgO, щелочи Na2O, окислы железа FeO и Fe2О3.
Влажность твердого топлива. Влажность твердого топлива W р доходит
до 50 % и более и определяет экономическую целесообразность использования данного горючего материала и возможность его сжигания. Влага снижает температуру в топке и увеличивает объем дымовых газов. Увеличенный объем дымовых газов требует дополнительной энергии на их удаление.
Очевидно, что влага является балластной примесью, так как уменьшает тепловую ценность исходного топлива. Кроме того, часть теплоты, выделяемой топливом при его сгорании, расходуется на испарение влаги.
Летучие вещества. При нагревании твердого топлива без доступа воздуха его органическая масса разлагается, в результате чего образуются газы, водяные и смоляные пары и углесодержащий остаток. Суммарное количество выделяющихся летучих веществ увеличивается с увеличением температуры и времени выдержки, этот процесс в основном заканчивается при 700—800 о С. Выход летучих веществ V г , в процентах на горючую массу, является важнейшей характеристикой горючей массы твердого топлива и уменьшается по мере увеличения его возраста. Чем больше выход летучих веществ, т.е. чем больше топлива превращается при нагревании в горючий газ, тем проще зажечь это топливо и легче поддерживать устойчивое горение. Органическая часть древесины и горючих сланцев при нагревании без доступа воздуха почти целиком переходит в летучие вещества
(V г = 85÷90%), в то время как у антрацитов V г = 3÷4 %. Именно большой выход летучих веществ определяет хорошую горючесть древесины.
Состав некоторых видов твердого топлива представлен в табл. 1.2.
Таблица 1.2. Примерный состав и теплотехнические характеристики горючей массы основных видов твердого топлива
Выход летучих веществ, V г , %
Низшая теплота сгорания, МДж/кг
Источник
1. Расчет горения топлива
Сжигается природный газ, элементарный состав которого на сухую массу, %:
Влагосодержание сухого газа составляет g с.г. =5 г ∕ м 3 .
Температура подогрева воздуха tв=300 ° С.
Коэффициент избытка воздуха α=1,2.
Влажность воздуха q св =14.
Механический недожог отсутствует.
1.2 Пересчет состава газа на рабочую (влажную) массу
Рассчитаем процентное содержание водяных паров в 1 м 3 природного газа:
H2O в . г = ;
H2O в.г =%
Пересчитаем состав газа на рабочую массу по формуле:
x в.г =x c .г % ;
CH4 в.г = 98,3*= 96,6%;
1.3 Расчет количества кислорода и воздуха для сжигания 1 м 3 газа
Найдем объем кислорода, необходимый для окисления горючих составляющих природного газа.
=0,01[(m+n∕ 4)∑CmHn в.г. ];
=0,01(2·96,6+3.5·0,129+5·0.009)=1,939 м 3 /м 3 .
Находим количество воздуха при α=1, необходимое для сжигания 1 м 3 природного газа, используя соотношение азота и кислорода в воздухе К=3,76:
L0 с.в =(1+K)
Практически введенное количество воздуха при α=1,2 составит:
1.4 Расчет объема и состава продуктов сгорания при сжигании 1 м 3 газа
Найдем объем продуктов сгорания при α=1
= 0,01[CH4 в. + 2C2H6 в.г +3C3H8 в.г +4C4H10 в.г ] =0,969 м 3 /м 3 ;
= 0,01[H2O в.г +2CH4 в.г +3C2H6 в.г +4С3H8 в.г +5C4H10 в.г ]=1,942 м 3 /м 3 ;
= 7,26 м 3 /м 3 ;
V0=0,969 +1,942 +7,26 =10,17м 3 /м 3 .
Выход продуктов сгорания при α=1,2 изменится только на величину содержания азота, внесенного с избытком воздуха, и на величину избыточного кислорода:
8,7 м 3 /м 3 ;
=0,386 м 3 /м 3 ;
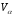
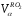
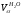
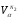
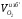
Состав продуктов сгорания при α=1:
Состав продуктов сгорания при α=1,2:
1.5 Расчет теплоты сгорания природного газа
В формулу для Qн р , подставим горючие составляющие, которые указаны в исходных данных и пересчитаны на рабочую массу:
Qн р =34666
1.6 Расчет температур горения
Определим химическую энтальпию топлива:
Физическая энтальпия подогретого воздуха, где св взята из прил. 2.
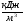
Общая энтальпия продуктов сгорания составит:
Используем приложение 1 — диаграмму itи вычисляем содержание избыточного воздуха в продуктах сгорания:
Теоретическая температура горения природного газа tα т =1950°С.
Энтальпия химического недожога
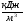
Общее балансовое теплосодержание продуктов сгорания:
Балансовая температура горения природного газа tα т =1970°С.
2 Определение тепловых потоков и температур металла по длине печи
2.1. Определение теплового потока и температур металла в сечении 2
Для расчета лучистого теплообмена необходимо знать эффективную толщину излучающего слоя печных газов вблизи сечение 2, м:
Высота рабочего пространства над заготовками найдена с использованием размеров, указанных на рис. 1.1:
H2 = Н— S=2,54-0,3= 2,24 м, а ширина печи D =2,6 м оставлена без изменения.
Задаем температуру газов в сечении 2 tг2 = 1280°С. Затем из расчета объема и состава продуктов сгоранияопределяем содержание Н20 и С02.
Получаем содержание излучающих газов, а печной атмосфере, а именно:
0,01 Sэф Н2О = 0,01∙ 2,21∙ 11,66= 0,25 атм∙м,
которые необходимы для определения степени черноты при с помощью прил. 6,7 и 8 заданной температуре газов tг2 = 1280°С: водяного пара εСО2 =0,096; εН2О=β∙ εН2О=1,05∙0,14=0,147
Затем определяем степени черноты: продуктов горения
Определяем степень развития кладки вблизи сечения 2:
Приведенный коэффициент излучения для системы «газ — кладка — металл» в сечении 2:
Удельный лучистый тепловой поток на металл в рассчитываемом сечении
При известном коэффициенте конвективного теплообмена ак2 определяем конвективную составляющую общего теплового потока:
Суммарный тепловой поток на металл в сечении 2 составит
Полагаем, что тепловая мощность низа печи составляет 50 % от общей, т.е. отношение этих мощностей равно
Используя это отношение, по прил. 9 находим = 0,58 и прогреваемые толщины слитка: сверху SB =0,580,35 = 0,203 м и снизу 5„ =0,35 -0,203 = 0,147 м.
Определяем минимальную температуру по сечению слитка перед его заходом на сплошной под
куда подставили из прил. 10 теплопроводность малоуглеродистой стали = 28 Вт/(м-К) при температуре на 100 °С ниже, чем конечная температура поверхности.
Определяем температуру массы верхней части слитка
Источник