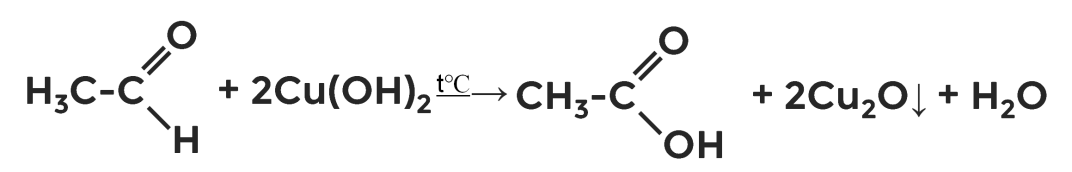- Конспект урока: Углеводы
- Моносахариды
- Дисахариды
- Строение моносахаридов: глюкоза и фруктоза
- Физические свойства углеводов
- Химические свойства моносахаридов. Глюкоза
- Свойства многоатомных спиртов
- Свойства альдегидов
- Брожение глюкозы
- Химические свойства дисахаридов. Сахароза
- Химические свойства полисахаридов. Крахмал и целлюлоза
- Получение углеводов
- Применение углеводов. Нахождение в природе
Конспект урока: Углеводы
Само название «углеводы» говорит о том, что это соединения с общей формулой C n H 2 n O n или C n ( H 2 O ) n , которые состоят из углерода и воды.
Содержание углеводов в живых клетках различно. В животных колеблется от 1 до 5 %. В растениях содержание углеводов заметно выше — до 70 % в некоторых запасающих органах, например, в клубнях картофеля. Кроме высокого содержания углеводов для растений характерно и большее их разнообразие.
Углеводы делятся на две группы: простые углеводы, или моносахариды (сахара), и сложные углеводы, или полисахариды. Часто выделяют ещё и третью группу — олигосахариды, состоящие из двух-десяти моносахаридных остатков. Чаще всего это дисахариды.
Моносахариды
Простые углеводы представляют собой многоатомные спирты, содержащие гидроксильную группу у каждого атома углерода, кроме одного, несущего альдегидную, или кетогруппу. Эта группа обычно взаимодействует с одной из спиртовых групп молекулы, образуя циклическую форму.
Моносахариды , обычно встречающиеся в живых организмах, содержат пять или шесть атомов углерода.
Пентозы (5 атомов углерода) входят в состав нуклеиновых кислот (рибоза и дезоксирибоза) ; гексозы (6 атомов углерода): глюкоза и фруктоза , которые являются наиболее распространёнными моносахаридами. Они хорошо растворимы в воде, образуют кристаллы и имеют сладкий вкус.
Дисахариды
Дисахариды — это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединённых друг с другом за счёт взаимодействия гидроксильных групп.
Примером наиболее распространённых в природе дисахаридов является сахароза (свекловичный или тростниковый сахар). Молекула сахарозы состоит из остатков глюкозы и фруктозы.Полисахариды
Молекулы моносахаридов могут образовывать связи между собой с потерей молекулы воды. В результате образуются полисахариды . Полисахариды нерастворимы в воде и не имеют сладкого вкуса. Так как к одному остатку моносахарида может быть присоединено несколько других остатков, полисахариды могут иметь разветвлённую структуру. В живых организмах наиболее широко распространены полимеры глюкозы — крахмал, гликоген и целлюлоза.
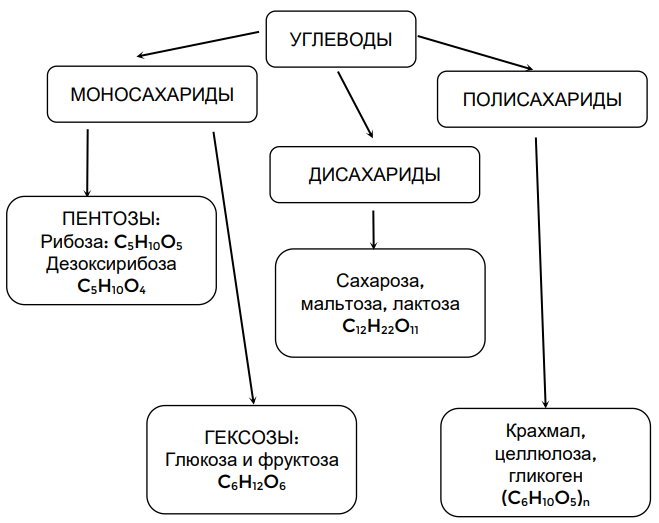
Классификацию углеводов с примерами можно представить в виде следующей схемы (рис. 1).
Рисунок 1. Классификация углеводов
Строение моносахаридов: глюкоза и фруктоза
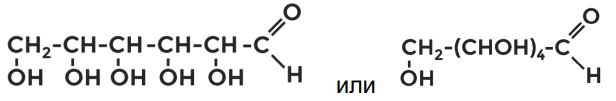
Глюкоза и фруктоза имеют одинаковые молекулярные формулы: C 6 H 12 O 6 . Они являются изомерами. Глюкоза — это альдегидоспирт :
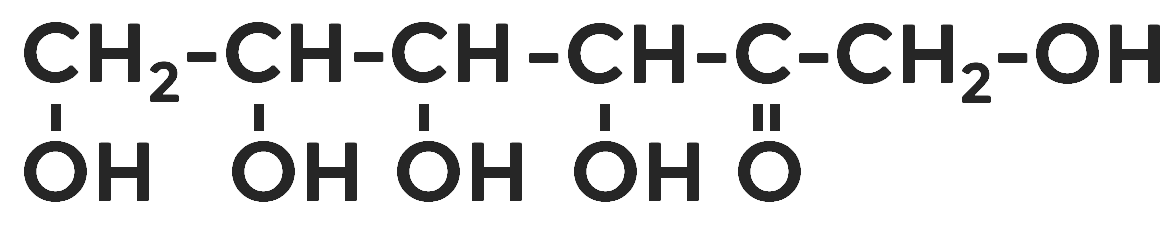
Фруктоза является кетоноспиртом.
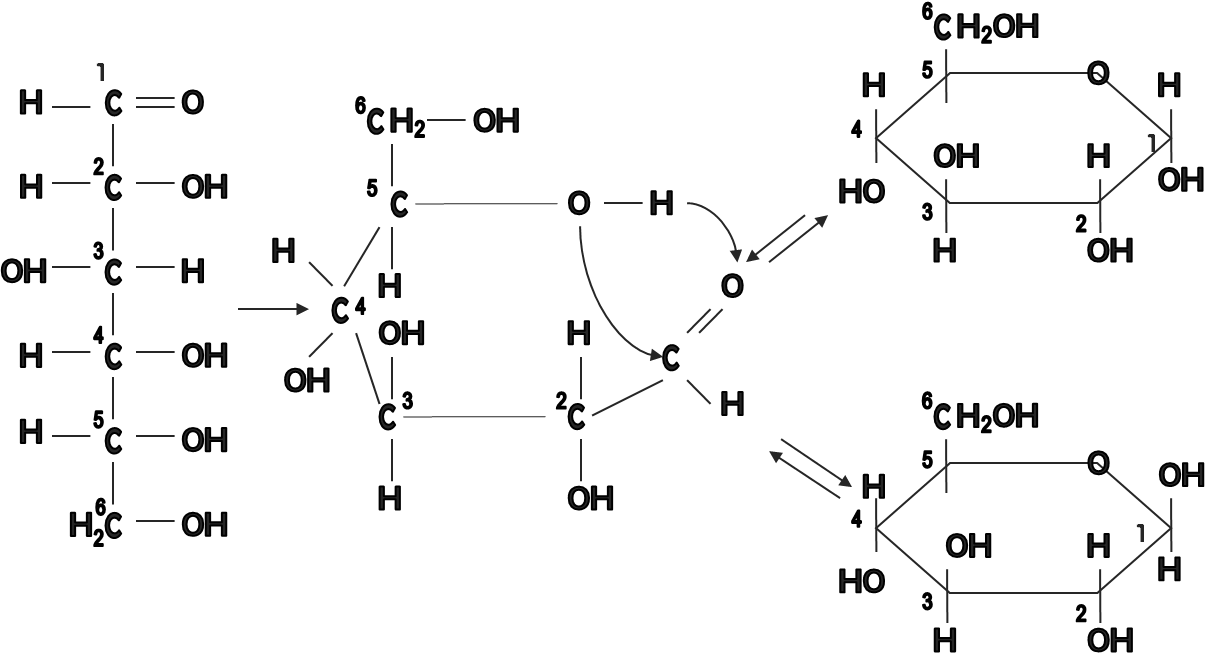
Глюкоза (как и фруктоза) может иметь циклические формулы (рис. 2).
Рисунок 2. Образование циклических форм глюкозы
Физические свойства углеводов
Моносахариды и дисахариды являются кристаллическими веществами, сладкими на вкус, хорошо растворимы в воде. Полисахариды хуже растворяются в воде и не имеют сладкого вкуса.
Химические свойства моносахаридов. Глюкоза
Моносахариды глюкоза и фруктоза содержат несколько гидроксильных групп, поэтому для них будут характерны свойства многоатомных спиртов. Кроме этого, они проявляют свойства карбонильных соединений, так как глюкоза содержит альдегидную группу, а фруктоза — кетогруппу.
Свойства многоатомных спиртов
Рисунок 3. Взаимодействие глюкозы с гидроксидом меди (II) без нагревания
Глюкозу можно представить как пятиатомный альдегидоспирт, а фруктозу — как пятиатомный кетоспирт.
Следовательно, они реагируют с гидроксидом меди (II) без нагревания с образованием раствора ярко-синего цвета. Это является качественной реакцией на многоатомные спирты (рис. 3).
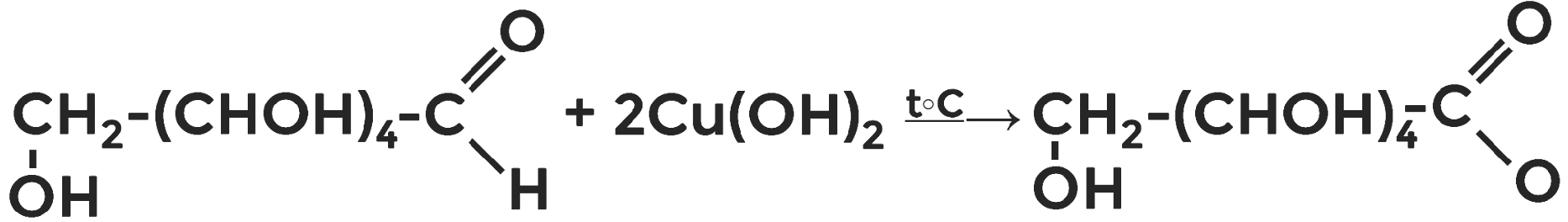
Рисунок 4. Взаимодействие глюкозы с гидроксидом меди (II) при нагревании
Фруктоза, будучи также многоатомным спиртом, реагирует с гидроксидом меди (II) аналогично (рис. 4).
Свойства альдегидов
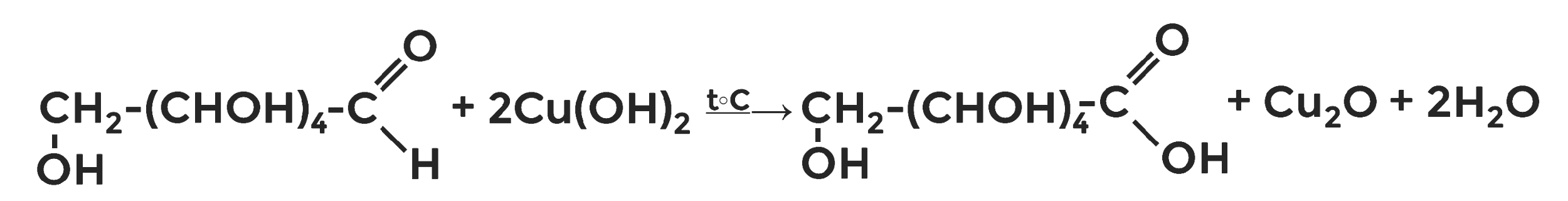
Глюкоза проявляет свойства альдегида. Поэтому при её нагревании с гидроксидом меди (II) образуется глюконовая кислота и характерный осадок оксида меди (I) красно-коричневого цвета.
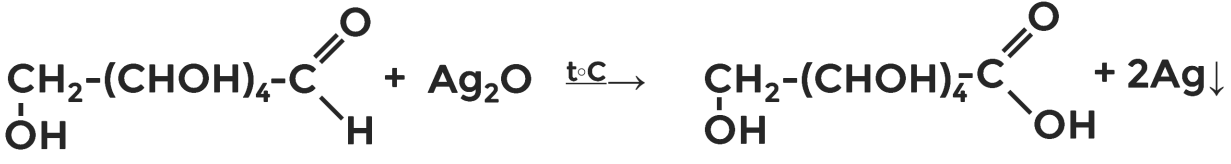
С аммиачным раствором оксидом серебра (I) и глюкозы мы наблюдаем под действием температуры уже известную вам реакцию «серебряного зеркала».
Рисунок 5. Реакция «серебряного зеркала» с глюкозой
Фруктоза, будучи кетоноспиртом, не вступает в реакции окисления.
Глюкоза (как и фруктоза) восстанавливается водородом до шестиатомного спирта сорбита, который применяется как сахарозаменитель.
Брожение глюкозы
Брожение относится к специфическим свойствам глюкозы. Она подвергается спиртовому брожению в присутствии дрожжей:
C 6 H 12 O 6 → C 2 H 5 OH + CO 2 ↑ .
Молочнокислому брожению , осуществляемому молочнокислыми бактериями:
C 6 H 12 O 6 → 2 CH 3 — CH ( OH ) — COOH .
Кроме этого, существует также маслянокислое брожение , которое инициируют маслянокислые бактерии:
C 6 H 12 O 6 → CH 3 — CH 2 — CH 2 — COOH + 2 H 2 ↑ + 2 CO 2 ↑ .
Химические свойства дисахаридов. Сахароза
Дисахариды состоят из двух молекул глюкозы: мальтоза, лактоза (глюкоза + галактоза) или из глюкозы и фруктозы — сахароза.
Главная особенность дисахаридов, которые, кстати, являются многоатомными спиртами, — способность подвергаться гидролизу при нагревании в присутствии кислоты. Так, сахароза гидролизуется на глюкозу и фруктозу:
C 12 H 22 O 11 + H 2 O → C 6 H 12 O 6 + C 6 H 12 O 6 .
Химические свойства полисахаридов. Крахмал и целлюлоза
Полисахариды крахмал и целлюлоза имеют похожую молекулярную формулу ( C 6 H 10 O 5 ) n , так как состоят из молекул глюкозы. Отличаются расположением структурных звеньев и их количеством.
Крахмал подвергается кислотному гидролизу, в результате которого сначала образуются декстрины (участки крахмала с меньшим числом звеньев), затем дисахарид мальтоза, потом глюкоза.
( C 6 H 10 O 5 ) n + nH 2 O → 0 , 5 nC 12 H 22 O 11 → nC 6 H 12 O 6
У целлюлозы возможны подобные процессы, но протекают они значительно сложнее по сравнению с крахмалом.
Получение углеводов
Вы знаете, что в природе углеводы, в первую очередь глюкоза, образуются в результате фотосинтеза в зелёных частях растений:
6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2 .
Углеводы являются источником энергии для животных и самих растений. «Сгорая» в кислороде, они образуют углекислый газ и воду:
C 6 H 12 O 6 + 6 O 2 → 6 CO 2 + 6 H 2 O .
Применение углеводов. Нахождение в природе
Моносахариды и дисахариды встречаются в различных растениях. Так, глюкоза содержится в соке фруктов и ягод, особенно винограда. Отсюда пошло второе название моносахарида — «виноградный сахар».
Фруктоза чаще всего встречается во фруктах, поэтому получила название «фруктовый сахар». Она слаще сахарозы и глюкозы, поэтому иногда применяется как сахарозаменитель.
Аналогично получил своё название «молочный сахар», так как в молочных продуктах содержится лактоза.
Мальтоза («солодовый сахар») образуется при гидролизе крахмала, содержится в проросших зёрнах зерновых растений.
Моносахариды и дисахариды выполняют энергетическую функцию.
Крахмал, гликоген, хитин, целлюлоза являются полисахаридами глюкозы. Они выполняют строительную, запасающую и энергетическую функции.
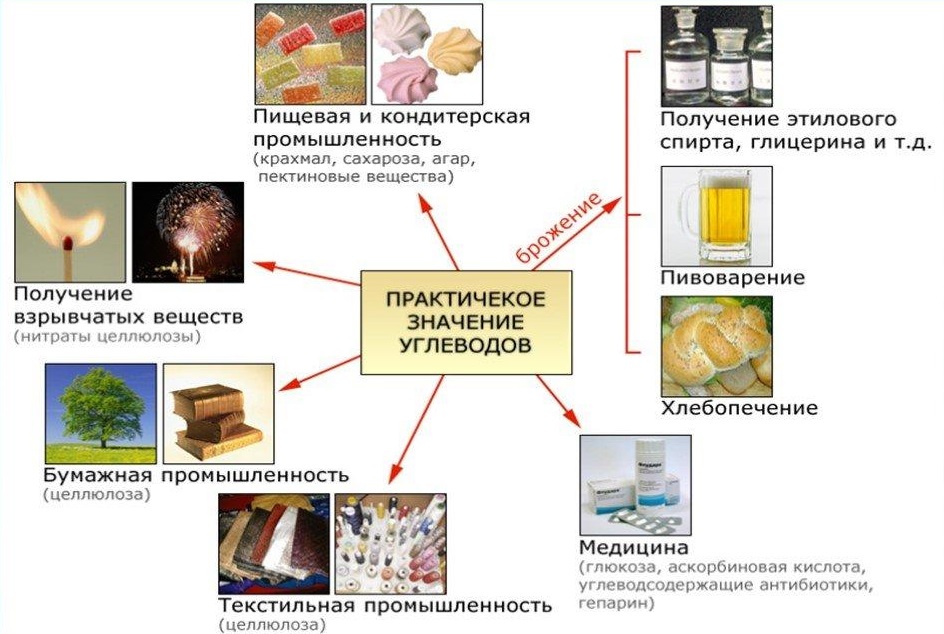
Углеводы очень широко применяются человеком. В первую очередь, это пищевая промышленность, производство алкоголя, лекарственных препаратов и т. д. (рис. 6).
Рисунок 6. Применение некоторых карбоновых кислот
Упражнение 1
Вам выдали три пробирки с неподписанными веществами: глюкоза, этаналь, глицерин. Имея в распоряжении свежеприготовленный гидроксид меди (II), составьте алгоритм определения веществ. Составьте уравнения химических реакций на альдегидную группу.
Упражнение 2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: крахмал → глюкоза → глюконовая кислота → глюконат кальция.
Формулы веществ записывайте структурно.
Контрольные вопросы
1. Какие углеводы вы знаете? В чём особенности их строения?
2. Какие химические свойства характерны для глюкозы? Почему это вещество относится к веществам с двойственными функциями?
3. Как глюкоза образуется в природе?
4. Где содержатся фруктоза, мальтоза и целлюлоза в природе? Укажите их значение.
5. Укажите области применения углеводов.
Упражнение 1
1. Ко всем веществам в трёх пробирках добавляем гидроксид меди (II).
Если образуется раствор ярко-синего (василькового) цвета, следовательно, это глицерин или глюкоза.
Там, где при нагревании появляется осадок кирпично-красного цвета, находилась глюкоза.
Значит, во второй пробирке глицерин.
2. Нагреваем третью пробирку, в которой пока не было видимых изменений. Появляется осадок. Это этаналь.
Упражнение 2
( C 6 H 10 O 5 ) n + nH 2 O → nC 6 H 12 O 6
Источник