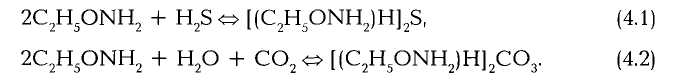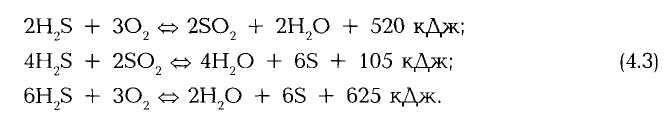Особенности очистки кислых газов
Очистка кислых газов – технологический процесс удаления сероводородных соединений и попутных компонентов: сероокиси углерода и меркаптанов. Применяются в сферах, связанных с добычей и транспортировкой попутного и природного газов.
Процесс очистки: польза и вред
Каждое из месторождений характеризуется своими параметрами сероводородных соединений. Извлеченные на поверхность земли, компоненты вредят окружающей среде. Высокая концентрация серы замедляет (или делает невозможным) выполнение следующих этапов переработки и транспортировки газа.
- ядовиты для человеческого организма;
- разъедают газоперерабатывающего оборудования и стенки трубопроводов;
- препятствуют работе катализаторов, которые используются при синтезе газа.
Согласно нормативам, в магистрали доля тиоловой серы не должна превышать 16 мг/м3, сероводорода — 7 мг/м3. Перед отправкой потребителю природное сырье очищают от серосодержащих соединений.
Широкое использование извлеченных серосодержащих добавок повышает рентабельность добычи. Кислые компоненты используют:
- при изготовлении сухого льда для заведений общественного питания;
- на предприятиях химической промышленности для получения углекислого газа, серной кислоты;
- как удобрение — при обработке земли и уходе за растениями.
Технологические приемы очистки
Очистку кислых газов производят с помощью трех методов: абсорбции, адсорбции и катализа. В состав первых двух групп входят технологии химической и физической очистки. При первом случае дополнительно используют комплексный метод.
Абсорбционная технология – наиболее востребованная. При выборе компонентов руководствуются требованиями:
- доступностью реактивов по цене и распространенности;
- высокой поглотительной способностью;
- стабильностью свойств в процессе использования, особенно — стойкостью термической и химической;
- низкими показателями: вязкости, токсичности, теплоемкости, селективности, регенерируемости, упругости паров.
Очистку катализатором специалисты разделяют на окисление и восстановление. Адсорбционный и каталитический методы используют редко: для переработки небольших объемов и тонкой очистки газов.
Особенности очистки газов
Сущность метода химической очистки основана на взаимодействии кислой среды с сорбентами. Особенность взаимодействия сероводорода с аминами — мгновенная реакция, которая сопровождается образованием сульфида амина или гидросульфида.
В качестве сорбентов чаще применяют алканоламины – вязкие прозрачные жидкости, обладающие повышенной гигроскопичностью. Когда алканоламины вступают в реакцию с низкомолекулярными спиртами (или водой), образуют нерастворимые в неполярной среде соединения.
При использовании безводной формы, сорбент предварительно растворяют в жидкости. При выборе концентрации исходят из коррозионной стойкости оборудования. Кроме алканоламина, применяют моноэтаноламин, триэтаноламин, метилдиэтаноламин, диэтаноламин, диизопропаноламин, дигликольамин.
На выбор компонентов для раствора влияет реакционная способность аминов. Если сравнивать растворы по концентрации молей амина, то использовать моноэтаноламины целесообразнее. Наиболее активные — первичные алканоламины (МЭА). Из-за низкой молекулярной массы, хемосорбенты МЭА демонстрируют наиболее удачное соотношением масс веществ, участвующих в химической реакции.
Если в газе присутствует сероокись, первичные алканоламины не применяют. Это связано со значительными потерями аминов и образованием трудноизвлекаемых побочных продуктов химической реакции. Используют диэтаноламин.
Для селективного извлечения сероводорода выгоднее применять третичные амины, например, метилдиэтаноламин.
Для физической очистки применяют технологию растворения кислых компонентов в абсорбенте. Важное значение имеет отдельно взятое давление каждого из компонентов. Чем выше парциальное давление, тем эффективнее процесс. В качестве хемосорбентов применяют
- метанол;
- пропиленкарбонат;
- N-метилпирролидон;
- полиэтиленгликоля алкиловые эфиры.
По сравнению с хемосорбентов, активные вещества для физического метода стоят дороже. Несмотря на это, итоговая стоимость очистки кислых газов получается ниже. Выгода от применения физических сорбентов — одновременное извлечение сероводорода, диоксида углерода и органических серосодержащих примесей. Нередким спутником процесса является осушение кислых газов с повышенной концентрацией влаги.
Кислые газы: выбор метода очистки
Технологии очистки газа от сероводородных соединений подразделяются в зависимости от состояния поглотителя. Есть сухие и мокрые способы. К популярным сухим реагентам относят: активированный уголь и гидрат окиси железа. Реже используют марганцевые руды. При мокрых технологиях применяют сульфат аммония и слабые щелочи.
Выбор метода определяется экономической целесообразностью добычи основного компонента. Перечень критериев включает:
- назначение, в том числе, требуемую степень чистоты газа;
- металлоемкость процесса;
- доступность энергоресурсов для конкретного месторождения;
- возможность применения безотходной технологии.
Извлечения кислых компонентов из газа относится к опасным и вредным производствам. На территории добычи складывается неблагоприятная обстановка, с повышенной концентрацией вредных соединений и пыли.
Работа насосно-компрессорных установок сопровождается высоким уровнем шума, достигающим 95-100 дБ. К сложностям процесса относят:
- постоянную вибрацию;
- статическое электричество;
- зависимость от метеоусловий;
- повышенную или пониженную температуру рабочих частей оборудования.
Факторы по обеспечению безопасности и предотвращению вреда, который может быть нанесен окружающей обстановке, снижают рентабельность бизнеса.
Источник
4.11. Очистка природного газа от сернистых соединений и углекислого газа
В составе природных газов многих месторождений содержатся сернистые компоненты и углекислый газ, так называемые кислые газы. Сернистые соединения отравляют катализаторы в процессах переработки газа, при сгорании образуют SO2 и SO3, высокое содержание которых в воздухе опасно для человека и окружающей среды. Сероводород H2S и углекислый газ СО2 в присутствии воды вызывает коррозию стальных труб, оборудования трубопроводов, компрессорных машин и т. д. Их присутствие ускоряет гидратообразование. Требования к газу, поставляемому потребителю, по содержанию сернистых компонентов постоянно возрастают. В настоящее время допускается содержание H2S в природном газе не более 5,7 мг/м 3 , общей серы не более 50 мг/м 3 , углекислого газа СО2 до 2 %. Сернистые компоненты природного газа и в первую очередь H2S служат отличным сырьем для производства серы. Из сероводорода природного газа получается наиболее чистая и дешевая сера. Степень чистоты так называемой газовой серы составляет 99,9 %. Современные процессы очистки природного газа связаны с производством серы и обеспечением чистоты воздушного бассейна.
Традиционные схемы очистки больших объемов газа включают процессы:
1) извлечения кислых компонентов, т. е. производство очищенного газа;
2) переработку кислых газов в серу;
3) очистку или сжигание отходящих газов;
Для извлечения кислых компонентов из природного газа применяют главным образом абсорбционные регенеративные процессы. Кислые компоненты из газа извлекают в процессе химической или физической абсорбции. Затем при регенерации насыщенного абсорбента получают поток кислого газа, направляемый на установку производства серы.
В процессах химической абсорбции применяют водные растворы поглотителей, которые вступают в обратимую реакцию с кислыми компонентами природного газа. В качестве химических поглотителей используют моноэтаноламин, диэтаноламин, дигликольамин, растворы солей щелочных металлов, растворы солей аминокислот и др. Схема процесса, типичного для химической абсорбции, приведена на рис. 4.23 [38].
Часто применяют моноэтанолоаминовый процесс, характеризующийся высокой реакционной способностью поглотителя, его хорошей химической устойчивостью и небольшими капитальными вложениями. Реакцию взаимодействия моноэтанолоамина с сероводородом и углекислым газом можно представить следующими уравнениями:
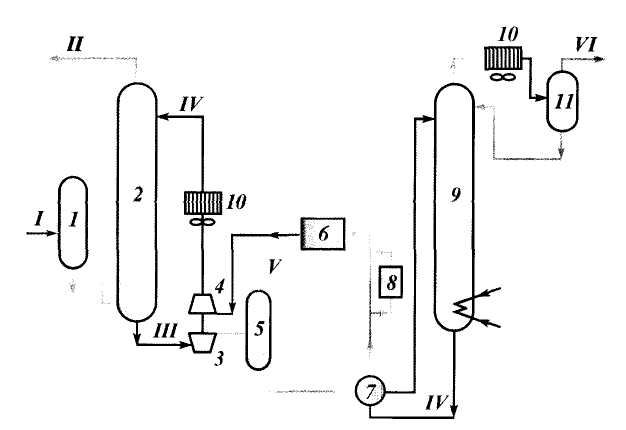
Рис. 4.23. Схема установки для очистки природного газа методом химической абсорбции:
1 — входной сепаратор; 2 — абсорбер; 3 — гидравлическая турбина; 4 — насос; 5 — выветриватель;
6 — промежуточная емкость; 7 — теплообменник; 8 — фильтр; 9 — десорбер; 10 — воздушный холодильник;
11 — сепаратор рефлюкса; / — сырой газ; II — очищенный газ; III — насыщенный абсорбент;
IV — регенерированный абсорбент; V — газ выветривания; VI — кислый газ
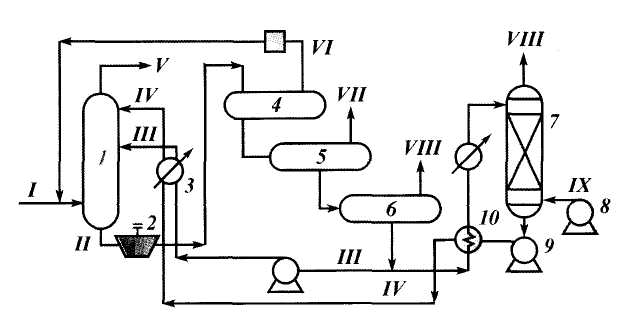
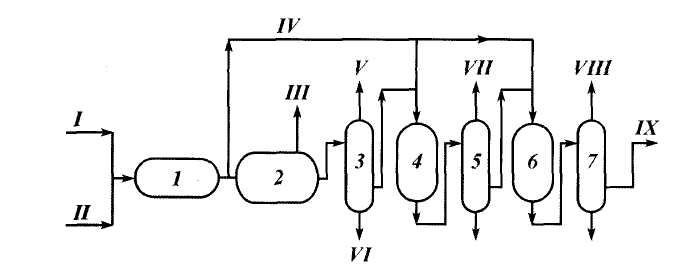
Рис. 4.24. Схема установки осушки газа методом физической абсорбции:
1 — абсорбент; 2 — детандер; 3 — холодильник; 4, 5 и 6 — первая, вторая и третья ступени выветривания соответственно; 7 — выпарная колонна; 8 — воздуходувка; 9 — насос; 10 — теплообменик; / — исходный газ; II — насыщенный абсорбент; III — груборегенерированный абсорбент; IV — тонкорегенерированный абсорбент; V — очищенный газ; VI — рецикловый газ; VII — газ выветривания среднего давления; VIII — кислый газ; IX — воздух или инертный газ
Во избежание коррозии оборудования концентрация моноэтаноламина в растворе с водой не превышает 15 — 20 %.
При физической абсорбции кислых газов из потоков природного газа используются органические растворители: метанол, пропиленкарбонат, диметиловый эфир полиэтиленгликоля и др. Процессы физической абсорбции характеризуются высокой степенью насыщения абсорбента кислыми газами и соответственно низкими скоростями циркуляции поглотителя, низкими энергозатратами, небольшими габаритами и простотой оборудования.
Схема, типичная для процесса физической абсорбции, приведена на рис. 4.24. Выбор растворителя основан на составе, температуре и давлении исходного газа, с учетом метода последующей его обработки и требований к качеству очищенного газа.
Вторая операция при очистке природного газа — получение серы из сернистых соединений. При обработке больших потоков природного газа чаще всего используются различные модификации процесса Клауса, основанного на каталитической реакции кислорода воздуха с сероводородом, поступающим из регенерационной колонны абсорбционных процессов, при повышенной температуре. Реакция Клауса протекает в две стадии по уравнениям
Рис. 4.25. Схема установки Клауса с однопоточным процессом:
1 — горелка и реакционная камера; 2 — котел-утилизатор; 3, 5,7 — конденсаторы; 4, 6 — первый и второй каталитические конверторы соответственно; / — кислый газ; II — воздух; III, VIII — пар (высокое давление); IV — обводная линия горячего газа; V, VII — пар (низкое давление); VI — сера; IX — «хвостовой газ»
Для увеличения выхода серы процесс проводится в соответствии с двумя стадиями реакции. Сначала в печи Клауса при высокой температуре сжигается часть сероводорода с получением оксида серы. В результате очень высокой температуры и некаталитического сжигания сероводорода с воздухом получается непосредственно сера с выходом около 60 %. После высокотемпературного сжигания и утилизации теплоты продуктов сгорания устанавливаются один или несколько каталитических конвертеров Клауса (рис. 4.25), где оставшийся сероводород взаимодействует с кислородом. Снижение температуры каталитической реакции способствует повышению выхода серы. При очистке отходящих с установок Клауса газов возможны два варианта. В одном случае газы, отходящие с установок Клауса, подаются непосредственно в установку доочистки, в другом — они предварительно сжигаются до превращения всех сернистых соединений в SO2 и только после этого поступают на установку доочистки.
Источник