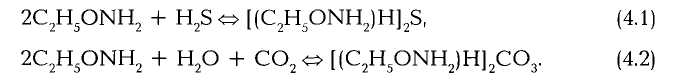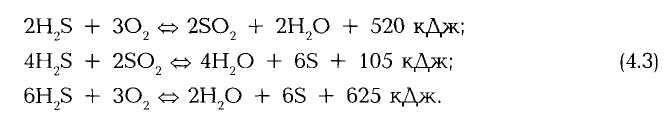11). Методы очистки от кислых компонентов.
очистки газов основаны на селект извлечении кислых компонентов тв поглот-ми – адсорбентами. Когда извлекаемый компонент удерживается адсорбентом только физ силами, имеет место физическая адсорбция. Если извлекаемый компонент вступает с адсорбентом в хим взаимодействие говорят о химической адсорбции.
Каталитические методы когда в газе присутствуют соединения, недостаточно полно удаляемые с помощью ж или тв поглотителей, например сероуглерод, серооксид углерода, сульфиды, дисульфиды, тиофен, а также в тех случаях, когда требуется тонкая очистка газа.
- Окислительные методы заключаются в проведении реакций кат окисления сероводорода до элементарной серы или кат окисления меркаптанов до дисульфидов.
- Восстановительные методы заключаются в восстановлении сернистых соединений при взаим их с водородом (гидрирование) или с водяным паром (гидролиз), а также в гидрировании диоксида углерода до метана. При восстановлении сернистых соединений все они превращаются в сероводород.
новые методы: микробиологические, мембранные, фотохимического разложения. Выбор процесса очистки природного газа от кислых компонентов зависит от: состава и параметров сырьевого газа, требуемой степени очистки, области использования товарного газа.
12). Очистка газов от диоксида углерода.
Методы очистки газов от диоксида углерода можно разделить на следующие группы:
- физическая абсорбция, основанная на хорошей растворимости диоксида углерода в полярных растворителях (вода, метанол);
- хемосорбция, основанная на химическом связывании диоксида углерода при взаимодействии его с соединениями щелочного характера (щелочь, этаноламины, растворы карбонатов);
- адсорбция, основанная на адсорбции диоксида углерода различными адсорбентами (например, цеолитами);
- каталитическое гидрирование.
13). Очистка газов от с помощью физических абсорбентов.
1) Абсорбция водой — распространенный метод улавливания диоксида углерода из газов.
+ доступность и дешевизна абсорбента,
— поглот спость водой СО2 (8 кг CO2 на 100 кг абсорбента) и селективность. Наряду с СО2 в воде растворяются водород, СО, азот.
Схема проста. Газ промывают холодной водой в башнях с насадкой (скрубберах) под 1,5—2,5МПа,тк растворимость СО2 в воде с р. При этом из газа удаляется частично и сероводород, растворимость которого также . Затем р и из воды выделяется (десорбируется) газ, содержащий до85%СО2 (остальное — водород, азот, сероводород), кот используют для получения сухого льда,карбамида,соды и др
2) Абс-я метанолом(«ректизол»процесс) + эф-н; при -60°С, резко поглотительная спос-ть метанола. Так, при —60°С и давлении около 0,4 МПа
Избирательность метанола по отношению к диоксиду углерода значительно, чем воды. СО2 из р-ра выделяют р и Т. Кроме метанола можно использовать и другие органические растворители: N-метилпирролидон, сульфолан, пропиленкарбонат.
широкого распространения они пока не получили.
От СО2 и Н2S применяют МЭГ ДЭГ ТЭГ
Источник
4.11. Очистка природного газа от сернистых соединений и углекислого газа
В составе природных газов многих месторождений содержатся сернистые компоненты и углекислый газ, так называемые кислые газы. Сернистые соединения отравляют катализаторы в процессах переработки газа, при сгорании образуют SO2 и SO3, высокое содержание которых в воздухе опасно для человека и окружающей среды. Сероводород H2S и углекислый газ СО2 в присутствии воды вызывает коррозию стальных труб, оборудования трубопроводов, компрессорных машин и т. д. Их присутствие ускоряет гидратообразование. Требования к газу, поставляемому потребителю, по содержанию сернистых компонентов постоянно возрастают. В настоящее время допускается содержание H2S в природном газе не более 5,7 мг/м 3 , общей серы не более 50 мг/м 3 , углекислого газа СО2 до 2 %. Сернистые компоненты природного газа и в первую очередь H2S служат отличным сырьем для производства серы. Из сероводорода природного газа получается наиболее чистая и дешевая сера. Степень чистоты так называемой газовой серы составляет 99,9 %. Современные процессы очистки природного газа связаны с производством серы и обеспечением чистоты воздушного бассейна.
Традиционные схемы очистки больших объемов газа включают процессы:
1) извлечения кислых компонентов, т. е. производство очищенного газа;
2) переработку кислых газов в серу;
3) очистку или сжигание отходящих газов;
Для извлечения кислых компонентов из природного газа применяют главным образом абсорбционные регенеративные процессы. Кислые компоненты из газа извлекают в процессе химической или физической абсорбции. Затем при регенерации насыщенного абсорбента получают поток кислого газа, направляемый на установку производства серы.
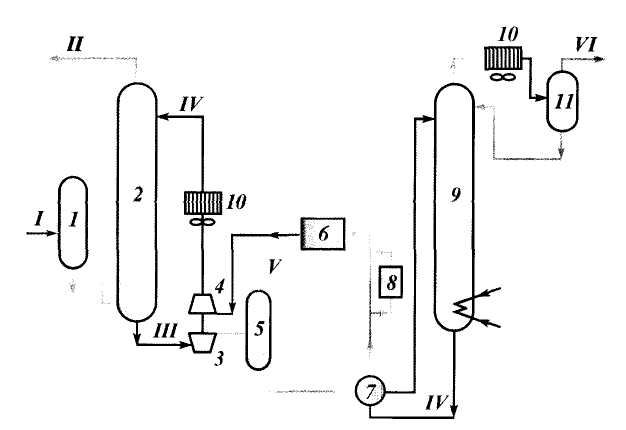
В процессах химической абсорбции применяют водные растворы поглотителей, которые вступают в обратимую реакцию с кислыми компонентами природного газа. В качестве химических поглотителей используют моноэтаноламин, диэтаноламин, дигликольамин, растворы солей щелочных металлов, растворы солей аминокислот и др. Схема процесса, типичного для химической абсорбции, приведена на рис. 4.23 [38].
Часто применяют моноэтанолоаминовый процесс, характеризующийся высокой реакционной способностью поглотителя, его хорошей химической устойчивостью и небольшими капитальными вложениями. Реакцию взаимодействия моноэтанолоамина с сероводородом и углекислым газом можно представить следующими уравнениями:
Рис. 4.23. Схема установки для очистки природного газа методом химической абсорбции:
1 — входной сепаратор; 2 — абсорбер; 3 — гидравлическая турбина; 4 — насос; 5 — выветриватель;
6 — промежуточная емкость; 7 — теплообменник; 8 — фильтр; 9 — десорбер; 10 — воздушный холодильник;
11 — сепаратор рефлюкса; / — сырой газ; II — очищенный газ; III — насыщенный абсорбент;
IV — регенерированный абсорбент; V — газ выветривания; VI — кислый газ
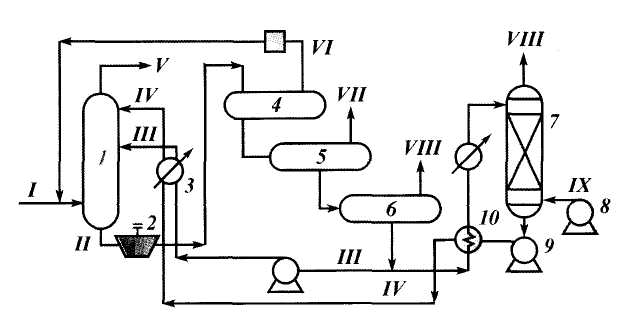
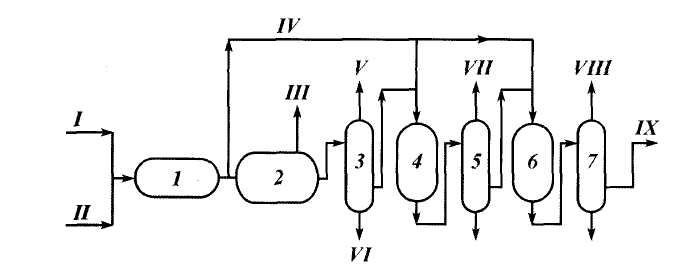
Рис. 4.24. Схема установки осушки газа методом физической абсорбции:
1 — абсорбент; 2 — детандер; 3 — холодильник; 4, 5 и 6 — первая, вторая и третья ступени выветривания соответственно; 7 — выпарная колонна; 8 — воздуходувка; 9 — насос; 10 — теплообменик; / — исходный газ; II — насыщенный абсорбент; III — груборегенерированный абсорбент; IV — тонкорегенерированный абсорбент; V — очищенный газ; VI — рецикловый газ; VII — газ выветривания среднего давления; VIII — кислый газ; IX — воздух или инертный газ
Во избежание коррозии оборудования концентрация моноэтаноламина в растворе с водой не превышает 15 — 20 %.
При физической абсорбции кислых газов из потоков природного газа используются органические растворители: метанол, пропиленкарбонат, диметиловый эфир полиэтиленгликоля и др. Процессы физической абсорбции характеризуются высокой степенью насыщения абсорбента кислыми газами и соответственно низкими скоростями циркуляции поглотителя, низкими энергозатратами, небольшими габаритами и простотой оборудования.
Схема, типичная для процесса физической абсорбции, приведена на рис. 4.24. Выбор растворителя основан на составе, температуре и давлении исходного газа, с учетом метода последующей его обработки и требований к качеству очищенного газа.
Вторая операция при очистке природного газа — получение серы из сернистых соединений. При обработке больших потоков природного газа чаще всего используются различные модификации процесса Клауса, основанного на каталитической реакции кислорода воздуха с сероводородом, поступающим из регенерационной колонны абсорбционных процессов, при повышенной температуре. Реакция Клауса протекает в две стадии по уравнениям
Рис. 4.25. Схема установки Клауса с однопоточным процессом:
1 — горелка и реакционная камера; 2 — котел-утилизатор; 3, 5,7 — конденсаторы; 4, 6 — первый и второй каталитические конверторы соответственно; / — кислый газ; II — воздух; III, VIII — пар (высокое давление); IV — обводная линия горячего газа; V, VII — пар (низкое давление); VI — сера; IX — «хвостовой газ»
Для увеличения выхода серы процесс проводится в соответствии с двумя стадиями реакции. Сначала в печи Клауса при высокой температуре сжигается часть сероводорода с получением оксида серы. В результате очень высокой температуры и некаталитического сжигания сероводорода с воздухом получается непосредственно сера с выходом около 60 %. После высокотемпературного сжигания и утилизации теплоты продуктов сгорания устанавливаются один или несколько каталитических конвертеров Клауса (рис. 4.25), где оставшийся сероводород взаимодействует с кислородом. Снижение температуры каталитической реакции способствует повышению выхода серы. При очистке отходящих с установок Клауса газов возможны два варианта. В одном случае газы, отходящие с установок Клауса, подаются непосредственно в установку доочистки, в другом — они предварительно сжигаются до превращения всех сернистых соединений в SO2 и только после этого поступают на установку доочистки.
Источник