Физико-химические свойства природных газов. Пересчет состава газа и конденсата , страница 2
В газовой промышленности за стандарт приняты условия Т=293,15 0 К и Р=0,1013 МПа, в этом случае 1 гмоль и 1 кгмоль будут занимать объемы соответственно 24,04 дм 3 /моль и 24,04 м 3 /кмоль.
Для природного газа, являющегося смесью углеводородных и неуглеводородных компонентов, вводится понятие кажущаяся молярная масса Мк, значение которой определяется по формуле
где Мi – молярная масса i-го компонента, кг/кмоль; ni — молярная масса i-го компонента в смеси; к – число компонентов в смеси.
Если ni дано в мольных процентах, формула имеет вид:
Иногда используют единицы измерения г/моль. Часто слово “кажущаяся” опускается и для природного газа это значение называют молярная (а иногда молекулярная) масса газа.
Плотность вещества – масса единицы объема. Плотность газа определяется, как отношение молярной массы к объему моля газа, т.е.
При стандартных условиях – ρст
где ρ0 и ρст – плотность газа при соответствующих условиях.
2.2. Пересчет состава газа и конденсата.
Пересчет состава газа и конденсата осуществляется следующим образом.
Дан состав газа (конденсата) в мольных долях – ∑Мi=1, где ni – мольная масса i-го компонента в смеси, к – число компонентов в смеси. При известной молярной массе Мi – каждого компонента определить состав в массовых долях, т.е. найти mi и ∑mi=1, mi – массовая доля i-го компонента. Решение приводится в таблице 2.2.
Таблица 2.2 – Пересчет мольного состава смеси углеводородов в массовый.
Мольные доли, ni
Молярная масса, mi
Масса i-го компонента
Источник
Состав и основные параметры природных газов
Природные газы, добываемые из газовых и газоконденсатных месторождений, состоят из предельных углеводородов с общей формулой CnH2n+2 и неуглеводородных компонентов: азота (N2), углекислого газа (СО2), сероводорода (H2S), инертных газов (гелия, аргона, криптона, ксенона). Кроме того, природные газы насыщены парами воды, содержание которых зависит от давления, температуры, состава газа и воды. Число углеродных атомов в молекуле углеводородов п может достигать 17-40.
Метан (СН4), этан (С2Н6), этилен (С2Н4) при нормальных условиях (Рат = 0,1 МПа и Тст = 273К) являются реальными газами. Пропан (С3Н8), бутан (С4Н10) в нормальных условиях находятся в газообразном состоянии, при повышенных давлениях — в жидком состоянии, входят в состав сжиженных углеводородных газов. Углеводороды от (С5Н12) до (С17Н36) при нормальных условиях находятся в жидком состоянии. Все компоненты, входящие в состав природного газа, характеризуются строго индивидуальными свойствами.
По составу компонентов природные газы можно подразделить на три группы:
1. Газы, добываемые из чисто газовых месторождений. Это сухие
газы без тяжелых углеводородов.
2. Газы, добываемые с нефтью (попутный нефтяной газ), это физическая смесь сухого газа, сжиженного газа и газового бензина.
3. Газы, добываемые из газоконденсатных месторождений. Они со
стоят из сухого газа и жидкого углеводородного конденсата.
Наименьшей частицей, характеризующей вещество, является молекула, состоящая из атомов одного или нескольких элементов. За единицу измерения массы атомов и молекул условно принята 1/12 массы атома изотопа углерода. Масса атома элемента, выраженная в углеродных единицах, называется атомной массой элемента. Сумма атомных масс атомов, образующих молекулу, называется молекулярной массой вещества. Состав природного газа выражается в объемных или массовых долях единицы или процентах. Объемный состав примерно совпадает с молярным, так как объем 1.кмоля идеального газа при одинаковых физических условиях, по закону Авогадро, имеет одно и то же численное значение, в частности, при нормальных условиях равен 22,41 м 3 .
Объемный (молярный) состав газа можно пересчитать в массовый для каждого компонента смеси по формуле
где gi, — массовая доля i-гo компонента в газе;
Xi — объемная доля i-гo компонента;
Мi — молекулярная масса i-гo компонента.
Если состав природного газа задан в массовых долях, то для пересчета его в объемные (молярные) единицы используется формула
где mi — число молей i-гo компонента в смеси, и mi=gi / Mi.
Одним из основных параметров, характеризующим природный газ, является плотность. Плотность газа — масса единицы объема — равна отношению молекулярной массы газа к объему 1 моля. Плотность определяется по формуле
Размерность плотности в системе СИ — кг/м 3 , в системе СГС — г/см 3 .
Плотность газа известного состава определяется как сумма произведений плотности отдельных компонентов на их объемное (молярное) содержание Xi:
или по известным молекулярным массам:
Для практических расчетов часто используется относительная плотность газа по воздуху , равная отношению плотности газа к плотности воздуха , взятой при том же давлении и температуре:
т.к. при нормальных условиях равна 1.293 кг/м 3 . Относительная плотность удобна тем, что не зависит от температуры, давления.
Плотность природных газов при различных давлениях и температурах определяют по формуле
где z — коэффициент сверхсжимаемости природного газа.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник
Смеси газов
Природные газы представляют собой смесь, состоящую из нескольких чистых веществ, химически не взаимодействующих между собой: метана СН







Массовой концентрацией 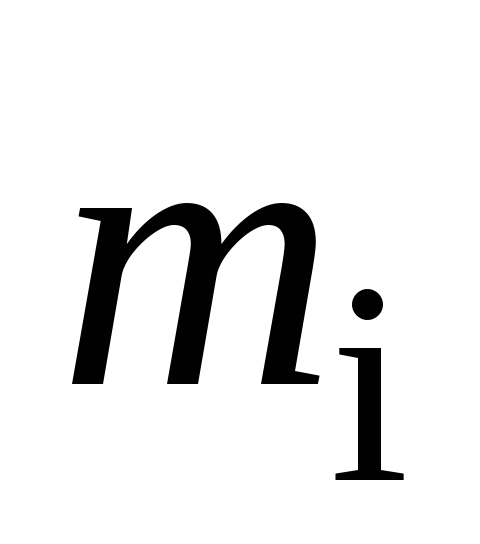


Физические характеристики компонентов природного газа
Плотность, кг/м
Плотность по отношению к воздуху
СН
С
С
С
С
С
С
С
С
С
С
С
Источник