Основные виды химической связи в веществах
В конце XVIII века Уильям Хиггинс опубликовал научную работу, в которой описал предположение о существовании неких связей между частицами всех веществ. Эта теория стала предвестником теории о валентности, которая на тот момент воспринималась как «соединительная сила» веществ. Такие представления существовали в мире химии до открытия электрона. С момента возникновения теории о химических связях понятие валентности было вытеснено из научного толкования, а сам термин стал претерпевать значительные изменения. Теория химических связей смогла более точно объяснить связь частиц тех веществ, с которыми сталкивался человек. Определение химической связи звучит следующим образом: Определение
Химическая связь — это взаимодействие атомов, осуществляемое путем обмена электронами или их перехода от одного атома к другому.
Процесс образования химических связей не может происходить бесследно для вещества. Он всегда сопровождается выделением энергии химической связи.
Большую роль в процессе формирования химической связи играют валентные электроны, находящиеся на внешнем энергетическом уровне (электронном слое) атома. Они вступают во взаимодействие с другими атомами, образуя новые химические соединения.
Способность притягивать электроны — электроотрицательность — играет важную роль при образовании химической связи и определяет ее вид. По правилу октета завершенным считается внешний энергетический уровень, содержащий 8 электронов у большинства веществ и 2 электрона у гелия.
Современная химия различает несколько видов связей:
- металлическая;
- ковалентная;
- ионная;
- водородная;
- ван-дер-ваальсова.
Основные теории и представления
До открытия электрона представления о химической связи заключались в теории валентности — способности атомов образовывать химические связи в определенном количестве, ограниченном числом неспаренных электронов.
Точное и полное понимание теории сложилось к 1852 году, когда свой труд о соединительной силе атомов опубликовал химик Эдуард Франкленд. Он переосмыслил все знания о валентности, существовавшие до него и объединил их в одну теорию, согласно которой появилось учение о валентности.
В 1861 году в теорию внес свой вклад А. М. Бутлеров, который показал четкое различие между изолированным и входящим в состав соединение атомом. Эти знания позволили получить наглядное изображение атома в виде первых молекулярных моделей.
Дальнейшие основные теории химической связи делятся на:
К электронным теориям относятся электронная теория химической связи и Боровская модель.
Электронная теория сформировалась в 1912-16 годах американским физиком и химиком Г. Н. Льюисом. Она стала основой классической теории строения в органической части химических исследований. Согласно этой теории атомы, вступающие в связь при ковалентном соединении, имеют общую электронную плотность, которая делится между ними.
Это мнение шло в противовес господствовавшей тогда теории о положительном и отрицательном заряде атомов, которые несут разные атомы. Также концепция Льюиса включала формулирование правило октета.
Боровская модель была опубликована в 1913 году Нильсом Бором в статье «Системы, содержащие несколько ядер». Согласно модели, электроны атомов образовывают кольцо, которое вращается перпендикулярно оси молекулы. Однако эта система требовала усовершенствования и доработки, а все попытки их осуществления приводили к неудачам.
Квантовые теории химической связи включают в себя теорию валентных связей и теорию молекулярных орбиталей.
В 1927 году В. Гайтлером и Ф. Лондоном была заложена теория валентных связей, основанная на том, что каждая пара атомов в молекуле удерживается при помощи общих электронных пар.
Молекулу как целый объект рассматривает теория молекулярных орбиталей. Согласно ей молекула является сложной системой, и поэтому должна рассматриваться как целое и не разбиваться при исследованиях на более мелкие частицы, иначе они теряют свои свойства. Данная теория описывает свойства отдельных молекул и дает понимание о распределении плотности вероятности обнаружения электрона в заданном пространстве.
Виды химических связей в неорганических, органических и комплексных соединениях
Химические соединения имеют сложную структуру. Одна молекула может иметь сразу несколько видов химической связи.
Химия выделяет 4 основных вида химической связи. Это:
Ковалентная связь при взаимодействии атомов бывает двух видов: полярная и неполярная. Атомы объединяются по типу обменного механизма или по донорно-акцепторному механизму. В таком соединении важна электроотрицательность атомов.
Электроотрицательность (ЭО) — способность атома в молекуле притягивать электронные пары в свою сторону.
Ионы — частицы, имеющие заряд, но образующиеся из нейтральных частиц.
Учитель непонятно объясняет предмет?
Источник
Природа химической связи
Химическая связь -это сила, удерживающая вместе два или несколько атомов, ионов, молекул или любую комбинацию из них. По своей природе она представляет собой электростатическую силу притяжения между отрицательно заряженными электронами и положительно заряженными ядрами. Величина этой силы притяжения зависит главным образом от электронной конфигурации внешней оболочки атомов (см. гл. 1). Например, благородные газы с трудом образуют химические связи, потому что они имеют устойчивую внешнюю электронную оболочку. В отличие от этого элементы, атомы которых имеют во внешней оболочке только один электрон, легко образуют связи. Примером таких элементов является водород.
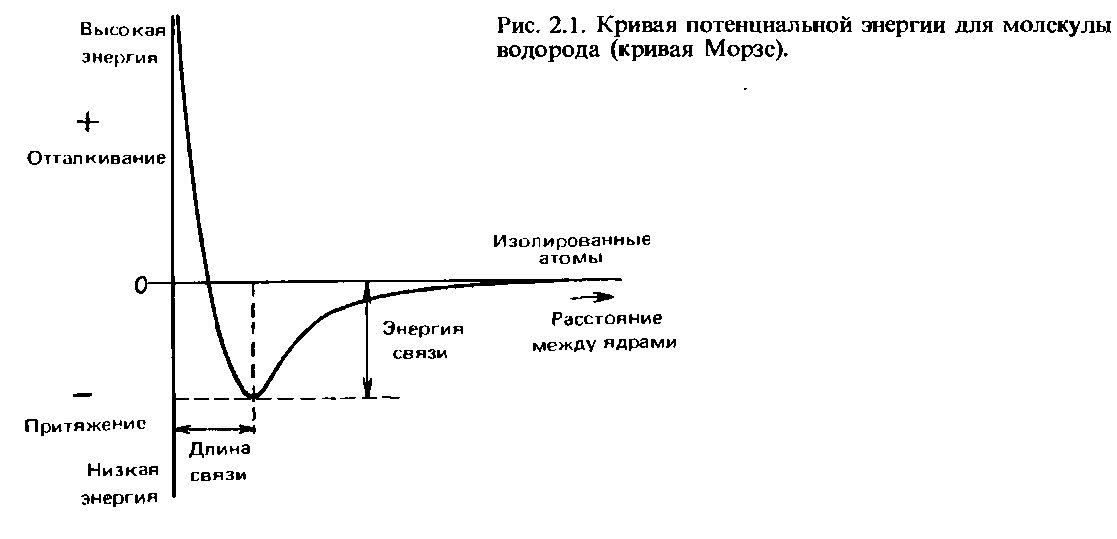
Когда два атома водорода сближаются на малое расстояние, они притягиваются друг к другу. Однако, если они сближаются слишком сильно, между ними возникает отталкивание. Оптимальным оказывается такое расстояние, при котором силы притяжения и отталкивания уравновешиваются. Ha таком расстоянии потенциальная энергия двух взаимодействующих атомов минимальна. Это расстояние называется длиной связи. Мы еще вернемся к ее более подробному обсуждению в данной главе. Ha рис. 2.1 показана зависимость потенциальной энергии от расстояния между ядрами. Кривая такого типа называется кривой Морзе. Энергия, необходимая для того, чтобы разделить два связанных между собой атома и удалить их друг от друга на расстояние, на котором они уже не испытывают силы притяжения друг к другу, называется энергия связи, или энергия диссоциации связи. Ее экспериментальное определение осуществляется путем измерения энтальпии связи (с этим понятием мы познакомимся в гл. 5).
Способность атома образовывать химические связи называется его валентностью. Впрочем, это понятие считается сильно устаревшим, поскольку в настоящее время гораздо чаще принято рассматривать химическую связь не вообще, а с учетом ее конкретного типа. Электроны, пршшмающие участие в образовании химических связей, называются валентными электронами. Эти электроны находятся на самых высоких по энергии орбиталях атома (см. гл. 1). Внешняя оболочка атома, которая содержит эти орбитали, называется валентной оболочкой.
Электронная теория валентности. Современные представления о природе химической связи основаны на электронной теории валентности. Эту теорию разработали независимо Г. Н. Льюис и В. Коссель в 1916 г. Согласно электронной теории валентности, атомы, образуя связи, приближаются к достижению наиболее устойчивой (т.е. имеющей наиболее низкую энергию) электронной конфигурации. Атомы могут достичь этого двумя способами:
1. Они могут терять либо приобретать электроны, образуя ионы. Если атомы приобретают электроны, они превращаются в анионы. Если они теряют электроны, то превращаются в катионы. Анионы и катионы с заполненной внешней электронной оболочкой имеют устойчивую электронную конфигурацию. Между анионом и катионом возникает химическая связь, представляющая собой электростатическую силу притяжения. Химическая связь такого типа ранее называлась электровалентной связью; современное название ионная связь.
2. Атомы могут также приобретать устойчивые внешние электронные конфигурации путем обобществления электронов. Возникающая при этом химическая связь называется ковалентной связью. Ковалентная связь образуется в результате обобществления пары электронов, поставляемых по одному от каждого атома. Однако в некоторых молекулах или многоатомных ионах оба таких электрона могут поставляться только одним атомом. Такая разновидность ковалентной связи называется координационной, донорно-акцепторной или дативной ковалентной связью.
Правило октета. Когда атом какого-либо элемента образует химическую связь, приобретая, теряя либо обобществляя валентные электроны, его электронная конфигурация становится такой же, как у атома благородного газа, расположенного в конце того же периода, что и данный элемент, либо в конце предыдущего периода. Атомы всех благородных газов, за исключением гелия, имеют во внешней оболочке устойчивый октет (восьмерку) электронов. Поэтому образование химических связей путем достижения устойчивых электронных конфигураций, как в атомах благородных газов, составляет суть так называемого правила октета. Это правило применимо и к ионным, и к ковалентным связям.
Другие типы химической связи. Особый случай представляет собой химическая связь в металлах; ее нельзя отнести ни к ионному типу, ни к ковалентному. В твердом состоянии металлы состоят из положительно заряженных ионов, плотно упакованных в кристаллическую решетку и удерживаемых вместе свободными электронами, которые «плавают» вокруг ионов в «электронном море». Такой тип связи называется металлической связью.
Существуют еще два типа химической связи, которые тоже будут рассматриваться в данной главе. Это — водородная связь и вандерваальсовы силы. Связи этих двух типов значительно слабее, чем связи других типов.
Источник
2. Природа и типы химических связей
Атомы большинства химических элементов не могут существовать в изолированном состоянии. Они соединяются между собой и образуют молекулы или кристаллы (атомные, металлические, ионные).
Химическая связь — это электростатическое взаимодействие атомов, в результате которого они объединяются в более сложные комплексы (ионы, радикалы, молекулы, кристаллы).
Образование химической связи происходит самопроизвольно, и при этом всегда наблюдается выделение энергии. Это значит, что полная энергия образовавшейся системы меньше, чем общая энергия отдельных атомов. Стремление системы к минимуму энергии является главной причиной возникновения химической связи между атомами.
В образовании химической связи, как правило, участвуют электроны, расположенные на наружном энергетическом уровне и слабо связанные с ядром.
Благородные газы не образуют химических связей. Они существуют в виде изолированных атомов (одноатомных молекул). Наличие химической инертности благородных газов, отличающихся от других атомов заполненным внешним энергетическим уровнем, позволило учёным прийти к выводу, что при образовании химических связей атомы стремятся к завершению своего внешнего электронного уровня.
В основе химической связи всегда лежит электростатическое взаимодействие заряженных частиц — ядер и электронов. Образование химической связи связано с перекрыванием электронных орбиталей и перераспределением электронной плотности между взаимодействующими атомами.
В зависимости от разности электроотрицательностей связанных атомов возможно возникновение трёх типов химической связи: ковалентной , ионной и металлической .
Ковалентная связь возникает между атомами неметаллов, т. е. между атомами с высокой электроотрицательностью. При взаимодействии одинаковых атомов неметаллов (\(χ\) больше \(2\), и электроотрицательности примерно равны) образуется ковалентная неполярная связь. Если взаимодействуют атомы, для которых разность \(χ\) от \(0,4\) до \(2\), то образуется ковалентная полярная связь.
Ионная связь возникает между атомами металлов и неметаллов, электроотрицательности которых различаются значительно (разность \(χ\) больше \(2\)).
Источник