Циклопарафины их химическое строение, свойства, нахождение в природе, практическое значение.
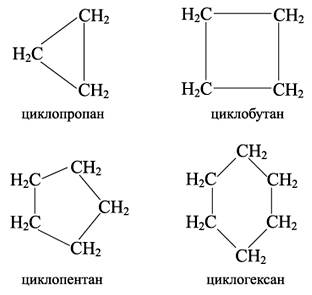
Циклоалканы (циклопарафины)- это предельные циклические углеводороды. Простейшие представители этого ряда:
Общая формула гомологического ряда циклоалканов СnH2n.
Каждый углеродный атом в циклоалканах находится в состоянии sp³-гибридизации и образует четыре σ-связи С-С и С-Н.
―Для циклоалканов характерна изомерия углеродного скелета (структурная изомерия). Структурная изомерия для циклоалканов обусловлена размером цикла.
Так, существует два циклоалкана формулы С4Н8: циклобутан и метилциклопропан.
При обычных условиях циклопропан и циклобутан газы, циклопентан и циклогексан жидкости, начиная с циклогептодекана твердые вещества. Температуры кипения и плавления циклоалканов выше, чем у соответствующих алканов.
Основной способ получения циклоалканов – отщепление двух атомов галогена от дигалогеналканов:
1,4 — дибромбутан циклобутан
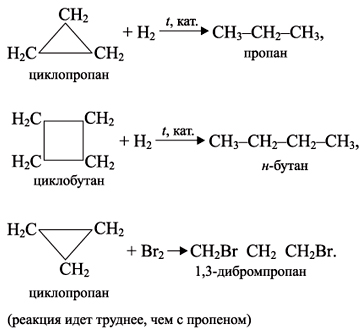
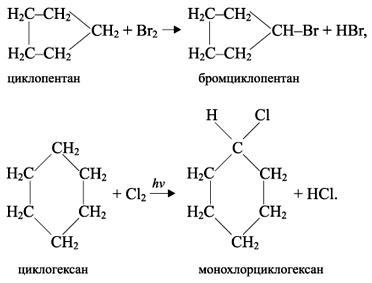
1. Присоединение галогенов.
Циклопропан 1,3 дибромпропан
2. Присоединение водорода (гидрирование). Реакция идёт при повышении температуры до 50º-70ºС используется катализатор платина.
Из циклопарафинов практическое применение имеют циклогексан, метилциклогексан и некоторые другие. В процессе ароматизации нефти эти соединения превращаются в ароматические углеводороды – в бензол, толуол и другие вещества, которые широко используются для синтеза красителей, медикаментов и т.д. Циклопропан используют для наркоза.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Студопедия рекомендует:
ОСНОВНЫЕ ЭТАПЫ ПРОЦЕССА УПРАВЛЕНИЯ Содержание процесса управления Типология процесса управления Основные этапы процесса управления Содержание процесса.
Понятие, признаки и виды органов исполнительной власти Орган исполнительной власти – это вид государственного органа.
Сбор мочи на исследование по Зимницкому Цель: определение концентрационной и выделительной функций почек.
Основные возможности MS Excel Программа обработки электронных таблиц Microsoft Excel Программа обработки электронных таблиц Microsoft Excel (в дальнейшем для.
Понятие и виды субъектов трудового права и их правовой статус СУБЪЕКТЫ ТРУДОВОГО ПРАВА Субъект права — это физическое или юридическое лицо, имеющее определенные права и обязанности, т.
Источник
Циклопарафины, их строение, свойства, нахождение в природе, практическое значение
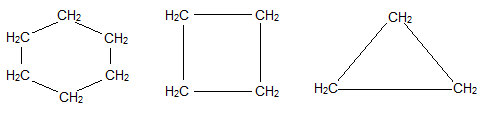
Помимо предельных углеводородов с открытой цепью существуют предельные углеводороды с замкнутой (циклической) цепью. Они имеют несколько названий: циклоалканы, циклопарафины, нафтены, цикланы, полиметилены. Циклоалканы различаются между собой размерами цикла:
По размеру цикла циклоалканы делятся на группы: малые (C3, C4) и обычные (C5 – C7) циклы.
Молекулы циклоалканов содержат на два атома Н меньше, чем соответствующие алканы (за счет их отщепления замыкается углеродное кольцо). Поэтому общая формула циклоалканов СnH2n.
Трех- и четырехчленные циклоалканы менее прочны, чем пяти- и шестичленные. Циклобутан и особенно циклопропан – соединения малоустойчивые. Это связано с тем, что в молекулах этих соединений углы между валентными связями значительно отличаются от “нормального” угла в правильном тетраэдре (109°28′). Например, в циклопропане, молекулу которого можно изобразить в виде равностороннего треугольника, угол между углерод-углеродными связями (60°) отличается от тетраэдрического угла на 49°28′ (а в расчете на одну связь на 24°44′). Такое отклонение от тетраэдрического угла создает в молекуле значительное напряжение, что существенно сказывается на ее устойчивости.
В циклогексане разница между тетраэдрическим углом и углом между углерод-углеродными связями в нем меньше и составляет 10°32′ (в расчете на одну связь она равна 5°16′). Чтобы еще уменьшить эту разницу, молекула циклогексана, как и другие молекулы циклоалканов, изгибается в пространстве. Существуют две основные формы – “ванна” и “кресло”. Наиболее устойчивой (энергетически выгодной) формой в циклогексане является форма “кресло”.
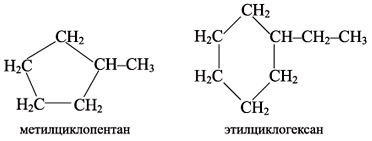
Молекулы циклоалканов часто содержат боковые углеводородные цепи:
У циклопарафинов возможна изомерия.
Структурная изомерия обусловлена размером цикла (например, циклобутан и метилциклопропан – изомеры) и положением заместителей в цикле (например, 1,1- и 1,2-диметилциклобутан).
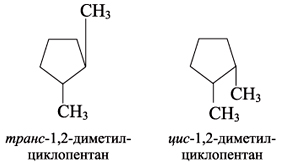
Также имеет место пространственная изомерия, связанная с различным расположением заместителей относительно плоскости цикла. При их расположении по одну сторону от плоскости цикла получаетсяцисизомер, по разные стороны – трансизомер:
Кроме того, каждому циклоалкану изомерен соответствующий алкен – это пример межклассовой изомерии.
Физические свойства. Циклопропан и циклобутан при нормальных условиях – газы, с С5 до С16 – жидкости, начиная с С17 и выше – твердые вещества. Температура кипения и плавления циклоалканов несколько выше, чем у алканов с тем же числом атомов С в молекуле. Циклопарафины в воде практически не растворяются.
Химические свойства. Циклоалканы химически малоактивны и в этом отношении напоминают алканы: они горючи, атомы Н могут замещаться галогенами.
Химические свойства циклоалканов определяются особенностями их строения.
1. Малые циклы (особенно циклопропан) неустойчивы и способны к разрыву, поэтому они склонны к реакциям присоединения:
2. Обычные циклы (С5–С7) очень устойчивы и вступают только в реакции замещения, подобно алканам:
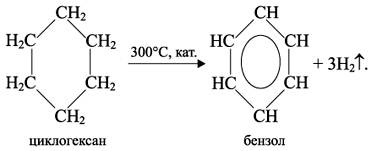
3. Циклопарафины подвергаются реакциям дегидрирования (отщепления Н):
Нахождение в природе. Циклопарафины главным образом находятся в составе некоторых нефтей. Отсюда и другое название циклопарафинов – нафтены. Пяти- и шестичленные циклопарафины были впервые выделены из нефти и изучены профессором Московского университета В.В.Марковниковым.
Практическое значение. Циклоалканы и их гомологи относятся к карбоциклическим соединениям.
Как вещества, составляющие значительную часть некоторых сортов нефти и получаемых из нее нефтепродуктов, они имеют большое практическое значение.
Циклопропан C3H6 используют в качестве анестезирующего средства в хирургии (для наркоза). Циклогексан С6Н12 – прекрасный растворитель. Циклоалканы являются компонентами моторного топлива.
Циклогексан, метилциклогексан и некоторые другие в процессе ароматизации нефти превращаются в ароматические углеводороды – бензол, толуол и другие вещества, которые широко используются для синтеза красителей, медикаментов и т.д.
Источник
Циклопарафины (циклоалканы)
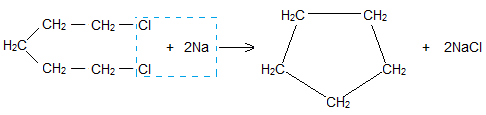
В отличии от остальных предельных углеводородов, в молекулах которых все углеродные атомы образуют открытые цепи, имеются углеводороды с замкнутыми цепями (циклами). Так, например, при действии на 1,5-дихлорпентан активным металлом цепь углеродных атомов замыкается и образуется циклический углеводород циклопентан:
Известны циклопарафины, молекулы которых состоят из трех, четырех и шести атомов углерода:
У циклопарафинов возможна изомерия. Например, молекулярной формуле C6H12 соответствует насколько веществ-изомеров; изомерия этих соединений связана с наличием боковых углеводородных цепей.
Общая формула циклопарафинов CnH2n.
Нахождение в природе
Циклопарафины главным образом находятся в составе некоторых нефтей. Отсюда и другое название циклопарафинов — нафтены. Пяти- и шестичленные циклопарафины были впервые выделены из нефти и изучены профессором Московского университета В. В. Морковниковым.
Получение
Как уже было сказано, в лаборатории циклопарафины получают из дигалогенопроизводных предельных углеводородов, действуя на них активными металлами. Циклопарафины можно выделить из нефти.
Физические свойства
Циклопропан и циклобутан при нормальных условиях — газы, а циклопентан и циклогексан — жидкости. Циклопарафины в воде практически не растворяются.
Химические свойства
У циклопарафинов, как и у предельных углеводородов, все связи насыщены, однако, в отличие от последних, они способны к реакциям присоединения. Это объясняется тем, что связи между атомами углерода в цикле могут разорваться. В результате образуются свободные связи, способные присоединять атомы водорода и других элементов. Соединения с малыми циклами легче вступают в реакции присоединения, что их аналоги с большими циклами. Так, например, реакция гидрирования (присоединение водорода) происходит при различной температуре у разных циклопарафинов. Для соединений с большими циклами характерны реакции замещения. В этом отношении они сходны с парафинами. Циклопарафины подвергаются и реакциям дегидрирования(отщепления водорода).
Применение
Из циклопарафинов практическое значение имеют циклогексан, митилциклогексан и некоторые другие. В процессе ароматизации нефти эти соединения превращаются в ароматические углеводороды — в бензол, толуол и другие вещества, которые широко используют для синтеза красителей, медикаментов и т.д. Циклопропан применяют для наркоза.
Источник