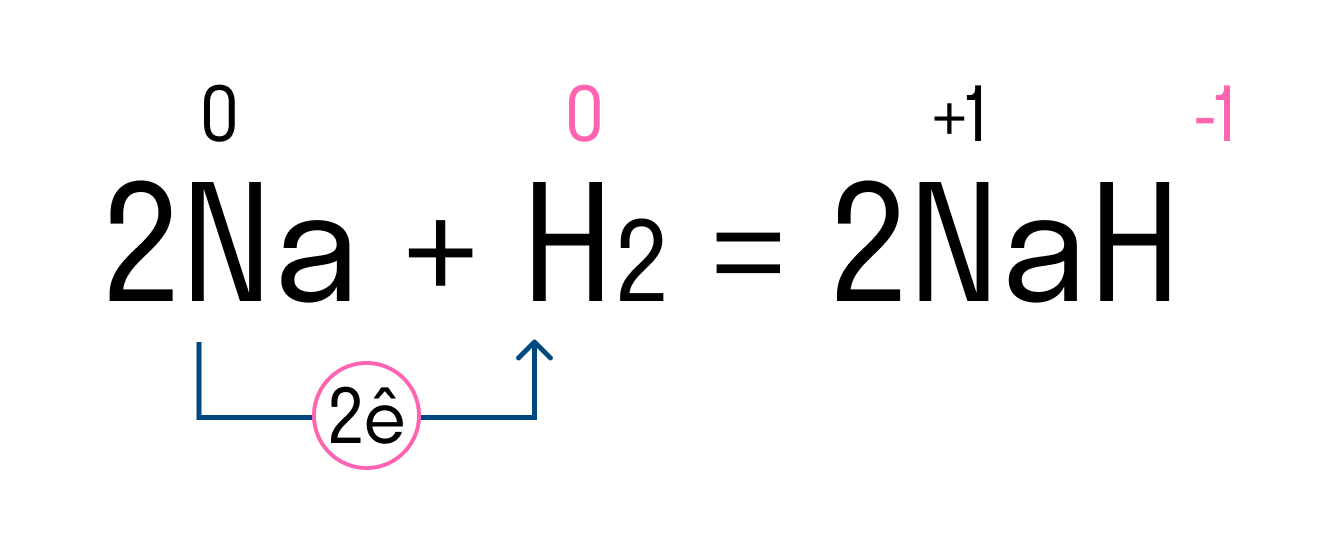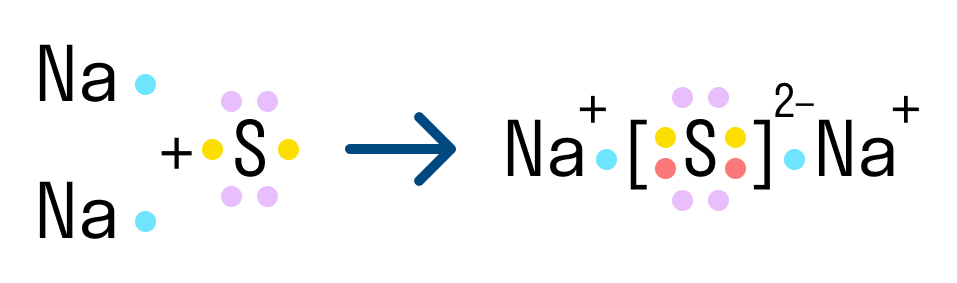- Химия. 11 класс
- Ионная связь природа связанных химических элементов.
- 2. Природа и типы химических связей
- Ионная связь
- Общие сведения о химических связях
- Определение ионной связи
- Координационное число
- Примеры веществ с ионной связью
- Характеристики ионной связи
- Физические свойства ионной связи
- Как определить ионную связь
- Вопросы для самопроверки:
Химия. 11 класс
Любое химическое соединение — молекулу (CO2), кристалл (NaCl), сложный ион () — с точки зрения электронного строения можно представить в виде системы, состоящей из атомных ядер и связывающих их электронов. Взаимодействие, которое делает эту систему устойчивой, называют химической связью.
Химическая связь — это взаимодействие, в результате которого отдельные атомы объединяются в более сложные системы (молекулы, кристаллы, ионы и др.).
Химическая связь обусловлена действием сил притяжения и отталкивания между положительно заряженными ядрами и отрицательно заряженными электронами, то есть имеет электростатическую природу.
Электроны, которые принимают участие в образовании химических связей, называют валентными. Это электроны внешних электронных оболочек атомов.
Рассмотрим, как и почему образуется химическая связь.
Основным условием образования химической связи является понижение полной энергии системы ядер и электронов по сравнению с энергией изолированных атомов.
Уменьшение полной энергии системы ядер и электронов достигается в результате совместного использования электронов разными атомами. В зависимости от того, как в результате распределена электронная плотность, различают три типа химической связи: ковалентную, ионную и металлическую.
Механизмы образования этих связей вы уже рассматривали при изучении химии в 8–10-х классах. Здесь мы дополним понятие химической связи представлениями о состоянии электронов в атоме.
Источник
Ионная связь природа связанных химических элементов.
Ионная, или электростатическая связь образуется в случае полного переноса связывающих электронов к более электроотрицательному атому, который становится в результате этого отрицательным ионом — анионом с зарядом, равным количеству перенесенных электронов.
Менее электроотрицательный атом теряет соответствующее количество электронов и становится положительным ионом — катионом. По существу, это предельный случай полярной ковалентной связи, который может реализоваться лишь при взаимодействии атомов, очень сильно отличающихся по электроотрицательности, например в LiF, CaF2, ВаО. Однако, строго говоря, даже в таких соединениях электроны не полностью переходят с катионов на
анионы, а некоторая часть электронной плотности остается делокализованной между ними. Такую связь правильнее рассматривать как преимущественно ионную с малой примесью ковалентности. Ионная связь имеет
электростатическую природу; это значит, что она не имеет определенного направления в пространстве и ионные соединения не состоят из отдельных молекул, а образуют трехмерные пространственные кристаллические структуры, в которых соотношение между количеством катионов и анионов определяется их зарядами, а взаимное расположение — соотношением радиусов. Энергия ионной связи может быть легко рассчитана по закону Кулона, если известны заряды и радиусы ионов и тип кристаллической решетки.
Источник
2. Природа и типы химических связей
Атомы большинства химических элементов не могут существовать в изолированном состоянии. Они соединяются между собой и образуют молекулы или кристаллы (атомные, металлические, ионные).
Химическая связь — это электростатическое взаимодействие атомов, в результате которого они объединяются в более сложные комплексы (ионы, радикалы, молекулы, кристаллы).
Образование химической связи происходит самопроизвольно, и при этом всегда наблюдается выделение энергии. Это значит, что полная энергия образовавшейся системы меньше, чем общая энергия отдельных атомов. Стремление системы к минимуму энергии является главной причиной возникновения химической связи между атомами.
В образовании химической связи, как правило, участвуют электроны, расположенные на наружном энергетическом уровне и слабо связанные с ядром.
Благородные газы не образуют химических связей. Они существуют в виде изолированных атомов (одноатомных молекул). Наличие химической инертности благородных газов, отличающихся от других атомов заполненным внешним энергетическим уровнем, позволило учёным прийти к выводу, что при образовании химических связей атомы стремятся к завершению своего внешнего электронного уровня.
В основе химической связи всегда лежит электростатическое взаимодействие заряженных частиц — ядер и электронов. Образование химической связи связано с перекрыванием электронных орбиталей и перераспределением электронной плотности между взаимодействующими атомами.
В зависимости от разности электроотрицательностей связанных атомов возможно возникновение трёх типов химической связи: ковалентной , ионной и металлической .
Ковалентная связь возникает между атомами неметаллов, т. е. между атомами с высокой электроотрицательностью. При взаимодействии одинаковых атомов неметаллов (\(χ\) больше \(2\), и электроотрицательности примерно равны) образуется ковалентная неполярная связь. Если взаимодействуют атомы, для которых разность \(χ\) от \(0,4\) до \(2\), то образуется ковалентная полярная связь.
Ионная связь возникает между атомами металлов и неметаллов, электроотрицательности которых различаются значительно (разность \(χ\) больше \(2\)).
Источник
Ионная связь
В этом материале речь пойдет о том, что такое ионная связь и чем она отличается от других видов, которые изучают на уроках химии в 8 классе.
· Обновлено 25 октября 2022
Общие сведения о химических связях
Давайте вспомним, как образуются химические связи. Для этого представим атом: он состоит из ядра с положительным зарядом и набора отрицательно заряженных электронов, которые располагаются на нескольких уровнях. Внешний уровень называется валентным, на нем располагаются валентные электроны. Они могут образовывать пары или быть свободными, т. е. неспаренными.
Во взаимодействии двух атомов участвуют свободные электроны внешней оболочки. Сколько таких электронов имеется у атома — столько химических связей он может образовать.
При этом каждый атом стремится приобрести устойчивую конфигурацию — двух- или восьмиэлектронную внешнюю оболочку, подобную той, что есть у инертного газа. Атом может достичь ее, отдавая или принимая часть электронов, а также образуя общую электронную пару с другим атомом. Если в результате получается два разноименно заряженных иона, говорят об ионном типе связи. Он характерен для взаимодействия атомов металла и неметалла.
Занятия где и когда удобно, 10+ кружков на выбор, никакого стресса с домашками и нудных родительских собраний
Определение ионной связи
Рассмотрим этот тип связи на примере реакции натрия и водорода, в результате которой получается гидрид натрия. У атома натрия Na есть один свободный электрон на внешнем уровне, в то время как атому водорода H не хватает одного электрона, чтобы завершить внешнюю оболочку и принять стабильную форму. Поскольку натрий имеет более низкую электроотрицательность, чем водород, он отдает свой валентный электрон и получает отрицательный заряд. Водород принимает этот электрон и получает положительный заряд. В итоге образуется два иона — катион Na + и анион H — .
Между положительным ионом Na + и отрицательным H — возникает электростатическое притяжение, которое и удерживает их вместе. Так образуется ионная связь в гидриде натрия.
Ионная связь — это тип химической связи, характерный для разноименно заряженных ионов, которые образовались в результате отдачи и присоединения электронов атомами. В нее вступают элементы с большой разностью электроотрицательности. Обычно так взаимодействуют атомы металла и неметалла.
Чаще всего именно так связаны в соединениях щелочные и щелочноземельные металлы с галогенами. Поскольку у щелочных металлов электроотрицательность ниже, их атомы становятся катионами, а атомы галогенов — анионами.
Механизм образования ионной связи похож на донорно-акцепторный механизм ковалентной связи. Первую даже называют крайним выражением второй.
Соли аммония NH4NO3, NH4Cl, (NH4)2SO4 хоть и не являются соединениями металла и неметалла, но также образованы с помощью ионной связи.
Координационное число
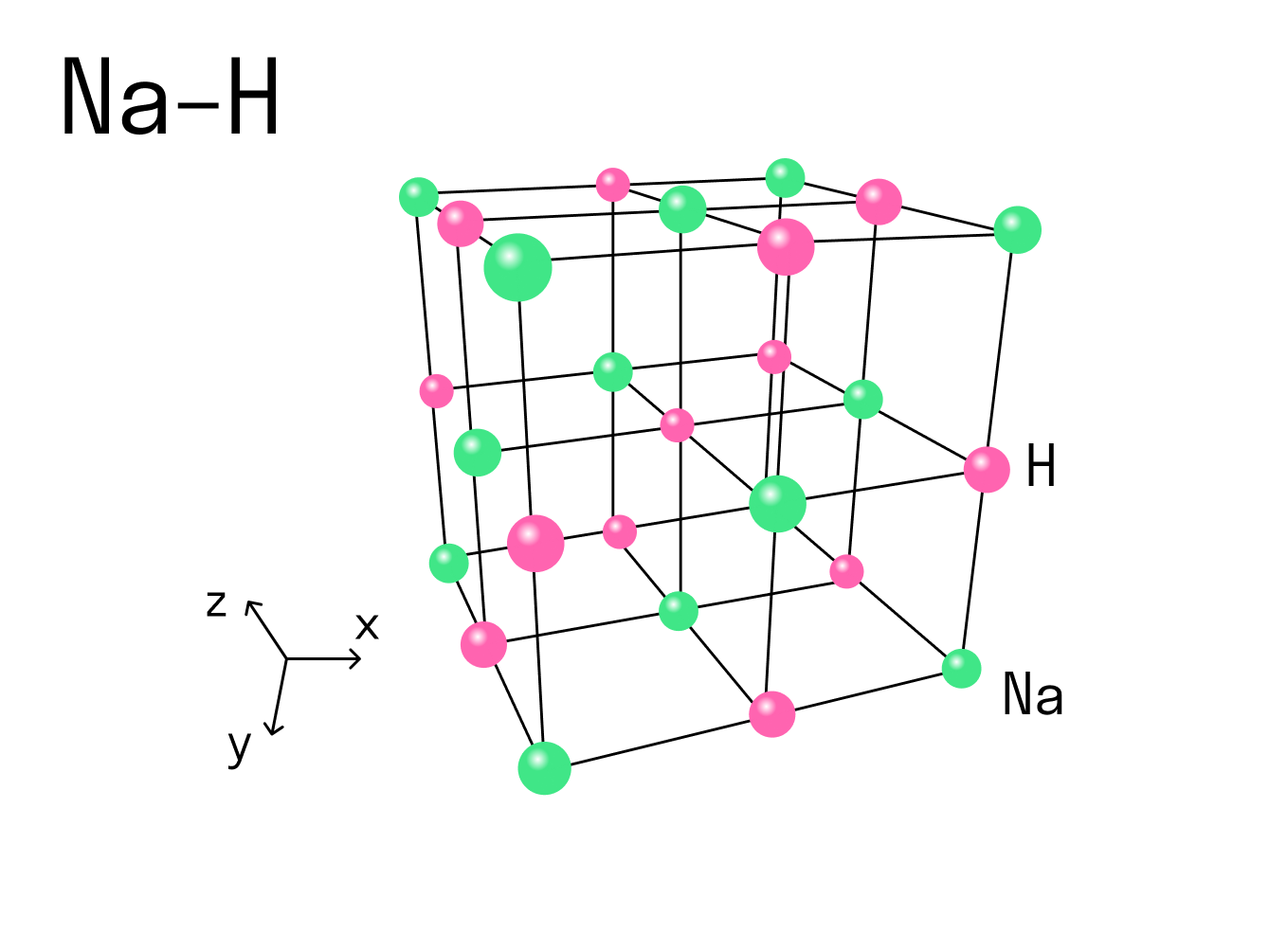
Вернемся к нашему примеру с гидридом натрия и посмотрим на кристаллическую решетку, которую имеет это ионное соединение. Каждый ион Na + контактирует с шестью ионами H — . Это максимально возможное для данного иона число химических связей, оно называется координационным.
Координационное число — это количество ближайших соседей иона в ионной кристаллической решетке. По сути это количество связей, которые образует каждый ион в составе сложного вещества.
При рассмотрении ковалентной химической связи говорят о валентности — она характеризует, сколько связей есть у конкретного атома с другими атомами. Но к ионным соединениям это понятие не применяют, потому что все ионы в кристаллической решетке взаимодействуют друг с другом. Вместо этого есть координационное число, и оно отражает количество таких взаимодействий.
Примеры веществ с ионной связью
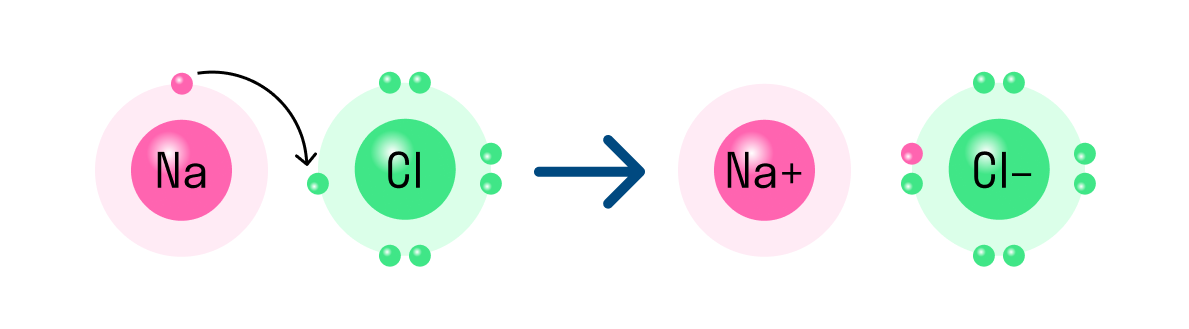
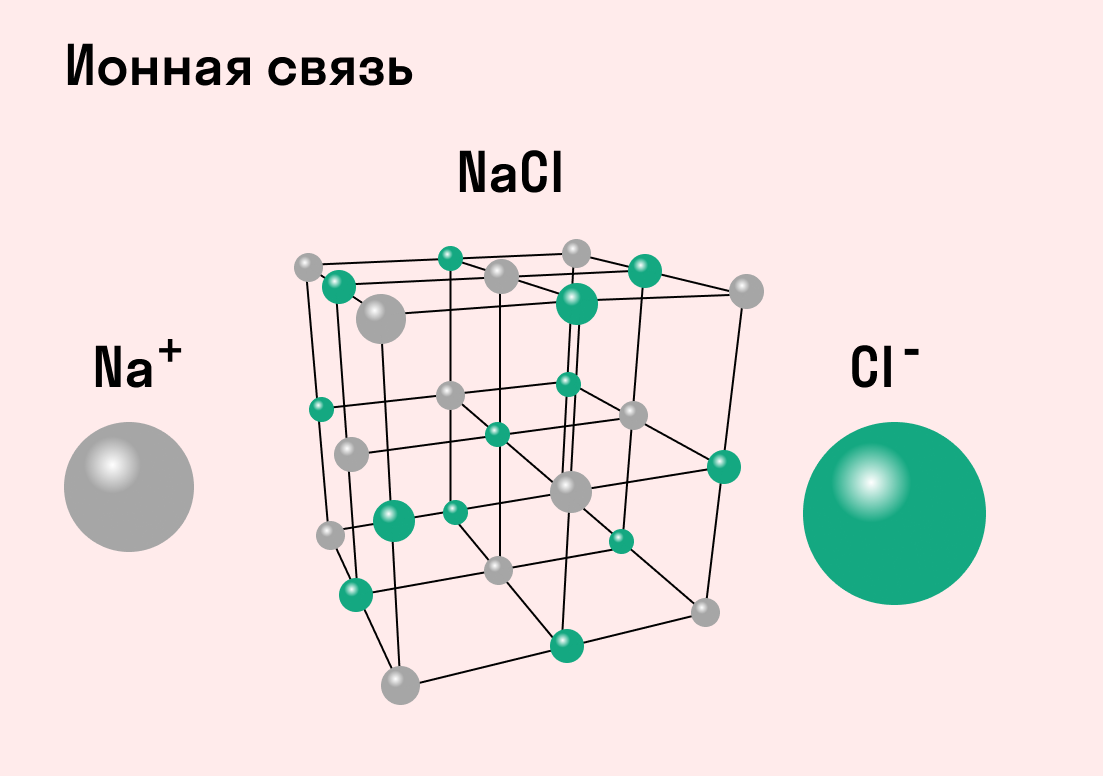
Таким же образом, как в гидриде натрия, ионы образуются и в других подобных ему соединениях. Например, в хлориде натрия NaCl атом натрия имеет один свободный электрон и отдает его атому хлора. В итоге оба завершают свой внешний уровень. Образуется ион натрия с положительным зарядом и отрицательно заряженный ион хлора.
Другой пример ионной химической связи — сульфид натрия Na2S. В данном случае у нас также есть натрий с одним свободным электроном и сера, у которой на внешнем уровне есть 2 свободных электрона из 6. Таким образом, чтобы завершить уровень и обрести стабильную форму, сере нужно 2 электрона. Поэтому в формуле сульфида серы присутствует два атома натрия.
Характеристики ионной связи
Мы узнали, как образуется ионная связь, а теперь поговорим о ее характеристиках. Она существенно отличается от других типов связи между атомами.
Разберемся в каждом пункте и начнем с направленности. Ковалентная полярная связь направлена, потому что она подразумевает смещение общей электронной пары к тому атому, который имеет большую электроотрицательность. В случае с ионами все иначе. Согласно закону Кулона притяжение между отрицательным и положительным ионом идет по прямой, соединяющей эти заряженные частицы. В кристаллической решетке все разноименно заряженные ионы взаимодействуют друг с другом и притяжение распределяется равномерно, поэтому говорят, что ионная связь не направлена.
А как насчет насыщаемости? Эта характеристика указывает на то, что атом может вступить в ограниченное количество химических связей, поскольку имеет ограниченное число неспаренных электронов. Но ионная связь — это не процесс соединения свободных электронов в пары, а взаимное притяжение ионов. Каждый ион может притягивать к себе неограниченное число ближайших соседей, поэтому нет смысла говорить о насыщаемости.
Из вышесказанного понятно, что ионная связь не имеет и кратности. Эта характеристика означает число общих электронных пар у атома, но в данном случае мы рассматриваем притяжение между ионами.
Физические свойства ионной связи
Между ионами в молекуле всегда образуется достаточно сильное притяжение, поэтому вещества с ионной связью в обычных условиях твердые и нелетучие. Такие соединения сложно разрушить при помощи тепловой энергии, что обуславливает высокую температуру кипения и плавления. При этом ионы имеют небольшой радиус взаимодействия — это придает веществам хрупкость.
Свойства ионных соединений:
- твердость,
- хрупкость,
- нелетучесть,
- тугоплавкость,
- растворимость в воде,
- электропроводность.
Типичным веществом с ионными связями можно считать хлорид натрия NaCl или поваренную соль. Ее кристаллы в точности соответствуют всем характеристикам.
Как определить ионную связь
Чтобы быстро понять, является ли нужное нам соединение ионным, выполните следующие действия:
- Посмотрите, какие элементы входят в состав соединения. Формула вещества с ионной связью должна включать металл и неметалл. Если это щелочной металл (I группа таблицы Менделеева) и галоген (VII группа), то связь между ними точно ионная.
- По шкале Полинга определите электроотрицательности обоих элементов соединения. Если разница между ними больше 1,7 — связь ионная. Это объясняется тем, что такой тип связи характерен для веществ, у которых сильно отличаются показатели электроотрицательности.
Дополнительным способом убедиться в правильности результата может стать оценка физических свойств вещества. Если оно имеет высокую температуру кипения или плавления и проводит электроток — связь скорее всего ионная.
Вопросы для самопроверки:
- Опишите, как образуется ионная связь. Какие условия для этого необходимы?
- Что такое координационное число элемента в ионном соединении?
- Каковы основные физические свойства ионных соединений?
- В чем разница между характеристиками ионной и ковалентной связей?
- Как можно определить ионную связь, зная электроотрицательность элементов в соединении?
Бесплатный курс для современных мам и пап от детского психолога Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Источник