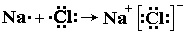Ионная связь
Ионная связь – это связь между ионами, осуществляемая электростатическим притяжением. Она образуется между элементами, которые резко отличаются по электроотрицательности (типичные металлы с типичными неметаллами). Атомы металлов отдают свои валентные электроны и превращаются в положительно заряженные ионы, а атомы неметаллов принимают электроны и превращаются отрицательно заряженные ионы. Положительно и отрицательно заряженные ионы притягиваются, образуя ионные соединения. Например, при образовании хлорида натрия атом натрия отдает один электрон и приобретает электронную конфигурацию перед ним стоящего инертного элемента (10Ne 1s 2 2s 2 2p 6 ; 11Na + 1s 2 2s 2 2p 6 ), а атом хлора принимает его и приобретает электронную конфигурацию за ним стоящего инертного элемента:
Между ионами Na + и Сl – возникают силы электростатического притяжения, в результате чего и образуется хлорид натрия:
Следует отметить, что валентность элемента в соединениях с ионными связями равна его степени окисления, т. е. числу отданных или принятых электронов. Согласно современной теории химической связи механизм образования ионной связи такой же, как и ковалентной (путем перекрывания электронных облаков), но с последующим переходом общей электронной пары к резко электроотрицательному элементу, например:
Следовательно, природа химической связи едина, и ионную связь рассматривают как предельный случай ковалентно–полярной связи. Поэтому говорят о степени ионности связи. Даже в таком соединении как CsF ионная связь выражена только на 89 %, т. е. молекул с чисто ионной связью нет. Степень ионности связи возрастает с увеличением разности электроотрицательности образующих ее атомов, табл. 9.
Таблица 9 – Зависимость степени ионности от разности ЭО атомов
Связи с разностью ЭО больше 1,7 относятся к ионным, а с меньшей – к ковалентным полярным.
Ионная связь, в отличие от ковалентной, не обладает направленностью и насыщаемостью. Электрическое поле иона имеет сферическую симметрию, поэтому взаимодействие между ионами осуществляется одинаково, независимо от направления.
Кроме того, взаимодействие двух противоположно заряженных ионов не приводит к полной компенсации их полей, они сохраняют способность притягивать ионы противоположного знака. Поэтому ионная связь не обладает насыщаемостью. Следствием особенностей ионной связи является соединение ионов с образованием ионной кристаллической решетки. Например, в кристалле Na + Cl – каждый ион Na + окружен ионами Cl – и наоборот. А молекулы хлорида натрия NaCl образуются только в газообразном состоянии.
Металлическая связь
Атомы металлов на внешнем энергетическом уровне имеют небольшое число электронов, но много свободных валентных орбиталей, кроме этого они обладают большими радиусами и низкой энергией ионизации. При сближении атомов в результате образования кристаллической решетки валентные орбитали соседних атомов перекрываются, в образовавшемся кристалле число электронов значительно меньше числа орбиталей и поэтому электроны свободно движутся из одной орбитали в другую, становятся общими и осуществляют связь между всеми атомами кристалла металла. Схематически для описания металлической связи используют модель «свободного электрона». Согласно этой модели атомы металлов отдают наружные электроны и превращаются в положительно заряженные ионы. Оторвавшиеся от атомов электроны образуют «электронный газ», который равномерно распределяется между всеми ионами и соединяет их.
Металлическая – это связь между положительными ионами металлов и оторвавшимися электронами. Она характерна для металлов в твердом и жидком состоянии, а в парообразном – атомы металлов связаны между собой ковалентной связью. Пары металлов состоят из отдельных молекул (Na2, K2, Сu2 и т.д.).
Металлическая связь имеет черты сходства и отличия с ковалентной и ионной связями. Как при ковалентной, так и при металлической, валентные электроны переходят в общее пользование. Но в случае металлической связи эти электроны связывают все атомы данного образца металла, а в случае ковалентной связи – два атома. В отличие от ковалентной связи металлическая связь не имеет направленного характера. Как при ионной связи, так и при металлической, имеются ионы. Но в металлах положительные ионы удерживаются свободно перемещающимися электронами, а в веществах с ионной связью – отрицательно заряженными ионами.
Источник
Химия. 11 класс
Любое химическое соединение — молекулу (CO2), кристалл (NaCl), сложный ион () — с точки зрения электронного строения можно представить в виде системы, состоящей из атомных ядер и связывающих их электронов. Взаимодействие, которое делает эту систему устойчивой, называют химической связью.
Химическая связь — это взаимодействие, в результате которого отдельные атомы объединяются в более сложные системы (молекулы, кристаллы, ионы и др.).
Химическая связь обусловлена действием сил притяжения и отталкивания между положительно заряженными ядрами и отрицательно заряженными электронами, то есть имеет электростатическую природу.
Электроны, которые принимают участие в образовании химических связей, называют валентными. Это электроны внешних электронных оболочек атомов.
Рассмотрим, как и почему образуется химическая связь.
Основным условием образования химической связи является понижение полной энергии системы ядер и электронов по сравнению с энергией изолированных атомов.
Уменьшение полной энергии системы ядер и электронов достигается в результате совместного использования электронов разными атомами. В зависимости от того, как в результате распределена электронная плотность, различают три типа химической связи: ковалентную, ионную и металлическую.
Механизмы образования этих связей вы уже рассматривали при изучении химии в 8–10-х классах. Здесь мы дополним понятие химической связи представлениями о состоянии электронов в атоме.
Источник
Химические связи
Химическая связь — связь между атомами в молекуле или молекулярном соединении, возникающая в результате переноса электронов с одного атома на другой, либо обобществления электронов для обоих атомов.
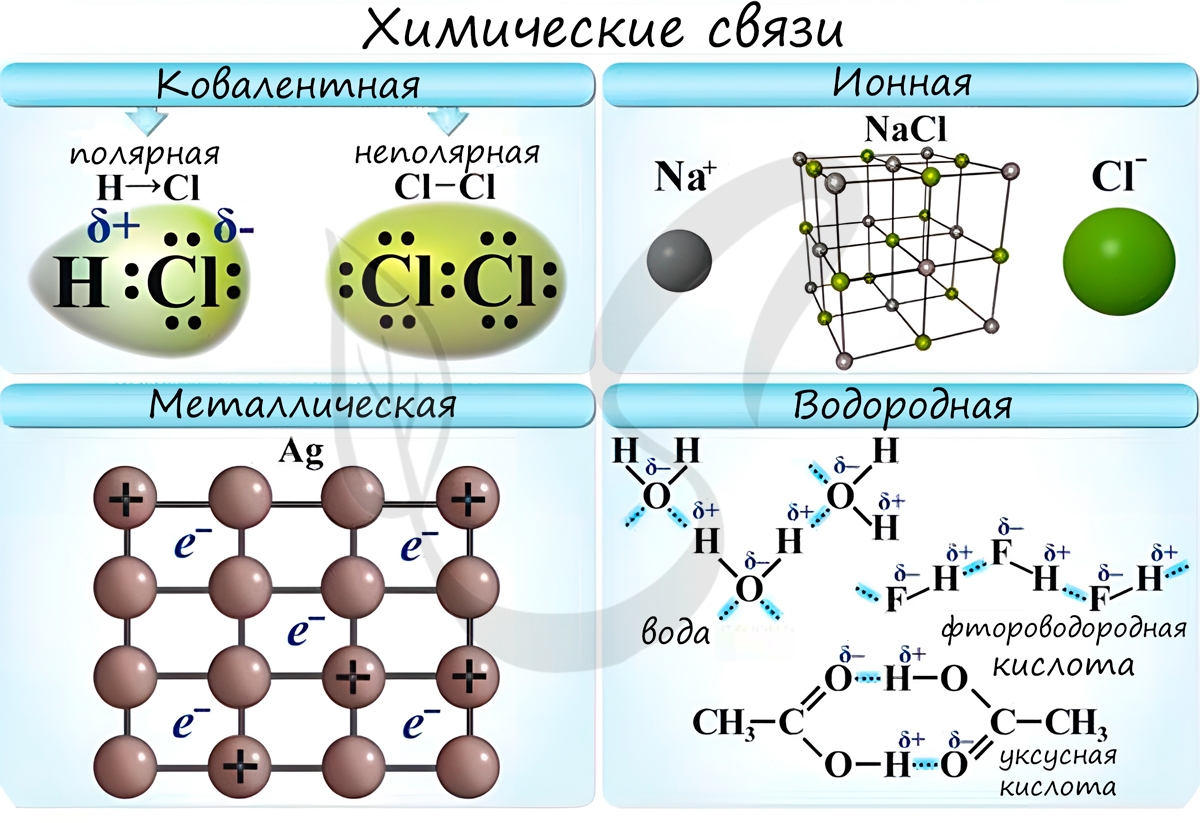
Различают несколько типов химических связей: ковалентная, ионная, металлическая, водородная.
Ковалентная связь ( лат. со — совместно + valens — имеющий силу)
Ковалентная связь возникает между двумя атомами по обменному механизму (обобществление пары электронов) или донорно-акцепторному механизму (электронов донора и свободной орбитали акцептора).
Ковалентной связью соединены атомы в молекулах простых веществ (Cl2, Br2, O2), органических веществ (C2H2), а также, в общем случае, между атомами неметалла и другого неметалла (NH3, H2O, HBr).
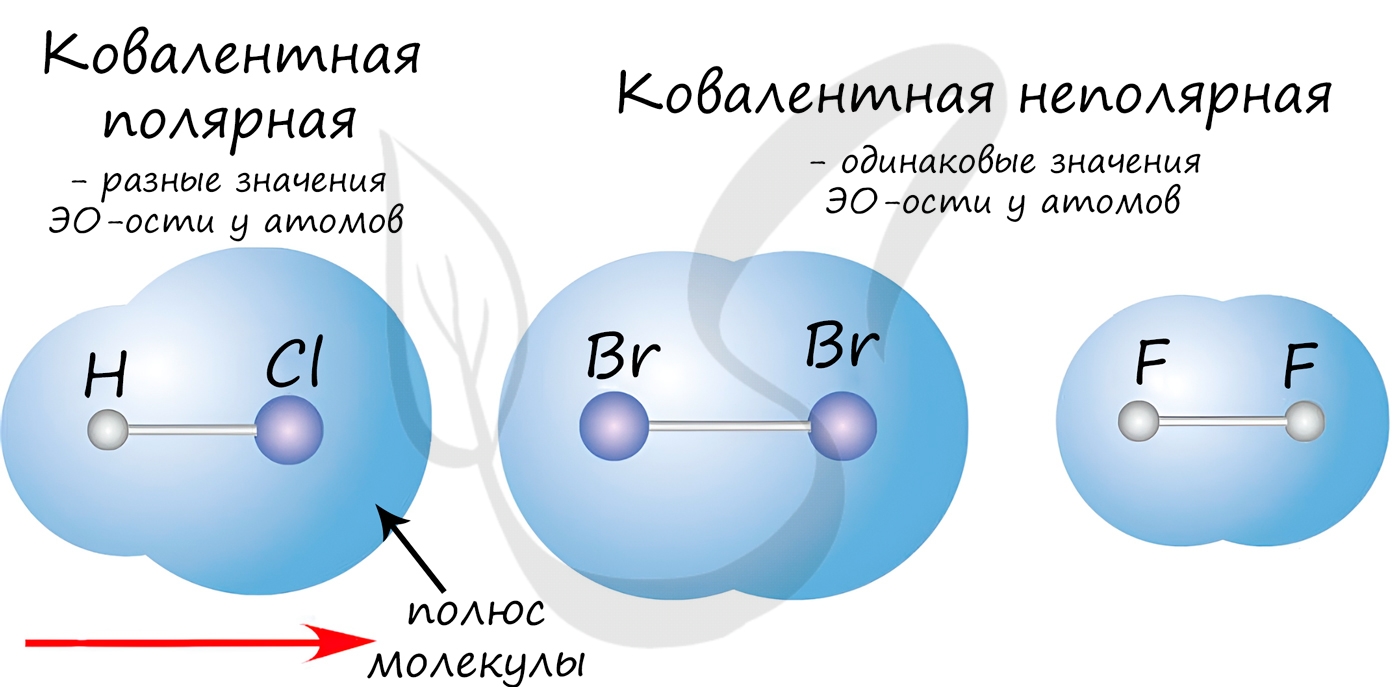
Если атомы, образующие ковалентную связь, имеют одинаковые значения электроотрицательности, то связь между ними называется ковалентной неполярной связью. В таких молекулах нет «полюса» — электронная плотность распределяется равномерно. Примеры: Cl2, O2, H2, N2, I2.
Если атомы, образующие ковалентную связь, имеют разные значения электроотрицательности, то связь между ними называется ковалентной полярной. В таких молекулах имеется «полюс» — электронная плотность смещена к более электроотрицательному элементу. Примеры: HCl, HBr, HI, NH3, H2O.
Ковалентная связь может быть образована по обменному механизму — обобществлению электронной пары. В таком случае каждый атом «одинаково» вкладывается создание связи. Например, два атома азота, образующие молекулу N2, отдают по 3 электрона с внешнего уровня для создания связи.
Существует донорно-акцепторный механизм образования ковалентной связи, при котором один атом выступает в качестве донора неподеленной электронной пары. Другой атом не тратит свои электроны, а только лишь предоставляет орбиталь (ячейку) для этой электронной пары.
- NH4 + — в ионе аммония
- NH4 + Cl, NH4 + Br — внутри иона аммония во всех его солях
- NO3 — — в нитрат ионе
- KNO3, LiNO3 — внутри нитрат иона во всех нитратах
- O3 — озон
- H3O + — ион гидроксония
- CO — угарный газ
- K[Al(OH)4], Na2[Zn(OH)4] — во всех комплексных солях есть хотя бы одна ковалентная связь, возникшая по донорно-акцепторному механизму
Ионная связь
Ионная связь — один из видов химической связи, в основе которого лежит электростатическое взаимодействие между противоположно заряженными ионами.
В наиболее частом случае ионная связь образуется между типичным металлом и типичным неметаллом. Примеры:
Большой подсказкой служит таблица растворимости, ведь все соли имеют ионные связи: CaSO4, Na3PO4. Даже ион аммония не исключение, между катионом аммония и различными анионами образуются ионные связи, например в соединениях: NH4I, NH4NO3, (NH4)2SO4.
Часто в химии встречаются несколько связей внутри одной молекулы. Рассмотрим, например, фосфат аммония, обозначив тип каждой связи внутри этой молекулы.
Металлическая связь
Металлическая связь — вид химической связи удерживающая вместе атомы металла. Этот тип связи выделен отдельно, так как его отличием является наличие высокой концентрации в металлах электронов проводимости — «электронного газа». По природе металлическая связь близка к ковалентной.
«Облако» электронов в металлах способно приходить в движение под различным воздействием. Именно оно является причиной электропроводности металлов.
Водородная связь
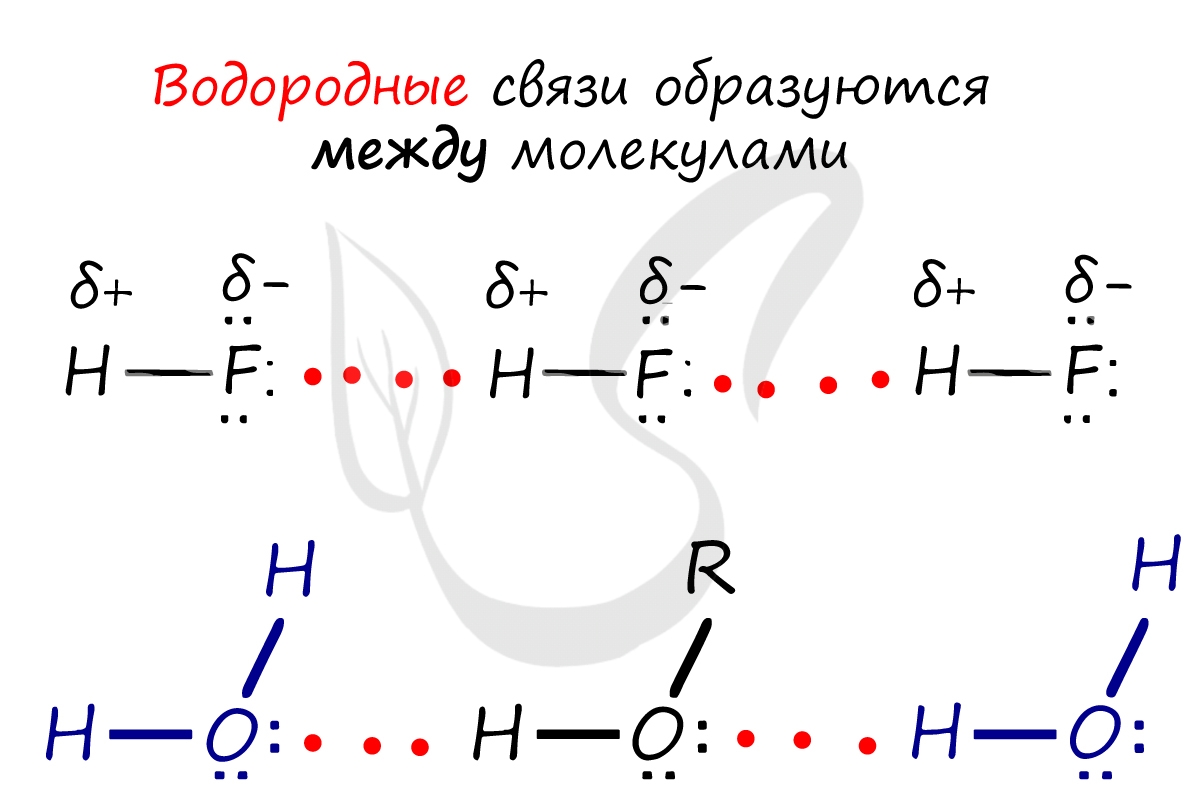
Водородная связь — вид химической связи, образующийся между некоторыми молекулами, содержащими водород. Одна из наиболее частых ошибок считать, что в самом газе, водороде, имеются водородные связи — это вовсе не так.
Водородные связи возникают между атомом водорода и другим более электроотрицательным атомом (O, S, N, C).
- H2O
- NH3
- HF
- Органических спиртов: С2H5OH, C3H7OH
- Органических кислот: CH3COOH, C2H5COOH
Отчасти за счет водородных связей наблюдается то самое исключение, связанное с усилением кислотных свойств в ряду галогеноводородных кислот: HF → HCl → HBr → HI. Фтор является самым ЭО-ым элементов, сильно притягивает к себе атом водорода другой молекулы, что снижает способность кислоты отщеплять водород и снижает ее силу.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Химические связи
Источник