Современное представление о природе химической связи. Типы химической связи
Природа химической связи едина: она имеет электрическое происхождение. Химическое взаимодействие обусловлено обменно-спиновым взаимодействием между электронами атомов, участвующих в образовании химической связи. Проявление сил химического взаимодействия весьма многообразно. Различают следующие основные типы химических связей: 1) ионная (электровалентная, гетерополярная) химическая связь; 2) ковалентная (атомная, гомеополярная) химическая связь, в том числе донорно-акцепторная (координационная); 3) металлическая связь (существует в металлах); 4) межмолекулярное взаимодействие (в том числе водородная связь). Все эти связи важны, особенно первые три типа. В общем случае характер связи между атомами элементов определяется различием величин их электроотрицательности, которая представляет собой сумму энергий ионизации элемента и его сродства к электрону. Между разностью электроотрицательностей связывающихся атомов и сдвигом электронного облака существует зависимость: чем больше разность электроотрицательностей атомов, тем больше и степень ионности образующейся связи, которую обычно оценивают в процентах.
Атомная связь (ковалентная связь)
Льюис и Ленгмюр в 1916 г. на основе теории строения электронной оболочки Н. Бора предложили новую теорию химической связи – теорию ковалентной связи, которая позволяет охватить практически все разновидности химической связи. Согласно этой теории, атомы в молекуле связаны между собой за счет образования общих электронных пар. При этом количество электронов, отдаваемых атомами для образования связывающих пар, определяет их степень окисления. Например, на рис. 3.1 показано образование молекул фтора.
Рис. 3.1. Образование молекулы F2
Позднее, в 1927 г. Лондон и Гейтлер развили эту теорию. Они провели квантовомеханический расчет энергии для молекулы водорода, используя уравнения Шредингера, и показали, что атомы водорода могут образовать молекулу лишь в том случае, если их электроны будут иметь противоположные по знаку спины. Если спины параллельны, то атомы будут отталкиваться и химическая связь не образуется.
Расчет впервые показал подлинную причину возникновения химической связи: стремление атомов к устойчивым двух- и восьми- электронным оболочкам благородных газов, а электрические силы, действующие между ядрами и движущимися электронами, обусловливают соединение атомов в молекулы.
Рассмотрим образование молекулы водорода: Н+Н = Н2 + 431 кДж/моль. Молекула Н2 включает два протона и два электрона. В ней действуют силы: две силы отталкивания между протонами и электронами и 4 силы притяжения между протонами и электронами
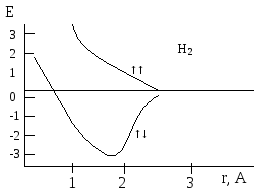
Рис 3.2.Кривые потенциальной энергии для молекулы водорода
Рис. 3.3. Перекрывание электронных облаков в молекуле водорода
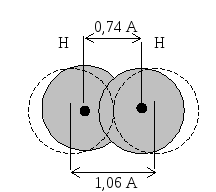
При сближении двух атомов водорода электроны стремятся попасть в межъядерное пространство вследствие электрического притяжения ядрами. На это проникновение влияет их спин. Возможны два случая (рис. 3.2, 3.3): а)спины параллельны (электроны отталкиваются, нет межатомного связывания), кривая 1 – потенциальная энергия системы при сближении атомов А и В растет; б) кривая 2 – спины направлены в противоположные стороны – сила притяжения между электронами значительно превосходит силу отталкивания их как одноименных зарядов, и оба электрона будут находиться в межъядерном пространстве, что приводит к появлению межатомной силы притяжения, которая называется ковалентной связью. Между ядрами появляется повышенная электронная плотность. Таким образом, ковалентная связь образована двумя электронами с антипараллельными спинами, движущимися в поле двух ядер. Это энергетически более выгодно, чем движение каждого электрона в поле своих ядер, происходит натекание электронной плотности в межъядерное пространство, и ядра как бы стягиваются. Происходит сближение ядер и перекрывание облаков. В молекуле Н2 r(Н1 – Н2) = 0,74 Å, в то время как сумма двух радиусов, определенных по Бору, составляет 0,53+ +0,53 = 1,06 Å . Чем больше область перекрывания, тем прочнее связь, тем устойчивее молекула.
Спиновая теория валентности была развита Гейтлером, Лондоном, Слейтером и Полингом, выполнившими квантовомеханические расчеты и показавшими роль спина. Эта идея спаривания электронов была высказана еще в 90 г. XIX в. Н.А. Морозовым. Он писал: «Во всех случаях, где обнаруживается соединение друг с другом пары однородных пунктов атомного сцепления, оно происходит путем спаривания их зарядов, как бы слившихся в один». Работами Гейтлера, Лондона, Полинга была разработана так называемая теория валентных связей или теория локализованных пар, которая получила широкое распространение для описания образования химической связи во многих соединениях. В настоящее время широко применяют два подхода к рассмотрению системы их химически связанных атомов, две теории химической связи: метод валентных связей (МВС) и метод молекулярных орбиталей (ММО).
Метод валентных связей (МВС) или метод локализованных электронных пар. Основные положения МВС: а) связывающее звено между атомами – общие электронные пары, каждая из которых образуется за счет перекрывания по одному электронному облаку от двух атомов и локализованы между ядрами этих атомов; б) обобщаться могут лишь неспаренные электроны; в) образование связи между неспаренными электронами двух атомов возможно лишь при антипараллельных спинах; г) образование общей пары электронов вызывает в пространстве между ядрами (по линии связи) повышение концентрации электронной плотности (причина связи); д) образующаяся связь – двухцентровая, и пара электронов находится на энергетическом уровне, общем для всей молекулы; е) общая пара – единица химической связи – единица валентности каждого из двух атомов; ж) число общих электронных пар у данного атома с другими атомами определяет число валентных связей.
Основные свойства ковалентной связи. Направленность. Идея Полинга: связи образуются в направлении максимального перекрывания электронных облаков вдоль линии, соединяющей ядра взаимодействующих атомов. Для s-электронов направление не имеет значения. Для р-электронов уже не безразлично, в каком направлении приближается другой атом. Таким образом, конфигурация молекулы из двух и более атомов будет определяться взаимным расположением АО, участвующих в образовании химической связи. Например, молекулу воды ранее (доквантовая теория) считали линейной. Однако экспериментальные данные свидетельствовали, что угол между связями О―Н равен 105º.
Угловая структура Н2О легко объясняется с учетом направления 2р-орбиталей кислорода (они направлены под углом 90º). Увеличение угла до 105º объясняется эффектом расталкивания электронных облаков и ядер водорода. Аналогично структура NH3 в виде тетраэдра объясняется участием в связи трех 2р-АО атома азота, направленных под углом друг к другу в 90º. Для объяснения структурных особенностей тех или иных молекул в МВС получила широкое распространение концепция гибридизации АО. Которая подробно будет рассмотрена далее (рис. 3.4).














Рz 



N(2рx, 2рy, 2рz)
у H(1S) NH3
Рис. 3.4.Схемы образования молекул:
а- воды из s-орбиталей водорода и негибридных р-орбиталей кислорода (2рХ , 2рУ); б – аммиака из s-орбиталей водорода и негибридных р-орби- талей азота (2рХ , 2рУ , 2рZ)
Насыщаемость ковалентной связи. Чем она вызвана? Почему образуется строго определенное число связей? Почему есть Н2, а не Н3 и т. д.? Причина насыщаемости – ограниченное число неспаренных электронов и принцип Паули.
Например, может ли молекула Н2 присоединить еще один атом водорода Н2 + Н → Н3 МВС утверждает, что образование такой молекулы исключается, так как молекула Н2 насыщена и все валентные возможности (неспаренные электроны) связанных в молекулу атомов водорода исчерпаны.
Другой пример, нет неспаренных электронов, нет и связи. Взаимодействие атомов гелия исключается, так как наборы электронов дадут совпадающие спины, что приведет к преобладанию компоненты отталкивания.


По МВС, если у атома нет неспаренных электронов, то взаимодействие между ними исключается. Но вот интересный пример: Be ↑↓ 2s 2 – нет неспаренных электронов, а дает BeCl2. У Ве есть вакантные орбитали, и один из s-электронов возбуждается и переходит на р-орбиталь. Такой Ве* уже может взаимодействовать с образованием двух ковалентных связей.
Ве 1s 2 2s 2 → Ве* 1s 2 2s 1 2p 1
Источник
Гродно 2010
Рецензенты: доктор биологических наук, профессор кафедры химии Учреждения образования «Гродненский государственный аграрный университет» З.В. Горбач, кандидат химических наук, доцент кафедры общей и неорганической химии Учреждения образования «Белорусский государственный технологический университет» Л.И.Хмылко.
Природа химической связи: лекции по курсу «Общая химия» для студентов сельскохозяйственных специальностей / З.В. Апанович. – Гродно: ГГАУ , 2010. – 37 с.
Учебно-методическое пособие включает лекции по отдельным темам курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического, ветеринарного и факультета защиты растений. Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Рекомендовано межфакультетской методической комиссией инженерно–технологического факультета 30 сентября 2010г. (протокол № 1).
© УО «Гродненский государственный аграрный университет»,2010
Природа химической связи
1) Развитие представлений о природе химической связи. Ее характеристики.
2) Свойства ковалентной связи.
3) Типы связей. Кратность связи.
4) Определение валентности по методу валентных связей (МВС).
5)Донорно-акцепторный механизм образования ковалентной связи.
6)Гибридизация атомных орбиталей (АО).
7) Полярность ковалентной связи.
8) Межмолекулярное взаимодействие. Водородная связь.
9) Понятие о методе молекулярных орбиталей (ММО).
Вопрос 1. Развитие представлений о природе химической связи. Ее характеристики.
Все вещества образуются в результате возникновения между атомами, входящими в их состав, прочных связей, называемых химическими. Все химические процессы происходят в результате перегруппировок атомов, сопровождающихся разрывом старых связей между ними и образованием новых. Не существует химических реакций, в ходе которых связи между атомами не изменялись бы. Поэтому вопрос о природе химической связи всегда считался важнейшим вопросом химии. Какова природа сил, связывающих атомы в молекулы? В начале XIX века французский ученый Бертолле и шведский ученый Бергман предположили, что характер этих сил гравитационный (взаимодействие масс атомов).
Гравитационная теория сменилась первой электрохимической теорией, предложенной шведским ученым Берцеллиусом. Он полагал, что различные атомы обладают противоположными электрическими зарядами, благодаря чему между ними возникает электростатическое притяжение. Однако и эта теория была отвергнута, т.к. не объясняла образования молекул из одинаковых атомов, но тем не менее она ближе к современной.
Большим вкладом в развитие представлений о строении молекул явилась теория химического строения Бутлерова (разработанная в 1861 г.).
Однако только после открытия электронного строения атомов удалось решить вопрос о природе химической связи. Впервые немецкий ученый Коссель в 1916г. предположил, что при взаимодействии атомов, один из них отдает, а другой принимает электроны. В том же году американским ученым Льюисом предложена теория образования химической связи с помощью электронных пар, принадлежащих одновременно двум атомам. Современное учение о химической связи развивалось на основе работ Косселя и Льюиса.
Главной причиной возникновения химических связей между атомами является понижение полной энергии системы при переходе от свободных взаимодействующих атомов к молекуле.
Природа химической связи по современным представлениям электрическая, объясняется взаимодействием электрических полей, образуемых электронами и ядрами атомов, участвующих в создании молекулы.
Любая молекула обладает меньшим запасом энергии, чем совокупность атомов, из которых она образуется. Из этого следует, что при образовании молекул из атомов энергия выделяется, в количестве, которое необходимо для разложения молекулы на атомы. Количественной характеристикой прочности связи является — энергия связи (Е) она равна работе, которую необходимо затратить на разрыв связи.
Н2 = Н + Н ЕН2 = 435 кДж/моль
В молекуле водорода энергия связи высока, что объясняется небольшими размерами взаимодействующих атомов.
Геометрической характеристикой является длина связи (r0) — межъядерное расстояние между химически связанными атомами, когда силы притяжения уравновешены силами отталкивания и энергия системы минимальна.
Для молекулы Н2 r0 = 0,074 нм.
Источник