- 2.1.3. Виды межмолекулярных сил притяжения
- Силы взаимодействия молекул
- Природа сил взаимодействия молекул
- Виды межмолекулярных сил
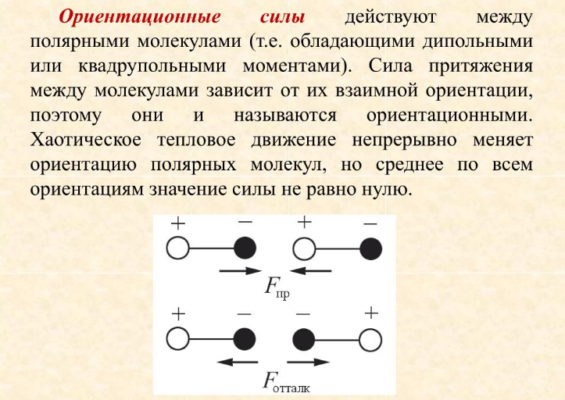
- Ориентационные силы
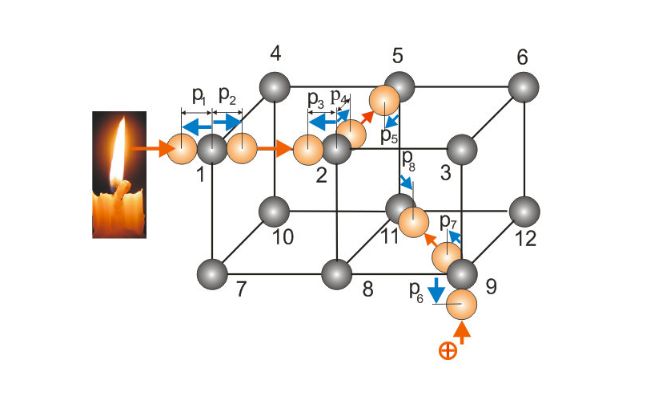
- Поляризационные (индукционные) силы
- Дисперсионные силы
- Что мы узнали?
- Взаимное притяжение и отталкивание молекул
- Общее описание
- Природа сил отталкивания и притяжения
- Что мы узнали?
2.1.3. Виды межмолекулярных сил притяжения
Наличие межмолекулярных сил мало сказывается на подвижности молекул в газовой фазе. В кристаллах взаимодействие между молекулами или ионами выражено сильно, поэтому образуются жесткие структуры. В жидкостях кинетическая энергия молекул сравнима с потенциальной энергией их взаимодействия. Силы притяжения, удерживающие молекулы вместе, носят название ван-дер-ваальсовых сил. Их можно подразделить на три типа: 1) диполь-дипольное взаимодействие между полярными молекулами, 2) взаимодействие диполь — индуцированный диполь и, наконец, 3) взаимодействие индуцированный диполь — индуцированный диполь, которое еще называют дисперсионным взаимодействием. Эти виды взаимодействия наряду с такими специфическими взаимодействиями, как водородная связь или перенос заряда в донорно-акцепторных комплексах, обусловливают наличие полимолекулярной структуры в жидкостях и молекулярных кристаллах, определяют температуры кипения и плавления вещества, а в газах обусловливают отклонения от идеального поведения. Ван-дер-ваальсовы силы притяжения обычно пропорциональны R 6 , т.е. расстоянию между взаимодействующими диполями в шестой степени. Это значит, что ван-дер-ваальсово взаимодействие проявляется на малых расстояниях и быстро убывает с увеличением этого расстояния.
Если две полярные молекулы находятся близко друг к другу, их диполи взаимодействуют. В жидкости одна молекула вращается во всех плоскостях относительно другой, поэтому можно ожидать, что при очень высоких температурах силы притяжения (когда диполи ориентированы по типу «голова к хвосту») будут уравновешиваться силами отталкивания (когда диполи ориентированы «голова к голове»). Однако при умеренных температурах преобладает тенденция диполей «выстраиваться в линию» с образованием такой предпочтительной конфигурации, когда силы притяжения преобладают над силами отталкивания.
Присутствие полярной молекулы вблизи другой молекулы, которая сама может быть как полярной, так и неполярной, оказывает на вторую молекулу поляризующее действие. Индуцированный диполь может затем взаимодействовать с дипольным моментом первой молекулы, и тогда две молекулы становятся связанными одна с другой. Величина этого эффекта зависит как от величины постоянного дипольного момента первой молекулы, так и от поляризуемости второй молекулы. Важно, что при повышении температуры тепловое движение не может дезориентировать индуцируемый момент от направления индуцирующего момента, т.е. эффект притяжения сохраняется, даже если полярная молекула свободно вращается вблизи поляризуемой молекулы.
Легко поляризуемые неполярные молекулы хотя и не обладают постоянными дипольными моментами, но их электронные облака флуктуируют, поэтому их можно рассматривать как частицы, имеющие мгновенный дипольный момент, который постоянно меняет свою величину и направление. Если одна молекула быстро перешла в электронную конфигурацию, которая дает мгновенный диполь m1*, то этот диполь будет поляризовать другую молекулу, индуцируя в ней мгновенный диполь m2*. Диполи m1* и m2* притягиваются друг к другу. Хотя направление диполя m1* будет изменяться и далее, вторая молекула будет реагировать на это изменение, и эффект притяжения все время сохраняется. Величина таких дисперсионных сил, или сил Лондона, зависит от поляризуемости обеих молекул.
Обобщенное выражение для всех трех видов ван-дер-ваальсовсовых взаимодействий имеет вид
V = —C6/R 6 ,
где V — потенциальная энергия; R — расстояние; C6 — некоторый коэффициент, зависящий от природы молекулы.
Хотя для всех трех типов взаимодействий энергия изменяется пропорционально R — 6 , только диполь-дипольное взаимодействие зависит от температуры, и при очень высоких температурах энергия стремится к нулю. Это связано с тем, что тепловое движение не может нарушить взаимную ориентацию постоянного и индуцируемого диполей или двух индуцированных диполей.
Источник
Силы взаимодействия молекул
Существование различных агрегатных состояний вещества объясняется тем, что между молекулами существуют силы притяжения и отталкивания. При изменении температуры баланс этих сил и энергии теплового движения изменяется, что и приводит к изменению состояния вещества. Кратко рассмотрим силы взаимодействия между молекулами.
Природа сил взаимодействия молекул
В 10 классе известно, что атомы всех элементов состоят из положительно заряженного ядра и отрицательно заряженных электронных оболочек вокруг. Взаимодействие электронных оболочек приводит к образованию молекул, состоящих из некоторого числа атомов.
Получается, что в любой молекуле существуют области, имеющие как положительный, так и отрицательный заряд. Распределение этих областей и создает силы, действующие на молекулы в данный момент времени, а с учетом изменения температуры оно определяет строение газообразных, жидких и твердых тел.
При этом природа этих сил всегда электростатическая. Впервые они были описаны в середине XIX в. Я. Ван-дер-Ваальсом. Поэтому нередко их называют ван-дер-ваальсовыми.
Виды межмолекулярных сил
Из-за того, что силы притяжения между молекулами изменяют пространственную ориентацию и форму самих молекул, они гораздо сильнее изменяются с изменением расстояния, как правило, пропорционально седьмой степени.
Это убывание гораздо быстрее, чем обычное кулоновское, пропорциональное квадрату расстоянию. Поэтому межмолекулярные силы играют значительную роль лишь на малых расстояниях.
По механизму их возникновения можно выделить следующие.
Ориентационные силы
Ориентационные силы еще называют дипольными. Они возникают в результате того, что многие молекулы представляют собой электрические диполи. Разноименные полюса диполей притягиваются, а одноименные — отталкиваются. В результате дипольные молекулы стремятся занять определенное пространственное положение друг относительно друга, что также влияет на величину сил.
В результате ориентационные силы прямо пропорциональны дипольным моментам молекул:
Поляризационные (индукционные) силы
Собственный дипольный момент молекул приводит к тому, что он наводит (индуцирует) небольшой дипольный момент у близлежащих молекул, немного «растягивая» их. Если близлежащие молекулы полярны, то индуцированный момент не играет большой роли по сравнению с собственным. Однако, если близлежащая молекула неполярна, то силы небольшого индуцированного момента будут заметны.
Сила взаимодействия будет пропорциональна дипольному моменту полярной молекулы и способности к поляризации под внешним воздействием неполярной молекулы (поляризуемости $\alpha$):
Дисперсионные силы
Поляризуемость неполярных молекул приводит к тому, что даже между ними возникают силы притяжения.
Хотя в среднем у неполярной молекулы дипольный момент отсутствует, в каждый конкретный момент времени электроны в электронном облаке могут иметь несимметричное положение. В результате мгновенный дипольный момент будет отличен от нуля. То же самое происходит и с соседними молекулами. Суммарное взаимодействие этих мгновенных дипольных моментов приводит к существованию сил притяжения, называемых дисперсионными.
Дисперсионные силы пропорциональны поляризуемостям взаимодействующих молекул:
Что мы узнали?
Силы взаимодействия молекул имеют электростатическую природу. Механизм их возникновения определяется существованием дипольных моментов у молекул. По виду эти силы делятся на ориентационные, поляризационные и дисперсионные. Их величина пропорциональная седьмой степени расстояния, поэтому они проявляются лишь на относительно небольших дистанциях.
Источник
Взаимное притяжение и отталкивание молекул
Взаимное притяжение и отталкивание молекул обуславливает существование тел. Без них мир выглядел бы как облако мельчайших частиц, не способных вступить в связь и создать большие структуры.
Общее описание
Рассмотрим несколько физических опытов, некоторые из которых можно наблюдать в повседневной жизни. Сухая одежда, если она не наэлектризована, к телу не прилипает. Но если ее намочить, моя руки под краном или потея на тренировке? Ровно тоже происходит с мокрыми листами бумаги – они слипаются. Теперь положим один кусок железа на другой и поставим их в печь, нагретую до 200-300-х градусов. Они склеятся. Или попробуем прижать друг к другу куски разбитой посуды или стекла – они рассыплются. Наконец, сдавим любое тело, для наглядности кистевой эспандер, и отпустим – он распрямится.
Для того, чтобы сделать качественные выводы из этих опытов, достаточно иметь начальное представление о строении вещества, которое дается школьникам в 7 классе. Всё вокруг состоит из молекул и атомов. В газообразных и жидких телах они двигаются свободно, в твердых – связаны в жесткую структуру. Теперь представим, что происходит, если между телами появляется вода: неровности на микроуровне заполняются молекулами воды. Образуется непрерывный слой веществ. При нагревании твердых тел атомы и молекулы, связанные в структуру, начинают колебаться сильнее, из-за чего могут покинуть свои «гнезда» и сблизится с атомами и молекулами других тел. Чем выше температура, тем вероятнее, что это событие произойдет.
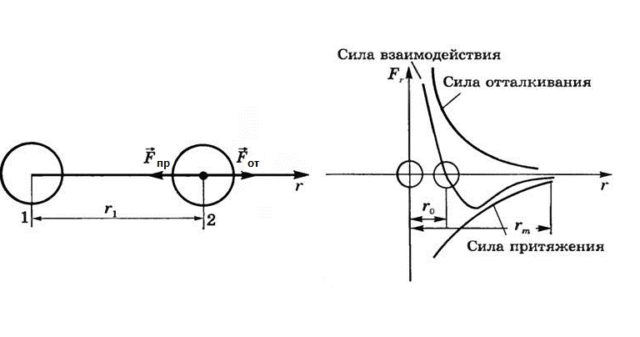
Выходит, когда молекулы сближаются на определенное расстояние, между ними возникает притяжение. И оно тем сильнее, чем ближе они к другу. Но из опыта с кистевым эспандером можно также заключить, что есть некое предельное расстояние, после которого молекулы уже отталкиваются друг от друга.
Со временем ученым удалось дать количественные характеристики этих явлений. Так, если расстояние между молекулами соразмерно диаметру самих молекул, силы притяжения достаточно значительны, чтобы тела соединялись. При большем сближении возникает отталкивание.
Природа сил отталкивания и притяжения
Поскольку атому состоят из ядер и электронов, силы притяжения и отталкивания носят электростатический характер. Когда расстояние между атомами молекул достаточно велико (электронные облака не перекрываются), имеют место три эффекта:
- Дисперсионный (т.к. электроны обращаются вокруг ядер, возможно возникновение кратковременных диполей – структур, в которых есть положительно и отрицательно заряженные стороны. В случае, когда диполи обращены друг к другу разноименными зарядами, возникает сила притяжения. Она цементирует дипольную структуру).
- Ориентационный (некоторые молекулы полярны, то есть состоят из разноименно заряженных ионов. Например, молекула хлорной кислоты состоит из положительного иона водорода и отрицательного хлора. Такие молекулы ориентируются относительно друг к другу разноименно заряженными частями, из-за чего возникает диполь-дипольное взаимодействие).
- Индукционный (неполярная молекула, находясь в поле полярной, также поляризуется – ее электроны сосредотачиваются на одной стороне, а ядро – на другой. Дальнейший механизм аналогичен).
При большем сближении атомов молекул их электронные облака перекрываются, возникают силы отталкивания как между ядрами атомов, так и между их электронами по принципу взаимодействия одноименных зарядов.
Что мы узнали?
В ходе урока были рассмотрены опыты, служащие примерами взаимного притяжения и отталкивания молекул. Дано качественное описание этих явлений на основе молекулярной теории, а также рассмотрена природа сил притяжения и отталкивания молекул.
Источник