- Уравнение реакции с помощью которых можно получить бензол из природного газа
- получения бензола
- Способы получения аренов
- Получение аренов
- 1. Реакция Вюрца-Фиттига
- 2. Дегидроциклизация алканов
- 3. Дегидрирование циклоалканов
- 4. Декарбоксилирование солей бензойной кислоты
- 5. Алкилирование бензола и его гомологов
- 6. Тримеризация ацетилена
- 7. Получение стирола
- Уравнение реакции с помощью которых можно получить бензол из природного газа
- Как получить бензол из метана?
- Если записывать правильно ответ в тетрадь, то решение должно быть записано примерно таким образом:
- Природный газ ацетилен бензол
Уравнение реакции с помощью которых можно получить бензол из природного газа
Мы рассмотрим «классические» методы получения бензола — те, которые описаны в каждом учебнике по химии, и рассмотрим получение из разных классов органических соединений, т.к. цепочки реакций, которые предлагаются в ЕГЭ, подразумевают умение получать бензол «из всего» 🙂
«Классические» реакции
получения бензола
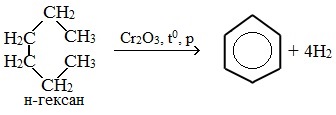
- Ароматизация нефти. Точнее, это реакция циклизации гексана. Называется метод «ароматизация нефти», т.к. из нее получают гексан:
С6H14 → C6H6 + 4H2
Обратите внимание на условия реакции — давление, температуру и катализатор. Они означают, что при обычных условиях гексан не вступит в такую реакцию. Алканы вообще довольно нереакционноспособные вещества.
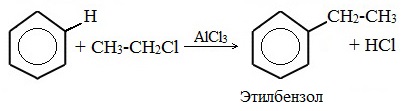
- Получение гомологов бензола: алкилирование бензола:
реакция проводится в присутствии катализатора — галогенидов алюминия, например, AlCl3:
C6H6 + CH3Cl → C6H5CH3 + HCl
Именная реакция — реакция Зелинского. Получение бензола из ацетилена:
3С2H2 → C6H6
1. Получение бензола из неорганических веществ:
- 1 вариант:
Исходное вещество — карбид кальция СaC2:
CaC2 + 2H2O → Ca(OH)2 + C2H2 — ацетилен
дальше — реакция Зелинского : 3С2H2 → C6H6 Это самый короткий путь получения. - 2 вариант:
Исходное вещество — карбид алюминия Al4C3:
Способы получения аренов
Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей. Общая формула: CnH2n–6 при n ≥ 6.
Получение аренов
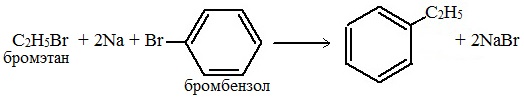
1. Реакция Вюрца-Фиттига
Хлорбензол реагирует с хлорметаном и натрием. При этом образуется смесь продуктов, одним из которых является толуол:
2. Дегидроциклизация алканов
Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды. Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол: Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:
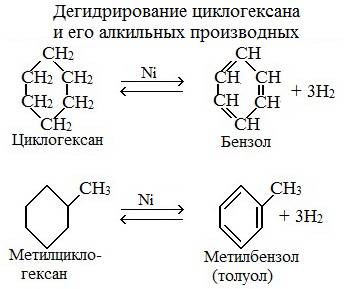
3. Дегидрирование циклоалканов
При дегидрировании циклогексана и его гомологов при нагревании в присутствии катализатора образуется бензол или соответствующие гомологи бензола.
| Например, при нагревании циклогексана в присутствии палладия образуется бензол и водород |
| Например, при нагревании метилциклогексана в присутствии палладия образуется толуол и водород |
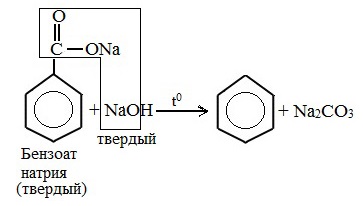
4. Декарбоксилирование солей бензойной кислоты
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. Взаимодействие бензоата натрия с гидроксидом натрия в расплаве протекает аналогично реакции получения алканов по реакции Дюма с образованием бензола и карбоната натрия:
5. Алкилирование бензола и его гомологов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
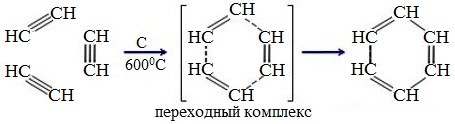
6. Тримеризация ацетилена
При нагревании ацетилена под давлением над активированным углем молекулы ацетилена соединяются, образуя бензол.
При тримеризации пропина образуется 1,3,5-триметилбензол.
7. Получение стирола
Стирол можно получить дегидрированием этилбензола:
Стирол можно также получить действием спиртового раствора щелочи на продукт галогенирования этилбензола (1-хлор-1-фенилэтан):
Уравнение реакции с помощью которых можно получить бензол из природного газа
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание2
Назовите основные продукты химической переработки природного газа и укажите процессы, с помощью которых их получают. Запишите уравнения соответствующих реакций.
Углерод (сажа), водород и ацетилен. Процесс получения: пиролизом (нагреванием без доступа воздуха)
CH4 t ⟶ C + 2H2↑
2CH4 t ⟶ C2H2 + 3H2↑
Синтез-газ. Процесс получения: конверсия (превращение) водяных паров с метаном:
CH4 + H2O t ⟶ CO + 3H2↑
Бензин и метиловый спирт Процесс получения: промышленный синтез :
nCO + (2n+1) H2 кат. ⟶ CnH2n+2 + nH2O
CO + 2H2 кат. ⟶ CH3OH
Галогенпроизводные. Процесс получения: галогенирование (присоединение галогенов) :
CH4 + Cl2 свет ⟶ CH3Cl + HCl
CH3Cl + Cl2 свет ⟶ CH2Cl2 + HCl
CH2Cl2 + Cl2 свет ⟶ CHCl3 + HCl
CHCl3 + Cl2 свет ⟶ CCl4 + HCl
Задание 3
Укажите важнейшие месторождения природного газа в Российской Федерации. Найдите их на карте полезных ископаемых нашей страны. Уренгой, Ямбург, Бованенковское, Штокмановское, Ленинградское, Русановское, Заполярное, Медвежье, Астраханское, Западно-Камчатский шельф, Сахалин, Среднеботуобинское нефтегазоконденсатное месторождение, Оренбургское газоконденсатное месторождение, Игримское, Ледовое, Ковыктинское.
Задание 4 Объёмные доли алканов в природном газе некоторого месторождения равны: метан – 82%, этан – 12%, пропан – 6%. Определите их массовые доли.
Дано: φ(CH4)=82%, φ(C2H6)=12%, φ(C3H8)=6%
Найти: ω(CH4)-?, ω(C2H6)-?, ω(C3H8)-?
Решение
1. Допустим имеется 1 л природного газа. Вычисляем объём каждого газа в смеси природного газа:
V(CH4)=φ(CH4)•V(смеси) : 100%=82% • 1 л : 100%= 0,82 л
V(C2H6)=φ(C2H6)•V(смеси) : 100%=12% • 1 л : 100%= 0,12 л
V(CH4)=φ(C3H8)•V(смеси) : 100%=6% • 1 л : 100%= 0,06 л
2. Вычисляем массу каждого газа.
M(CH4)=16 г/моль, M(C2H6)=30 г/моль, M(C3H8)=44 г/моль
m(CH4)=V(CH4)•M(CH4):Vm=0,82 л • 16 г/моль : 22,4 л/моль = 0,586 г
m(C2H6)=V(C2H6)•M(C2H6):Vm=0,12 л • 30 г/моль : 22,4 л/моль = 0,161 г
m(C3H8)=V(C3H8)•M(C3H8):Vm=0,06 л • 44 г/моль : 22,4 л/моль = 0,118 г
3. Вычисляем массу смеси природного газа:
m(смеси)=m(CH4)+m(C2H6)+m(C3H8)=0,586 г + 0,160 г + 0,118 г = 0,864 г
4. Определяем массовые доли каждого газа в смеси природного газа.
ω(CH4)=(m(CH4):m(смеси)) •100% =(0,586 г : 0,864 г) • 100% = 67,8%
ω( C2H6 )=(m( C2H6 ):m(смеси)) •100% =(0,161 г : 0,864 г) • 100% = 18,6 %
ω( C3H8 )=(m( C3H8 ):m(смеси)) •100% =(0,118 г : 0,864 г) • 100% = 13,6 %
Ответ: ω(CH4)=67,8%, ω(C2H6)=18,6%, ω(C3H8)=13,6%
Задание 5 Рассчитайте объём воздуха (содержащего 20% кислорода), необходимого для сжигания 100 м 3 природного газа (н.у.), в котором объёмные доли метана, этана, пропана и азота равны соответственно 80%, 12%, 6% и 2%.
Дано: φ(O2)=20%, V(смеси)=100 м 3 , φ(CH4)=80%, φ(C2H6)=12%, φ(C3H8)=6%, φ(N2)=2%
Найти: V(воздуха)-?
Решение
В смеси природного газа азот не поддерживает горение.
1. Вычисляем объём метана, этана и пропана в смеси природного газа:
V(CH4)=φ(СН4)•V(смеси):100%=80%•100 м 3 :100%=80 м 3
V(C2H6)=φ(C2H6)•V(смеси):100%=12%•100 м 3 :100%=12 м 3
V(C3H8)=φ(С3Н8)•V(смеси):100%=6%•100 м 3 :100%=6 м 3
2. Составляем химические уравнения сжигания метана, этана и пропана:
СН4 + 2О2 → СО2 + 2Н2О (1)
2С2Н6 + 7О2 → 4СО2 + 6Н2О (2)
2С3Н8 + 10О2 → 6СО2 + 8Н2О (3)
Согласно закону объёмных отношений Гей-Люссака по уравнению реакции (1) имеем V(СН4):V1(О2)=1:2 , поэтому
V1(О2)=2•V(CH4)=2•80 м 3 =160 м 3
Согласно закону объёмных отношений Гей-Люссака п о уравнению реакции (2) имеем V(С2Н6):V2(О2)=2:7 , отсюда по свойству пропорции имеем 2•V(O2)=7•V(C2H6), поэтому V2(О2)=7•V(C2H6):2=7•12 м 3 : 2=42 м 3
Согласно закону объёмных отношений Гей-Люссака п о уравнению реакции (3) имеем V(С3Н8):V3(О2)=2:10=1:5 , поэтому
V3(О2)=5•V(C3H8)=5•6 м 3 =30 м 3
3. Рассчитываем общий объём кислорода, необходимый для сжигания 100 м 3 природного газа:
Источник
Как получить бензол из метана?
Если это задача для школьников, то и будем ее решать путем самым простым.
Сразу получить из метана бензол не получится. В любом случае используем сопутствующие реакции.
Во-первых, для начала из метана мы получим ацетилен. Эта реакция протекает приблизительно при температуре 1500 градусов по Цельсию. Чтобы нагреть метан до такой температуры, его сжигают в условиях ограниченного доступа воздуха.
Во-вторых, используем реакцию Зелинского, которую называют реакцией полимеризации ацетилена (тримеризация). Используется в качестве катализатора активированный уголь, и температура около 600 градусов по Цельсию.
Если записывать правильно ответ в тетрадь, то решение должно быть записано примерно таким образом:
Получить бензол из метана в один ход не получится.
Сначала необходимо получить из метана ацетилен. Получается так называемый пиролиз, когда метан нагревают до 1500 градусов Цельсия и получается ацетилен с двумя атомами углерода и тройной связью:
После этого происходит тримеризация ацетилена, когда из трех молекул ацетилена под воздействием повышенной температуры и катализатора получается бензол.
Роль катализатора играет активированный уголь. Реакция протекает и с получением других веществ, но выход бензола при этом весьма велик, потому метод используется в промышленности.
Вы помните сказку, как солдат из топора кашу варил? Точно так же нужно относиться к Вашему вопросу. Зачем получать бензол из метана, когда проще всего получить его из бензина, точнее из фракции содержащей гексан и его изомеры.
Но, если Вам непременно хочется получить бензол из метана, то алгоритм примерно такой. Если струю поток метана пропустить через электрическую дугу (температура выше 2000°С, процесс называется «электрокрекинг метана»), то в потоке газа произойдут сотни если не тысячи самых различных превращений, и образуются десятки продуктов, среди которых правды в очень малых количества будут и ароматические углеводороды, в том числе и бензол. Но его там так мало, что выделять его из этой смеси и совершенно нецелесообразно. Главными (нужными) продуктами электрокрекинга метана будут этилен, ацетилен и сажа (почти чистый углерод). И Самое главное, эти газы этилен и ацетилен можно сравнительно легко выделить. Ну а как получить из ацетилена бензол — это во всех школьных учебниках написано (пропусканием над активированным углём при высокой температуре порядка 600°С).
Источник
Природный газ ацетилен бензол
Основным природным источником ароматических углеводородов является нефть и каменный уголь.
В промышленности
1.При коксовании (сухая перегонка) каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения.
2.Ароматизация нефти
а) дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора (с числом атомов углерода больше 6):
б) дегидрирование циклоалканов и его гомологов:
3.Тримеризация ацетилена
При пропускании ацетилена над активированным углем образуется бензол (реакция Зелинского):
В лаборатории
1.Декарбоксилирование солей бензойной кислоты (сплавление солей бензойной кислоты с твердой щелочью)
Соли бензойной кислоты называются бензоаты.
2.Гомологи бензола получают из галогенпроизводных (реакция Вюрца- Фиттига)
Реакции получения аренов указывают на взаимосвязь между различными группами углеводородов и на взаимное превращение их друг в друга.
3.Алкилирование бензола (получение гомологов бензола)
Гомологи бензола получают его взаимодействием с галогеналканами или алкенами в присутствии безводного хлорида алюминия (реакция Фриделя-Крафтса):
При дегидрировании этилбензола образуется производное бензола с непредельной боковой цепью – винилбензол (стирол) C6H5-CН=СН2 (исходное вещество для получения ценного полимера полистирола).


Источник