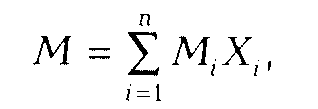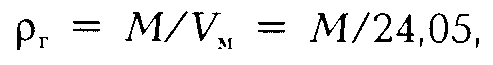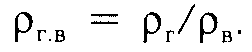4. Основные физико-химические свойства нефтяного и природного газов.
Газы газовых месторождений называются природными газами. Природные углеводородные газы представляют собой смесь предельных УВ. Основным компонентом является метан СН4. Наряду с метаном в состав природных газов входят более тяжелые УВ, а также неуглеводородные компоненты: азот N, углекислый газ СО2, сероводород H2S, гелий Не, аргон Аr.
Попутным или нефтяным газом называется газ нефтяных месторождений, добываемый вместе с нефтью.
Попутный нефтяной газ (ПНГ) представляет смесь газов. Основными составляющими ПНГ являются предельные углеводороды — гомологи метана от СН4 до С6Н14. Суммарное содержание гексана и более тяжелых углеводоро дов в попутном газе, как правило, не превышает 1 %, содержание пентана находится в пределах 2 %. Кроме того, в ПНГ присутствуют инертные газы, в основном, азот и углекислый газ.
На месторождениях нефти Удмуртской Республики и ряде месторождений Пермского края в составе ПНГ преобладает азот (до 80 %), содержание метана составляет 12-15%. Калорийность газа — 1,46 МДж/м 3 . Давления насыщения нефти газом высокие и близки к начальным пластовым давлениям (от 2,7 до 11,5 МПа).
Газовые смеси характеризуются массовыми или молярными концентрациями компонентов. Для характеристики газовой смеси необходимо знать ее среднюю молекулярную массу, среднюю плотность или относительную плотность по воздуху.
где Мi — молекулярная масса i-го компонента; Xi — объемное содержание i-го компонента, доли ед. Для реальных газов обычно М = 16-20.
где Vм — объем 1 моля газа при стандартных условиях. Обычно значение ρг находится в пределах 0,73-1,0 кг/м 3 .
Чаще пользуются относительной плотностью газа по ρг.в, которая определяется по следующей формуле:
,
где ρг- — плотность газа;
ρ в -плотность воздуха при тех же давлении и температуре
Уравнения состояния газов
Уравнения состояния газов используются для определения многих физических свойств природных газов. Уравнением состояния называется аналитическая зависимость между давлением, объемом и температурой.
Состояние газов в условиях высоких давления и температуры определяется уравнением Клайперона — Менделеева:
pV = NRT,
V — объем идеального газа;
N — число киломолей газа;
R — универсальная газовая постоянная;
Эти уравнения применимы для идеальных газов.
Идеальным называется газ, силами взаимодействия между молекулами которого пренебрегают. Реальные углеводородные газы не подчиняются законам идеальных газов. Поэтому уравнение Клайперона — Менделеева для реальных газов записывается в виде
pV=ZNRT,
где Z — коэффициент сверхсжимаемости реальных газов, зависящий от давления, температуры и состава газа и характеризующий степень отклонения реального газа от закона для идеальных газов.
- Коэффициент сверхсжимаемостиZ реальных газов — это отношение объемов равного числа молей реального V и идеального Vи газов при одинаковых термобарических условиях (т.е. при одинаковых давлении и температуре):
Z = V/Vи
Значения коэффициентов сверхсжимаемости наиболее надежно могут быть определены на основе лабораторных исследований пластовых проб газов.
где Pкрi, и Tкрi — критические давление и температура i-го компонента;
Xi — доля i-го компонента в объеме смеси (в долях единицы).
- Влагосодержание природных газов связано с тем, что природные газы и газоконденсатные смеси контактируют с пластовыми водами различных форм и вследствие чего содержат определенное количество паров воды.
Концентрация водяных паров в газе зависит от его состава, давления, температуры.
Объемный коэффициент пластового газа bг представляет собой отношение объема газа в пластовых условиях Vпл.г к объему того же количества газа Vст, который он занимает в стандартных условиях, можно найти с помощью уравнения Клайперона — Менделеева:
bг = Vпл.г/Vст = Z(Pcт×Тпл/(Рпл×Тст),
где Рпл, Тпл, Pcт,××Тст — давление и температура соответственно в пластовых и стандартных условиях.
Значение величины bг имеет большое значение, так как объем газа в пластовых условиях на два порядка (примерно в 100 раз) меньше, чем в стандартных условиях.
Источник: Эксплуатация магистральных газопроводов: Учебное пособие. (Под ред. Ю.Д. Земенкова) Изд-во «Вектор Бук» Тюмень, 2002
Источник
Нефтяные газы и их свойства
Природные углеводородные газы находятся в недрах земли или в виде самостоятельных залежей, образуя чисто газовые месторождения, либо в растворенном виде содержится в нефтяных залежах. Такие газы называются нефтяными или попутными, так как их добывают попутно с нефтью.
Природные нефтяные газы – смеси предельных углеводородов, главной составляющей которой является метан. В виде примесей в природном газе присутствуют азот, углекислый газ, сероводород, меркаптаны, гелий, аргон и пары ртути.
Физические свойства природного газа зависят от его состава, но в целом они близки к свойствам метана, как основного компонента смеси.
Попутные газы месторождений Муравленковского региона содержат от 59,7 % до 84 % метана.
Молекулярная масса газа: 16-20 кг/кмоль.
Плотность газа: 0,73 – 1 т/м 3 .
При расчетах пользуются относительной плотностью -плотность газа, взятая по отношению к плотности воздуха.Относительная плотность нефтяных газов колеблется от 0.554 для метана до 2.49 для пентана и выше. Чем больше в нефтяном газе легких углеводородов — метана СН4 и этана С2Н6 (относительная плотность — 1.038), тем легче этот газ. При нормальных условиях метан и этан находятся в газообразном состоянии. Следующими за ними по относительной плотности являются пропан С3Н8 (1.522) и бутан С4Н0 (2.006), которые также относятся к газам, но легко переходят в жидкость даже при небольших давлениях.
Относительная плотность попутных газов Муравленковского региона варьируется от 0,763 до 1,029.
Вязкость нефтяного газа при давлении 0,1 МПа и температуре 0 0 С обычно не превышает 0,01 МПа·с. С повышением давления и температуры она незначительно увеличивается. Однако при давлениях выше 3 МПа увеличение температуры вызывает понижение вязкости газа, причем газы, содержащие более тяжелые углеводороды, как правило, имеют большую вязкость.
Теплоемкость газа. Теплоемкостью называется количество тепла, необходимое для нагревания единицы веса или объема этого вещества на 1 0 С. Весовая теплоемкость газа измеряется в кДж/кг∙град, а объемная в кДж/м 3 ∙град.
Теплота сгорания газа. Теплота сгорания какого-либо вещества определяется количеством тепла, выделяющимся при сжигании единицы веса или единицы объема данного вещества. Теплота сгорания газов выражается в кДж/кг и кДж/м 3 и является основным показателем, характеризующим газ или топливо. Если при постоянной температуре повышать давление какого-либо газа, то после достижения определенного значения давления этот газ сконденсируется, т.е. перейдет в жидкость. Для каждого газа существует определенная предельная температура, выше которой ни при каком давлении газ нельзя перевести в жидкое состояние.
Наибольшая температура, при которой газ не переходит в жидкое состояние, как бы велико ни было давление, называется критической температурой.
Природный газ — смесь газов. Компонентами природного газа являются углеводороды парафинового ряда: метан, этан, пропан, изобутан, а также неуглеводородные газы: сероводород, углекислый газ, азот. При эксплуатации газовых и газоконденсатных месторождений в скважинах, газосборных сетях, магистральном газопроводе при определенных термодинамических условиях образуется кристаллогидраты. По внешнему виду они похожи на сажеобразную массу или лед. Гидраты образуются при наличии капельной влаги и определенных давлениях и температурах. В зависимости от преобладания в нефтяных газах легких (метан, этан) или тяжелых (пропан и выше) углеводородов газы разделяются на:
Сухие -природный газ, который не содержит тяжелых углеводородов или содержит их в незначительных количествах.
Жирные — газ, содержащий тяжелые углеводороды в таких количествах, когда из него целесообразно получать сжиженные газы или газовые бензины.
На практике принято считать жирным газом такой, в 1 м 3 которого содержится более 60 гр газового бензина. При меньшем содержании газового бензина газ называют сухим. С тяжелыми нефтями добывают преимущественно сухой газ, состоящий главным образом из метана. В нефтяных газах, кроме углеводородов, содержатся в незначительных количествах углекислый газ, сероводород и др. Важной характеристикой природного газа является растворимость его в нефти.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник
2 Состав и физико-химические свойства природных газов и нефти
2.1 Состав и физико-химические свойства природных газов
Природные газы – это вещества, которые при нормальных (стандартных) условиях находятся в газообразном состоянии и в зависимости от условий могут находиться в трёх состояниях: свободном, сорбированном, растворённом.
Углеводородные газы в пластовых условиях (в залежах) в зависимости от их состава, давления и температуры могут находиться в различных агрегатных состояниях – газообразном, жидком, в виде газожидкостных смесей.
Свободный газ обычно расположен в повышенной части пласта, в газовой шапке. Если газовая шапка в нефтяной залежи отсутствует, то весь газ залежи растворён в нефти. Это возможно при высоком пластовом давлении или особом строении залежи. Этот газ, по мере снижения давления при добыче, выделяется из нефти. Он называется попутным газом.
В пластовых условиях все нефти содержат растворённый газ. Чем выше давление в пласте, тем больше растворённого газа содержится в нефти. Давление, при котором весь имеющийся в залежи газ растворён в нефти, называется пластовым давлением насыщения. Давление насыщения нефти газом в пластовых условиях определяется составом нефти, газа и температурой в пласте.
2.1.1 Состав природных газов
Природные газы, добываемые из газовых, газоконденсатных и нефтяных месторождений, состоят из углеводородов (СН4-С4Н10, и выше), а также неуглеводородных компонентов (H2S, N2, CO, CO2, Ar, H2, He и др.).
Составы сухого газа, жидких газов и газового бензина
Компоненты Название смеси
Метан, этилен, этан Сухой газ
Пропан, пропилен, изобутан, нормальный бутан, бутилен Жидкий газ
Изопентан, нормальный пентан, амилены, гексан и др. Бензин
Природные газы, добываемые из чисто газовых, нефтяных и газоконденсатных месторождений, состоят из углеводородов гомологического ряда метана с общей формулой СnH2n+2, а также неуглеводородных компонентов: азота (N2), углекислого газа (СО2), сероводорода (H2S), меркаптанов (RSH), редкоземельных (инертных) газов (гелия, аргона, криптона, ксенона), ртути. Число углеродных атомов в молекуле углеводородов п может достигать 18 и более.
Метан (СН4), этан (С2Н6) и этилен (С2Н4) при обычных условиях давления (P = 0,1 МПа) и температуры (T=288—303 К) являются газами.
Пропан (С3Н8), пропилен (С3Н6), изобутан (i-C4Hio), нормальный бутан (n = C4H10), бутилены (С4Н8) при атмосферных условиях находятся в парообразном (газообразном) состоянии, при повышенных давлениях — в жидком состоянии. Они входят в состав жидких углеводородных газов.
Углеводороды, начиная с изопентана (i-C5Hi2) и более тяжелые (17>n>5), при атмосферных условиях находятся в жидком состоянии. Они входят в состав бензиновой фракции.
Углеводороды, в молекулу которых входит 18 атомов углерода (от C18H38) и более расположенных в одну цепочку, при атмосферных условиях находятся в твердом состоянии.
В таблице 2.1 приведены составы сухого газа, жидких газов и газового бензина.
Природные газы подразделяются на три следующие группы:
– газы, добываемые из чисто газовых месторождений и представляющие собой сухой газ, свободный от тяжелых углеводородов.
– газы, добываемые вместе с нефтью. Это физические смеси сухого газа, пропан-бутановой фракции (жидкого газа) и газового бензина.
– газы, добываемые из газоконденсатных месторождений,— смесь сухого газа и жидкого углеводородного конденсата. Углеводородный конденсат состоит из большого числа тяжелых углеводородов, из которых можно выделить бензиновые, лигроиновые, керосиновые, а иногда и более тяжелые масляные фракции.
Качественный состав газов нефтяного происхождения всегда одинаков, что нельзя сказать о газах вулканических извержений.
При нормальных и стандартных условиях в газообразном состоянии существуют только углеводороды С1–С4. Углеводороды С5 и выше при нормальных условиях находятся в жидком состоянии. При высоких давлениях жидкие углеводороды растворяются в газовой фазе (газовые растворы, газоконденсаты). Поэтому при высоких давлениях плотность газа может приближаться к плотности легких углеводородных жидкостей.
Газы, добываемые из чисто газовых месторождений, содержат более 95 % метана (табл. 2.1) и представляют собой группу сухих газов.
Таблица 2.1 – Химический состав газа газовых месторождений, об. %
Источник