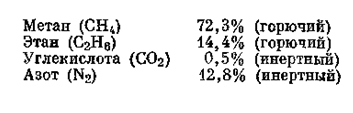Состав природного газа
Основным углеводородным компонентом природного газа является метан (СН4), представляющий собой наиболее устойчивое из всех нефтяных углеводородов соединение. В различных, но всегда небольших количествах в природном газе часто присутствуют также другие парафиновые углеводороды, такие, как этан (С2Н6), пропан (С3Н8), бутан (С4Н10), пентан (С5Н12) и гексан (С6Н14), а в некоторых случаях даже гептан (С7Н16), октан (С8Н18) и нонан (С9Н20). Свободный водород в природном газе встречается очень редко, за исключением некоторых областей развития вулканизма и соляных копей в Германии, геохимики СССР установили более широкое распространение водорода в природных газах. Иногда в очень незначительном количестве в природном газе содержатся окись углерода и непредельные углеводороды.
Фото: «Врата Ада» в центре пустыни Каракум, выход природного газа
Свойства природного газа
При температурах и давлениях, свойственных нефтяным природным резервуарам, метан не переходит в жидкое состояние и поэтому всегда представлен в виде газа; при более высоких давлениях он может растворяться в жидких УВ. Критические температуры других входящих в состав природного газа углеводородов таковы, что последние в обычных условиях нефтяных и газовых природных резервуаров могут существовать как в жидкой, так и в газообразной фазе. Общее содержание углерода в типичном природном газе составляет около 35 фунт/тыс. куб. фут. Около ⅓ этого количества может быть извлечено в виде газовой сажи, состоящей из чрезвычайно мелких частиц, углерода диаметром от 10 до 150 мк, которая образуется при сгорании газа в условиях ограниченного доступа воздуха. Многие крупные месторождения газа можно узнать по видимым еще издалека огромным тучам черного дыма, поднимающегося над сажевыми заводами. Плотность природного газа колеблется от величины плотности метана, равной 0,554 (относительно воздуха) до величины плотности некоторых жирных газов, превышающей плотность воздуха. В большинстве случаев плотность природного газа колеблется в пределах 0,65-0,90 (плотность воздуха = 1,0). Анализы газа из некоторых крупных газовых залежей сведены в табл. 1.
Классификация природного газа
Природный газ при выходе из скважины классифицируется в полевых условиях как сухой, тощий или жирный в зависимости от количества содержащихся в нем газолиновых паров. Сухой газ содержит их менее 0,1 галлона на1000 куб. футов, а жирный ‑0,3 галлонаи более на 1000 куб. футов. Остаточным газом называется природный газ, из которого удалены газолиновые пары. Газ, извлекаемый на поверхность из нефтяной скважины, называется попутным газом. Для отличия газов с относительно низким или высоким содержанием сероводорода используются соответственно термины «пресный газ» и «кислый газ». Природный газ промышленного назначения, перекачиваемый по трубопроводам, характеризуется теплотворной способностью, изменяющейся в пределах от 900 до 1200 британских тепловых единиц, и в основном имеет следующий состав:
Таблица 1. Средний состав различных товарных природных газов
Источник
Алканы
Мы приступаем к новому разделу — органической химии. Совершенно необязательно (и даже преступно по отношению к собственному времени!) знать наизусть, зубрить свойства органических веществ.
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций 😉
- Атомы в молекуле соединены в определенной последовательности, в соответствии с их валентностью. Порядок связи атомов отражает химическое строение.
- Зная свойства веществ, можно установить их химическое строение, и наоборот, зная строение вещества можно сделать вывод о его свойствах.
- Атомы или группы атомов оказывают взаимное влияние друг на друга непосредственно или через другие атомы
- Свойства вещества зависят от количественного и качественного состава, а также от химического строения молекулы
Алканы (парафины) — насыщенные углеводороды, имеющие линейное или разветвленное строение, содержащие только простые связи. Относятся к алифатическим углеводородам, так как не содержат ароматических связей.
Алканы являются насыщенными соединениями — содержат максимально возможное число атомов водорода. Общая формула их гомологического ряда — CnH2n+2.
Номенклатура алканов
Номенклатура (от лат. nomen — имя + calare — созывать) — совокупность названий индивидуальных химических веществ, а также правила составления этих названий. Названия у алканов формируются путем добавления суффикса «ан»: метан, этан, пропан, бутан и т.д.
Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Перечисленные выше алканы, являются по отношению друг к другу гомологами, то есть составляют один гомологический ряд (греч. homólogos — соответственный).
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить читателя с ними. Итак, алгоритм составления названий следующий:
- В структурной формуле вещества необходимо выбрать самую длинную (пусть и изогнутую на рисунке!) цепь атомов углерода
- Атомы выбранной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
- В начале название перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле имеется несколько одинаковых радикалов, то цифрой указывают нахождение каждого из них в главной цепи и перед их названием соответственно ставят частицы ди-, три-, тетра- и т.д.
- Основой названия служит наименование предельного углеводорода с тем же количеством атомов углерода, что и в главной цепи
Внимательно изучите составленные для различных веществ названия ниже.
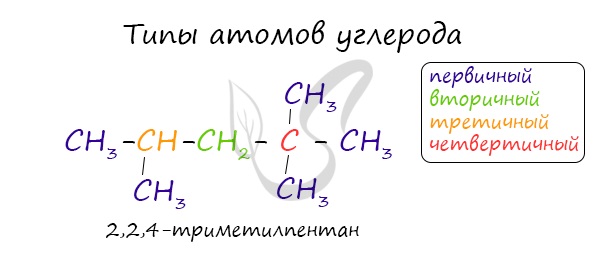
В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.
Изомерами (греч. isomeros — составленный из равных частей) называют вещества, имеющие одну молекулярную формулу, но отличающиеся по строению (структурная изомерия) или расположению атомов в пространстве (пространственная изомерия).
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной (геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.
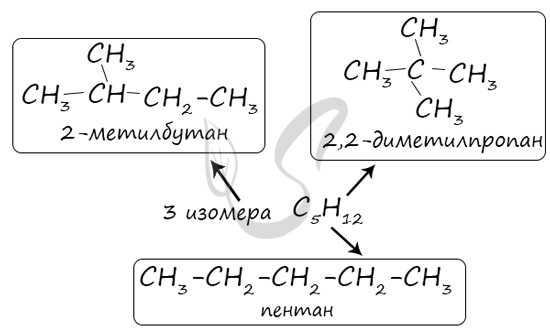
В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана C5H12 существует 3 структурных изомера.
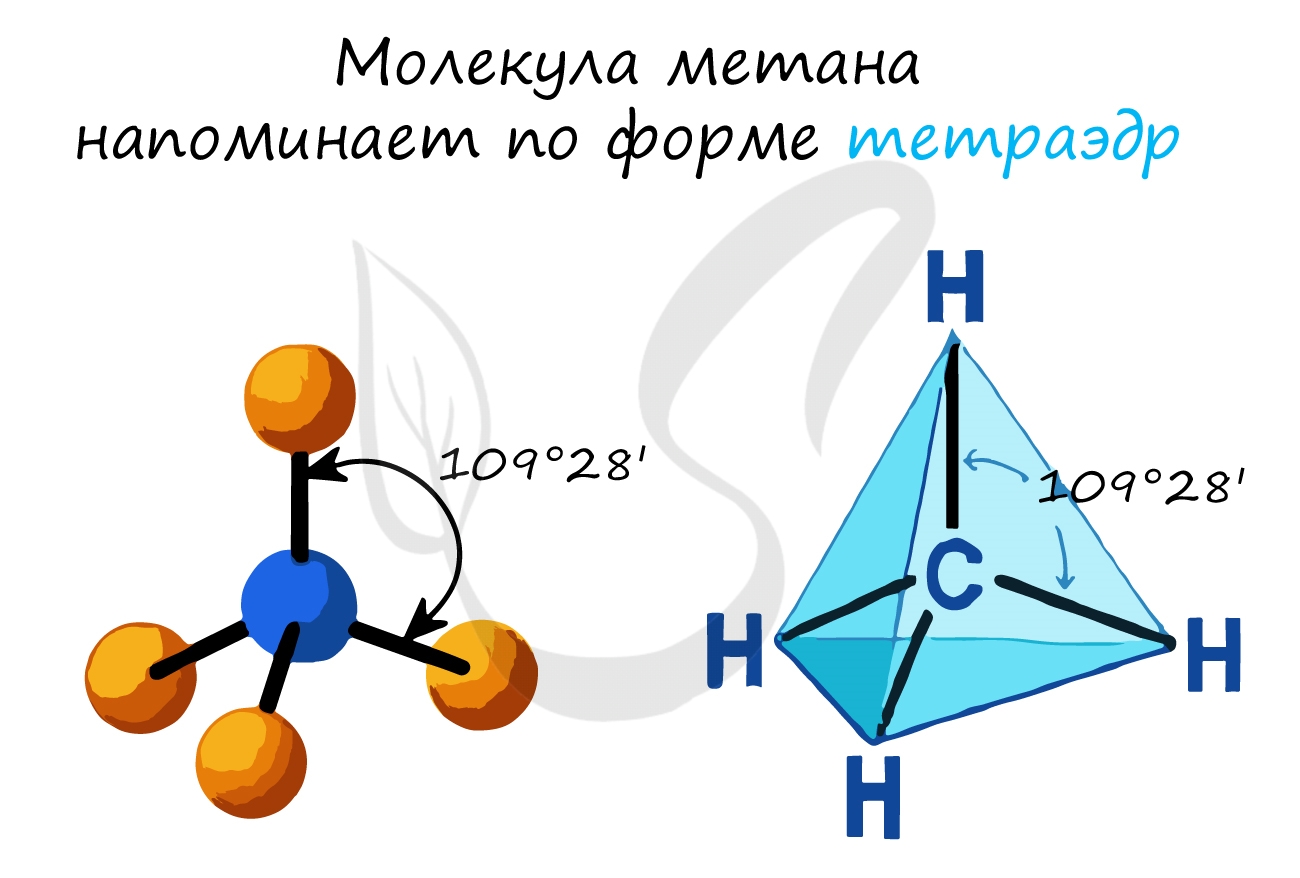
- В молекулах алканов присутствуют одиночные сигма-связи (σ-связи), длина которых составляет 0,154 нм
- Тип гибридизации атомов углерода — sp 3
- Валентный угол (между химическими связями) составляет 109°28′
Природный газ и нефть
Алканы входят в состав природного газа: метан 80-97%, этан 0.5-4%, пропан 0.2-1.5% , бутан 0.1-1%, пентан 0-1%. Состав нефти нельзя выразить одной формулой, он непостоянен и зависит от месторождения.
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем крекинга из нефти получают алканы.
Получение алканов
В ходе крекинга нефти получается один алкан и один алкен.
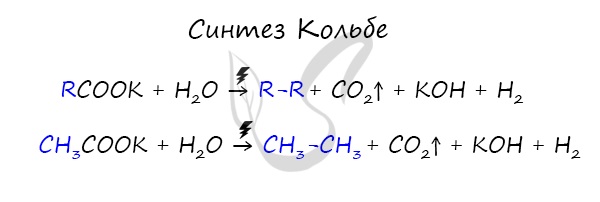
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.
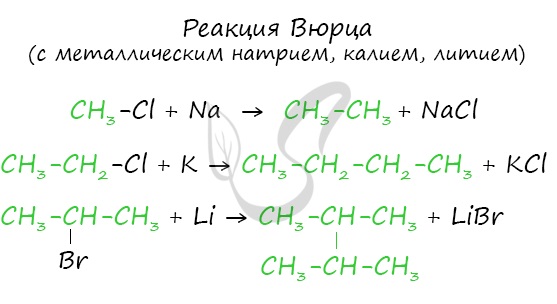
Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
В ходе синтеза Гриньяра с помощью реактива Гриньяра (алкилмагнийгалогенида) получают различные органические соединения, в том числе несимметричные (в отличие от реакции Вюрца).
На схеме выше мы сначала получили реактив Гриньяра, а потом использовали его для синтеза. Однако можно записать получение реактива Гриньяра и сам синтез в одну реакцию, как показано на примерах ниже.
В результате электролиза солей карбоновых кислот может происходить образование алканов.
В результате разложения карбида алюминия образуется метан и гидроксид алюминия.
Химические свойства алканов
Атом галогена замещает атом водорода в молекуле алкана. Запомните, что легче всего идет замещение у третичного атома углерода, чуть труднее — у вторичного и значительно труднее — у первичного.
Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы, которые и осуществляют атаку на молекулу углеводорода.
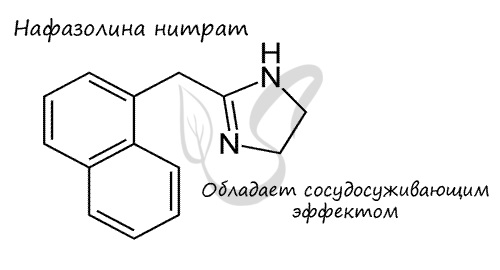
Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция идет при повышенном давлении, по свободнорадикальному механизму.
Для удобства и более глубокого понимания, азотную кислоту — HNO3 — можно представить как HO-NO2.
Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
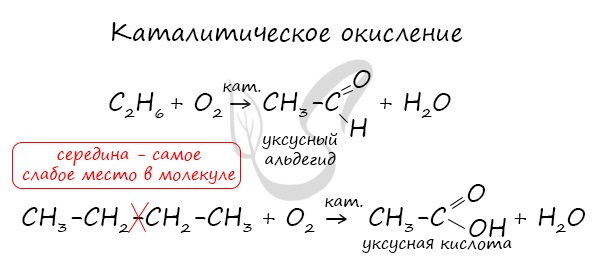
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
Пиролиз (греч. πῦρ — огонь + λύσις — разложение) — термическое разложение неорганических и органических соединений. Принципиальное отличие пиролиза от горения — в отсутствии кислорода.
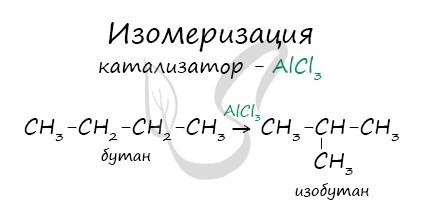
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.
Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их химическое свойство.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник