«Птичье лицо»: что будет, если вовремя не исправить прикус ребёнку
Стоматолог: из-за неправильного прикуса ребёнок вырастает с «птичьим лицом». У человека с таким дефектом недоразвита нижняя челюсть, поэтому визуально подбородок у него скошен и западает назад. Врач Алексей Сошников посоветовал в первый раз показать ребёнка ортодонту в возрасте 2,5–3 лет. Также это можно сделать в 6 и в 11 лет, когда легко исправить даже самые тяжёлые патологии.
Когда показать ребёнка ортодонту
Стоматолог-терапевт Алексей Сошников объяснил, что в возрасте от 2,5 до 3 лет у ребёнка формируется молочный прикус. Если он в итоге окажется неправильным, то потом дефекты могут перенестись на постоянные зубы. Поэтому до 3 лет малыша надо уже хотя бы раз показать ортодонту.
Если вы этого не сделали, то обязательно приводите ребёнка к специалисту в 6 лет. В этом возрасте можно исправить даже мезиальный и открытый прикусы, сказал врач «Газете.Ru». Но даже 11 и 12 лет — ещё не поздно.
«11–12 лет — это пик возраста, когда можно сделать практически невозможное, например, расширить зубные ряды, исправить асимметрию, повлиять на профиль и лицевые признаки в лучшую сторону», — добавил стоматолог в беседе с «Газетой.Ru». А ещё это самый лучший возраст для установки брекетов на постоянные зубы.
Что будет, если не исправить прикус
Всё зависит от тяжести патологии. По словам Сошникова, нарушение прикуса у детей в большинстве случаев отражается на лице.
«То есть всегда есть вероятность изменения формы лица, появления асимметрии, чрезмерно выпуклого или вогнутого профиля — это так называемое птичье лицо », — пояснил врач.
Но проблема не только в эстетических дефектах. При неправильном прикусе человек не может нормально откусывать и пережёвывать еду. Потенциально это грозит заболеваниями желудочно-кишечного тракта (ЖКТ). Кроме того, у ребёнка может развиться патология височно-нижнечелюстного сустава, то есть появятся щелчки, хруст и боли, в области челюсти.
«Если не устранять у ребёнка патологии прикуса — например, не расширять зубные ряды, не исправлять зубы, — то у него останутся узкие носовые ходы, нарушится дыхание », — предупредил врач.
Неправильный прикус ребёнку можно исправить с помощью несложной пластики. Операцию обычно делают в 5–6 лет, когда молочные зубы меняются на постоянные. Подробнее об этой процедуре мы рассказывали здесь.
Источник
Синдром Ниймеген
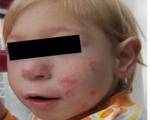
Синдром Ниймеген — это крайне редкое моногенное заболевание с аутосомно-рецессивным типом наследования, которое характеризуется первичным иммунодефицитом, множественными аномалиями. Патология связана с мутацией гена NBN. Основные признаки синдрома Ниймеген: деформация лицевого скелета в виде «птичьего» лица, частые рецидивирующие бактериальные инфекции, микроцефалия, отставание детей в физическом развитии. Диагностика включает иммунологические и генетические исследования. Основу лечения синдрома составляет пожизненная заместительная терапия иммуноглобулинами, также рассматривается вариант инфузии гемопоэтических стволовых клеток.
МКБ-10
Общие сведения
Синдром назван в честь голландского города Ниймеген, где в 1981 г. была впервые описана клиническая картина заболевания. Генные нарушения, лежащие в основе болезни, картированы в 1998 г. В медицинской литературе описано около 150 случаев синдрома. Однако, согласно данным из национальных регистров (чешского, польского), его истинная распространенность намного выше. В основном синдром Ниймеген встречается на территории Восточной Европы, что обусловлено частым носительством мутации среди здорового славянского населения («эффект основателя»). У неславян распространенность патологии составляет 1:3-5 млн. жителей.
Причины
Патология возникает при дефекте гена NBN (NBS1 — Nijmegen breakage syndrome 1), расположенного на длинном плече 8-й хромосомы. Он кодирует образование белка нибрина, участвующего в работе трехмерного протеинового комплекса MRN, в который, кроме нибрина, входят белки MRE11 и RAD50.
Синдром Ниймеген имеет аутосомно-рецессивный характер наследования: при наличии специфического генного дефекта у обоих родителей риск рождения больного ребенка составляет 25%. В парах, где носителем мутировавшего гена является только отец или мать, больные дети не рождаются, однако у половины потомства в кариотипе есть дефектный ген.
Патогенез
Комплекс MRE11/RAD50/NBN, функционирование которого нарушается у детей, страдающих болезнью Ниймеген, отвечает за репарацию ДНК. Белки регулируют восстановление нормальной двуцепочечной структуры генетического материала после повреждения ионизирующим излучением, процессов мейоза и V(D)G-рекомбинации, которые происходят на раннем этапе образования иммунных клеток.
До 90% больных детей славянского происхождения являются гомозиготными по гипоморфной мутации 657del5, то есть у них происходит делеция 5 пар оснований в шестом экзоне гена NBN. При этом синтезируются два аномальных усеченных протеина — р26-нибрин, р70-нибрин, которые не в состоянии обеспечить нормальное функционирование белка.
У больных из неславянских стран (Великобритании, Германии, Голландии, Италии, Канады, Мексики) выявлено еще 11 вариантов повреждения, локализованных не только в 6 экзоне, но и в других участках мутировавшего гена. Учеными доказана обратная связь между показателями экспрессии белка р70 и развитием онкогематологических заболеваний в рамках синдрома Ниймеген.
Симптомы
При болезни Ниймеген с рождения отмечаются характерные особенности внешности по типу «птичьего» лица. У детей узкое лицо с высоким лбом, крупный нос, маленькая нижняя челюсть. Также с момента рождения заметны признаки микроцефалии (уменьшенные размеры черепной коробки), часто выявляются расщелины неба, деформации ушных раковин, монголоидный разрез глаз в сочетании с гипертелоризмом.
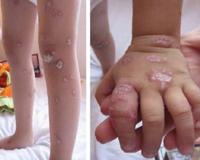
Пороки развития скелета включают клинодактилию, частичную синдактилию, полидактилию, дисплазию тазобедренных суставов. У 50-70% детей определяются дерматологические проявления синдрома: пятна цвета «кофе с молоком», участки витилиго, прогрессирующая депигментация по всему телу.
Патогномоничная особенность синдрома — врожденный дефицит клеточного (Т-лимфоциты) и гуморального (антитела) звеньев иммунитета. Из-за этого с первых месяцев жизни у детей возникают рецидивирующие инфекции дыхательных путей (бронхиты, пневмонии, синуситы), воспалительные болезни уха (отит, мастоидит), бактериальные поражения органов ЖКТ и мочеполовой системы. Реже встречаются вирусные инфекции (цитомегаловирус, вирус Эпштейн-Барр).
Типичны аномалии мочеполовых органов, которые включают гипоплазию/аплазию почек, эктопические почки, уретро-анальную фистулу, у мальчиков зачастую диагностируется крипторхизм, гипоспадия. В мозговой ткани присутствуют арахноидальные кисты, возможно частичное или полное отсутствие мозолистого тела. У детей замедляется физическое развитие, уровень интеллекта в пределах нормы или умеренно снижен.
Осложнения
Наиболее прогностически неблагоприятным последствием синдрома Ниймеген являются злокачественные опухоли, которые диагностируются у 40% детей. Чаще всего поражается лимфоидная ткань: появляются Т- и В-клеточные неходжкинские лимфомы, лимфома Ходжкина, острые лимфобластные лейкозы. Среди солидных неоплазий встречаются медуллобластома, рабдомиосаркома, саркома Юинга. Онкопатология является главной причиной смерти пациентов молодого возраста (до 20 лет).
Особую опасность синдрома Ниймеген представляют рецидивирующие инфекции, которые на фоне иммунодефицита обычно быстро переходят в генерализованные формы. Летальный исход может наступать от септических осложнений. У некоторых детей вследствие затяжных инфекций развивается амилоидоз, вызывающий хроническую почечную недостаточность и заканчивающийся смертью.
Диагностика
О наличии синдрома Ниймеген могут свидетельствовать специфические фенотипические особенности (уменьшенный череп, «птичье» лицо), которые сочетаются с признаками иммунодефицита. Обследованием детей занимается педиатр, для комплексной диагностики привлекают иммунолога-аллерголога, генетика, ортопеда-травматолога. Для подтверждения синдрома назначаются следующие диагностические мероприятия:
- Иммунологические анализы. В расширенной иммунограмме у детей выражены лейко- и лимфопения со снижением абсолютного числа CD3, CD4, изменением соотношения CD4/CD8. Абсолютное количество В-клеток снижено у 72% больных, также наблюдается дефицит IgG, IgA, IgM.
- Генетическое тестирование. Для верификации синдрома обязательно выполняется молекулярно-генетическое исследование, с помощью которого определяются мутации в экзонах 6-10 гена NBN.
- Инструментальная визуализация. С учетом повышенной чувствительности детей с синдромом Ниймеген к радиации, для выявления пороков внутренних органов проводится ультразвуковая диагностика, эндоскопия, магнитно-резонансная томография.
Лечение синдрома Ниймеген
Унифицированные протоколы терапии для детей с клиникой синдрома Ниймеген отсутствуют, поскольку на современном этапе развития медицины этиотропное лечение не разработано. Основной задачей врачей является контроль иммунного статуса пациента, предупреждение осложнений, улучшения качества жизни. Для этого используется несколько направлений лечения:
- Заместительнаятерапия. Регулярное введение иммуноглобулинов G необходимо для поддержания иммунной защиты, снижения риска тяжелых инфекций у детей. Подкожные инъекции признаны эффективным, безопасным и удобным способом коррекции иммунодефицита. Маркером для начала заместительной терапии служит уровень IgG менее 2,5–3,0 г/л.
- Антибиотикотерапия. Проводится периодическими или постоянными курсами при часто рецидивирующих или хронических инфекциях дыхательных органов.
- Трансплантация гемопоэтических клеток. Это более современный вариант лечения синдрома, который успешно корректирует иммунологический дефект и может применяться в лечении онкогематологических болезней.
- Полихимиотерапия. Цитостатики рекомендованы для лечения лимфоидных и солидных опухолей. Больным назначаются уменьшенные дозы препаратов. Как правило, они комбинируются с моноклональными антителами для таргетной терапии.
Прогноз и профилактика
Синдром Ниймеген нередко заканчивается смертью пациентов в молодом возрасте от онкопатологии, септических процессов. Однако благодаря интенсивной заместительной терапии иммуноглобулинами, проведению ТГСК удается продлить жизнь больных. Профилактика появления синдрома у детей включает медико-генетическое консультирование пар с отягощенной наследственностью на этапе планирования зачатия, в процессе беременности.
1. Диагностика и лечение острого лимфобластного лейкоза у больного с синдромом Ниймеген, впервые диагностированным во взрослом возрасте/ К.И. Зарубина, Е.Н. Паровичникова, А.В. Кохно, О.А. Гаврилина// Гематология и транфузиология. — 2020. — №1.
2. Случай синдрома Ниймеген у ребенка с частыми рецидивами респираторной инфекции/ Е.А. Беседина, Д.В. Прометной, С.Г. Пискунова, О.С. Селезнева// Педиатр. — 2019. — №6.
3. Прогноз и оптимизация терапии на этапах клинической эволюции синдрома Ниймеген у детей. Диссертация на соискание ученой степени кандидата медицинских наук/ Е.В. Дерипапа. — 2018.
4. Синдром Ниймеген (клиническое наблюдение)/ М.Ю. Каган, Н.С. Шулакова, Р.А. Гумирова, Е.А. Злодеева// Педиатрическая фармакология. — 2012. — №3.
Источник