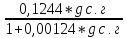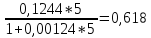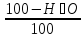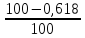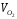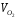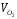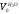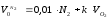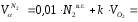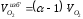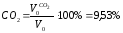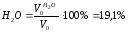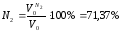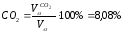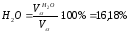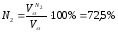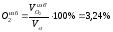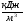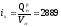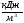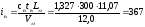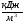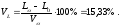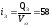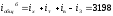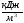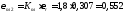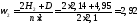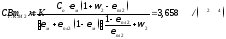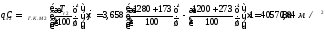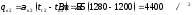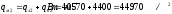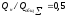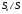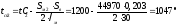Расчет горения природного газа
Природный газ Верхне-Омринского месторождения. Содержание влаги в газе W р = 1,0 об.%.
| СН4 с | С2Н6 с | С3Н8 с | С4Н10 с | С5Н12 с и высшие | СО2 с | N2 с | Сумма |
| 85,0 | 3,90 | 1,40 | 0,41 | 0,23 | 0,10 | 8,70 | 99,74 |
Коэффициент избытка воздуха при сжигании газа в горелке частичного смешивания a = 1,15. Влагосодержание атмосферного воздуха d = 10 г/кг сухого воздуха (в этом и других примерах).
Определяем состав рабочего топлива. Пользуясь формулой (3), находим содержание элементов в рабочем топливе:
СН4 вл = % = = 85,0·0,9926 = 84,37%;
СО2 вл = 0,10·0,9926 = 0,099% » 0,10%;
Результаты пересчета состава сводим в таблицу.
Состав влажного рабочего топлива, объемные %
| СН4 вл | С2Н6 вл | С3Н8 вл | С4Н10 вл | С5Н12 вл | СО2 вл | N2 вл | Н2О вл | Сумма |
| 84,37 | 3,87 | 1,39 | 0,41 | 0,23 | 0,10 | 8,64 | 1,00 | 100,00 |
Рассчитываем теплоту сгорания природного газа по формуле (8):
= 358,2·84,38 + 637,5·3,87 + 912,5·1,39 + 1186,5·0,41 + 1460,8·0,23 =
Тепловой эквивалент согласно формуле (9) составляет:
Теоретически необходимое количество сухого воздуха находим по формуле (11):
L0 = 0,0476·(2·84,37 + 3,5·3,87 + 5·1,39 + 6,5·0,41 + 8·0,23) = 9,22 нм 3 /нм 3 .
Определяем действительное количество атмосферного воздуха при a = 1,15 по формуле (12):
Lд = 1,15 · 9,22= 10,60 нм 3 / нм 3 .
Рассчитываем действительное количество атмосферного воздуха по формуле (13):
Lд¢ = (1 + 0,016 d) Lд = 1,016·10,60 = 10,77 нм 3 / нм 3 .
Количество продуктов горения газа при a = 1,15 по формулам (14) ‑ – (17):
VСО2= 0,01 (0,10 + 84,37 + 2·3,87 + 3·1,39 + 4·0,41 + 5·0,23) =
VН2О = 0,01 (2·84,37 + 3·3,87 + 4·1,39 + 5·0,41 + 6·0,23 + 0,99 +
+ 0,16·10·10,60) = 2,073 нм 3 /нм 3 ;
VN2= 0,79·10,60 + 0,01·8,64 = 8,463 нм 3 /нм 3 ;
VО2= 0,21 (1,15 – 1) 9,22 = 0,290 нм 3 /нм 3 .
Находим общий объем продуктов горения при a = 1,15 по формуле (22):
Va = 0,991 + 2,073 + 8,464 + 0,290 = 11,818 » 11,82 нм 3 / нм 3 .
Процентный состав продуктов горения:
Составляем материальный баланс процесса горения на 100 нм 3 природного газа при a = 1,15.
Материальный баланс процесса горения природного газа
| Приход | кг | Расход | кг |
| Природный газ | 60,49 | Продукты горения | |
| СН4 = 84,37·0,717 | 5,25 | СО2 = 0,991·1,977 | 196,02 |
| С2Н6 = 3,87·1,356 | 2,81 | Н2О = 2,073·0,804 | 166,65 |
| С3Н8 = 1,39·2,020 | 1,16 | N2 = 8,463·1,251 | 1058,74 |
| С4Н10 = 0,41·2,840 | 0,73 | О2 = 0,290·1,429 | 41,50 |
| С5Н12 = 0,23·3,218 | 0,20 | ||
| N2 = 8,64·1,251 | 10,80 | Невязка | -0,89 |
| Н2О = 0,99·0,804 | 0,80 | ||
| Воздух | |||
| О2 = 10,60·0,21·100·1,429 | 318,20 | ||
| N2 = 10,60·0,79·100·1,251 | 1047,94 | ||
| Н2О = 10,60·0,0016·10·100·0,804 | 13,64 | ||
| Итого | 1462,02 | Итого | 1462,02 |
Невязка баланса составляет: = 0,061%.
Определяем теоретическую температуру горения природного газа. Для этого находим общее теплосодержание продуктов горения по формуле (23), пренебрегая теплосодержанием природного газа и воздуха и теплотой диссоциации:
i общ = = 2942 кДж/нм 3 .
По i–t-диаграмме (рис. 2) находим теоретическую температуру горения при коэффициенте a = 1,15: tтеор = 1780°С.
Находим расчетное теплосодержание продуктов горения с учетом пирометрического коэффициента, который примем равным h = 0,78:
i¢общ = i общ . h = 2942 · 0,78 = 2295 кДж/нм 3 .
По i–t-диаграмме (рис. 2) находим действительную температуру горения природного газа tдейств = 1450°С.
Допустим, требуется создать в печи температуру 1680ºС.
Для этого необходимо повысить теплосодержание ПГТ. Определяем по i–t-диаграмме, что при 1680ºС i¢общ = 2724 кДж/нм 3 .
Снизить коэффициент избытка воздуха α ,чтобы уменьшился общий объем ПГТ Va и таким образом повысилось их теплосодержание i общ, нельзя, так как a = 1,15 близко к минимально допустимому значению и в результате снижения a ухудшится смешивание потоков топлива и воздуха.
Общее теплосодержание продуктов горения топлива i общ может быть повышено за счет теплоты подогретого воздуха i возд, идущего на горение. Определим температуру подогрева. Вклад в теплосодержание ПГТ от нагретого воздуха:
Δi общ = = = 550 кДж/нм 3 .
Приравниваем добавочную теплоту величине теплосодержания воздуха. При сжигании газа доля вторичного воздуха может достигать 100%, т.е. в формуле (23) k = 1,00.
Δi общ = i возд = , т.е.
i возд = = 550 = 613 кДж/нм 3 .
По i–t-диаграмме (рис. 1) определяем, что воздух обладает теплосодержанием i возд = 613 кДж/нм 3 при подогреве до tвозд = 420ºС.
Источник
Расчет горения природного газа проектный
Температура подогрева воздуха, tв = 20 °C.
1.1.2. Пересчитываем состав сухого газа на влажный рабочий газ при содержании H2O = 1%:
При точности анализа – один знак после запятой, другие составляющие газа остаются без изменений, т.е. состав рабочего газа будет:
| CH4 | C2H6 | C3H8 | C4H10 | C5H12 | CO2 | N2 | H2O | Сумма |
| 97,0% | 0,5% | 0,3% | 0,1% | 0,2% | 0,1% | 0,8% | 1,0% | 100,0% |
1.1.3.Теплота сгорания газа:
Q p н = 385,18 ⋅ 97,0 + 637,48 ⋅ 0,5 + 912,3 ⋅ 0,3 + 1186,46 ⋅ 0,1 + 1460,77 ⋅ 0,2 = 35746,69 , кДж/нм 3
Q p н = 85,55 ⋅ 97,0 + 152,26 ⋅ 0,5 + 217,9 ⋅ 0,3 + 283,38 ⋅ 0,1 + 348,9 ⋅ 0,2 = 8538 , ккал/нм 3 .
1.1.4.Теоретически необходимое количество сухого воздуха:
V о в = 4,762 (2 ⋅ 97 + 3,5 ⋅ 0,5+ 5 ⋅ 0,3+ 6,5 ⋅ 0,1+ 8 ⋅ 0,2)/100 = 4,762 ⋅ 199,5/100 = 9,5 нм 3 /нм 3 .
1.1.5.Теоретически необходимое количество воздуха с учетом его влажности:
V о в .вл = (1+0,0016d) ⋅ V о в , нм 3 /нм 3
V о в .вл = (1+0,0016 ⋅ 10) ⋅ 9,5 = 9,65 нм 3 /нм 3 ,
где: 0,0016 = 1,293/(0,804 ⋅ 1000) представляет собой коэффициент пересчета весовых единиц влаги воздуха, выраженных в г/кг сухого воздуха, в объемные единицы – нм 3 водяных паров, содержащихся в 1 нм 3 сухого воздуха.
1.1.6. Действительное количество сухого воздуха при коэффициенте избытка воздуха α=1,2:
Vα = α ⋅ V о в = 1,2 ⋅ 9,5 = 11,4 нм 3 /нм 3
1.1.7.Действительное количество атмосферного воздуха при коэффициенте избытка α=1,2:
V ′α = α ⋅ V о в .вл = 1,2 ⋅ 9,65 = 11,58 нм 3 /нм 3
1.1.8.Количество продуктов горения при α=1,2:
VCO 2 = 0,01(0,1 + 97 + 2 ⋅ 0,5 + 3 ⋅ 0,3 + 4 ⋅ 0,1 + 5 ⋅ 0,2) = 1,004 нм 3 /нм 3
VH2 O = 0,01(2 ⋅ 97 + 3 ⋅ 0,5 + 4 ⋅ 0,3 + 5 ⋅ 0,1 + 6 ⋅ 0,2 + 1,0 + 0,16 ⋅ 10 ⋅ 11,4) = 2,176 нм 3 /нм 3
VN 2 = 0,01 ⋅ 0,8 + 0,79 ⋅ 11,4 = 9,014 нм 3 /нм 3
VO 2 = 0,21(α — 1)V о в , нм 3 /нм 3
VO 2 = 0,21 ⋅ (1,2 — 1) ⋅ 9,5 = 0,399 нм 3 /нм 3
Общее количество продуктов горения:
VДГ = 1,004 + 2,176 + 9,014 + 0,399 = 12,593 нм 3 /нм 3
1.1.9. Процентный состав продуктов горения:
СО2 = 1,004 ⋅ 100/12,593 ≅ 7,973%
H2O = 2,176 ⋅ 100/12,593 ≅ 17,279%
N2 = 9,014 ⋅ 100/12,593 ≅ 71,579%
Итого: 99,999% или с точностью до двух знаков после запятой – 100%.
1.1.10.Материальный баланс процесса горения на 100 нм 3 газа (перевод нм 3 каждого газа в кг производят путем умножения на его плотность ño, кг/нм 3 ).
| Приход | кг | % | Расход | кг | % |
| Природный газ: | Продукты горения: | ||||
| CH4=97,0 ⋅ 0,717 | 69,55 | 4,466 | CO2=1,004 ⋅ 100 ⋅ 1,977 | 198,49 | 12,75 |
| C2H6=0,5 ⋅ 1,356 | 0,68 | 0,044 | H2O=2,176 ⋅ 100 ⋅ 0,804 | 174,95 | 11,23 |
| C3H8=0,3 ⋅ 2,020 | 0,61 | 0,049 | N2=9,014 ⋅ 100 ⋅ 1,251 | 1127,65 | 72,42 |
| C4H10=0,1 ⋅ 2,840 | 0,28 | 0,018 | O2=0,399 ⋅ 100 ⋅ 1,429 | 57,02 | 3,66 |
| C5H12=0,2 ⋅ 3,218 | 0,644 | 0,041 | Неувязка | -0,91 | -0,06 |
| CO2=0,1 ⋅ 1,977 | 0,20 | 0,013 | Итого: | 1551,2 | 100,00 |
| N2=0,8 ⋅ 1,251 | 1,00 | 0,064 | |||
| H2O=1,0 ⋅ 0,804 | 0,80 | 0,051 | |||
| Воздух: | |||||
| O2=199,5 ⋅ 1,2 ⋅ 1,429 | 342,1 | 21,964 | |||
| N2=199,5 ⋅ 1,2 ⋅ 3,762 ⋅ 1,251 | 1126,68 | 72,415 | |||
| H2O=0,16 ⋅ 10 ⋅ 11,4 ⋅ 0,804 | 14,66 | 0,941 | |||
| Итого: | 1557,2 | 100,0 | |||
1.1.11.Общая энтальпия продуктов горения при tв=20 °C и áв=1,2:
iобщ = 35746,69/12,593 + 11,58 ⋅ 26,38/12,593 = 2862,9 кДж/нм 3 или
iобщ = 8538/12,593 + 11,58 ⋅ 6,3/12,593 = 683,8 ккал/нм 3 ,
где: i ′в = св ⋅ tв = 1,319 ⋅ 20 = 26,38 кДж/нм 3 или
i ′в = св ⋅ tв = 0,315 ⋅ 20 = 6,3 ккал/нм 3
i ′в может быть определена также по i-t диаграмме рис. 7.1.
1.1.12.Теоретическая температура горения при α=1,2
tтеор=1775 °С, по i-t диаграмме рис. 7.2.
1.1.13.Коэффициент сохранения тепла в топке:
ϕ = 1 – q5 /100= 1 – 0,5/100 = 0,995
где: q5 – потери тепла в окружающую среду, зависят от конструктивных особенностей топки, в примере q5 принимаем равными 0,5%.
1.1.14.Действительная энтальпия газов в топке:
i ′ общ = 2862,9 ⋅ 0,995 =2848,6 кДж/нм 3 или
i ′ общ =683,8 ⋅ 0,995 = 680,4 ккал/нм 3
1.1.15.Действительная средняя температура газов в топке:
tдейст ≈ 1750 °С, по i-t диаграмме рис. 7.2.
Источник
1. Расчет горения топлива
Сжигается природный газ, элементарный состав которого на сухую массу, %:
Влагосодержание сухого газа составляет g с.г. =5 г ∕ м 3 .
Температура подогрева воздуха tв=300 ° С.
Коэффициент избытка воздуха α=1,2.
Влажность воздуха q св =14.
Механический недожог отсутствует.
1.2 Пересчет состава газа на рабочую (влажную) массу
Рассчитаем процентное содержание водяных паров в 1 м 3 природного газа:
H2O в . г = ;
H2O в.г =%
Пересчитаем состав газа на рабочую массу по формуле:
x в.г =x c .г % ;
CH4 в.г = 98,3*= 96,6%;
1.3 Расчет количества кислорода и воздуха для сжигания 1 м 3 газа
Найдем объем кислорода, необходимый для окисления горючих составляющих природного газа.
=0,01[(m+n∕ 4)∑CmHn в.г. ];
=0,01(2·96,6+3.5·0,129+5·0.009)=1,939 м 3 /м 3 .
Находим количество воздуха при α=1, необходимое для сжигания 1 м 3 природного газа, используя соотношение азота и кислорода в воздухе К=3,76:
L0 с.в =(1+K)
Практически введенное количество воздуха при α=1,2 составит:
1.4 Расчет объема и состава продуктов сгорания при сжигании 1 м 3 газа
Найдем объем продуктов сгорания при α=1
= 0,01[CH4 в. + 2C2H6 в.г +3C3H8 в.г +4C4H10 в.г ] =0,969 м 3 /м 3 ;
= 0,01[H2O в.г +2CH4 в.г +3C2H6 в.г +4С3H8 в.г +5C4H10 в.г ]=1,942 м 3 /м 3 ;
= 7,26 м 3 /м 3 ;
V0=0,969 +1,942 +7,26 =10,17м 3 /м 3 .
Выход продуктов сгорания при α=1,2 изменится только на величину содержания азота, внесенного с избытком воздуха, и на величину избыточного кислорода:
8,7 м 3 /м 3 ;
=0,386 м 3 /м 3 ;
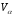
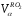
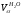
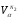
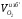
Состав продуктов сгорания при α=1:
Состав продуктов сгорания при α=1,2:
1.5 Расчет теплоты сгорания природного газа
В формулу для Qн р , подставим горючие составляющие, которые указаны в исходных данных и пересчитаны на рабочую массу:
Qн р =34666
1.6 Расчет температур горения
Определим химическую энтальпию топлива:
Физическая энтальпия подогретого воздуха, где св взята из прил. 2.
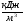
Общая энтальпия продуктов сгорания составит:
Используем приложение 1 — диаграмму itи вычисляем содержание избыточного воздуха в продуктах сгорания:
Теоретическая температура горения природного газа tα т =1950°С.
Энтальпия химического недожога
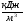
Общее балансовое теплосодержание продуктов сгорания:
Балансовая температура горения природного газа tα т =1970°С.
2 Определение тепловых потоков и температур металла по длине печи
2.1. Определение теплового потока и температур металла в сечении 2
Для расчета лучистого теплообмена необходимо знать эффективную толщину излучающего слоя печных газов вблизи сечение 2, м:
Высота рабочего пространства над заготовками найдена с использованием размеров, указанных на рис. 1.1:
H2 = Н— S=2,54-0,3= 2,24 м, а ширина печи D =2,6 м оставлена без изменения.
Задаем температуру газов в сечении 2 tг2 = 1280°С. Затем из расчета объема и состава продуктов сгоранияопределяем содержание Н20 и С02.
Получаем содержание излучающих газов, а печной атмосфере, а именно:
0,01 Sэф Н2О = 0,01∙ 2,21∙ 11,66= 0,25 атм∙м,
которые необходимы для определения степени черноты при с помощью прил. 6,7 и 8 заданной температуре газов tг2 = 1280°С: водяного пара εСО2 =0,096; εН2О=β∙ εН2О=1,05∙0,14=0,147
Затем определяем степени черноты: продуктов горения
Определяем степень развития кладки вблизи сечения 2:
Приведенный коэффициент излучения для системы «газ — кладка — металл» в сечении 2:
Удельный лучистый тепловой поток на металл в рассчитываемом сечении
При известном коэффициенте конвективного теплообмена ак2 определяем конвективную составляющую общего теплового потока:
Суммарный тепловой поток на металл в сечении 2 составит
Полагаем, что тепловая мощность низа печи составляет 50 % от общей, т.е. отношение этих мощностей равно
Используя это отношение, по прил. 9 находим = 0,58 и прогреваемые толщины слитка: сверху SB =0,580,35 = 0,203 м и снизу 5„ =0,35 -0,203 = 0,147 м.
Определяем минимальную температуру по сечению слитка перед его заходом на сплошной под
куда подставили из прил. 10 теплопроводность малоуглеродистой стали = 28 Вт/(м-К) при температуре на 100 °С ниже, чем конечная температура поверхности.
Определяем температуру массы верхней части слитка
Источник