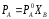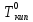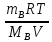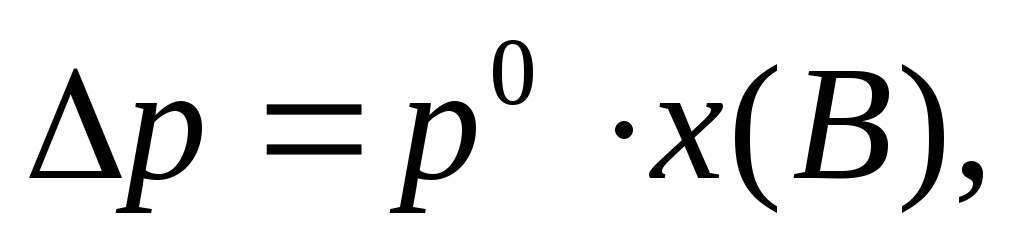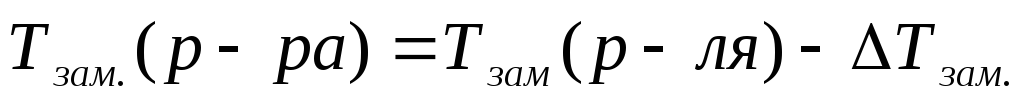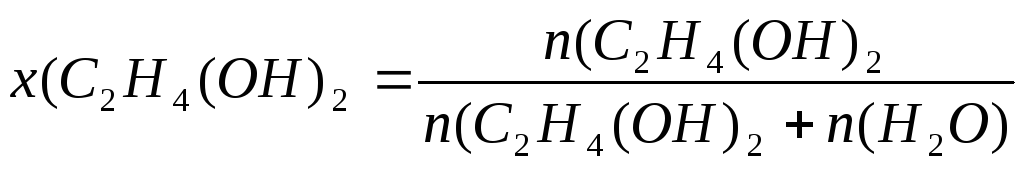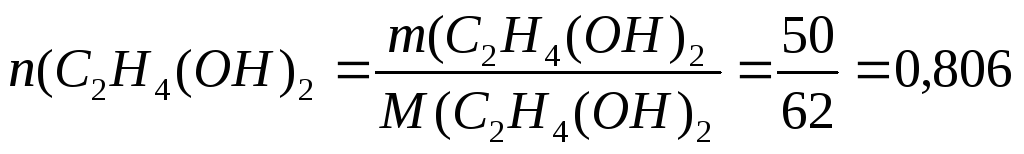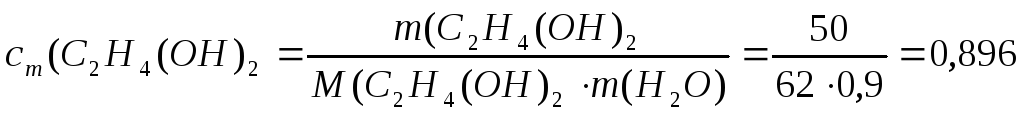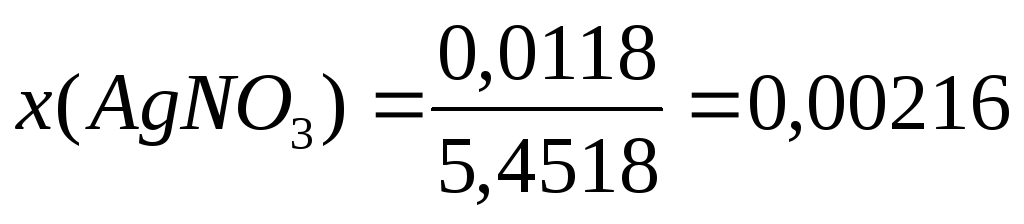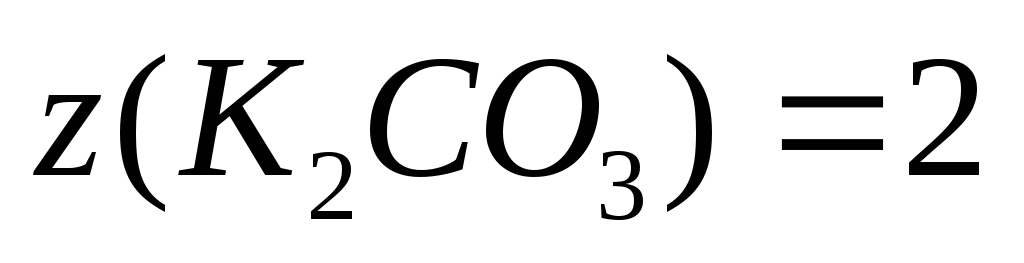10 Лекция: Растворы неэлектролитов. Общие понятия и определения.
Раствор – это гомогенная смесь, состоящая из двух или более веществ, однофазовая система (нет поверхности раздела).
В растворе в каждой точке его объема физическая величина имеет одно и то же значение. Растворы бывают: твердые, жидкие (неэлектролиты, электролиты).
Составляющие раствор вещества компоненты делятся на растворитель и растворённое вещество.
Растворитель – вещество, концентрация которого намного больше концентрации остальных веществ.
Наибольшая концентрация растворимого вещества, при которой устанавливается равновесие, называется растворимостью.
Раствор, находящийся в равновесии с избытком растворимого вещества, называется насыщенным.
Межчастичные взаимодействия в растворах.
В процессе образования раствора вещества теряют свою индивидуальность.
Физические и термодинамические свойства раствора определяются: природой частиц присутствующих в растворе, характером взаимодействия между ними.
В растворе могут взаимодействовать, как молекулы так и более сложные образования – комплексы.
В растворах неэлектролитов преобладает межмолекулярное взаимодействие, которое можно разделить на две группы:
1) Взаимодействие обусловленное ориентационными, индукционными и дисперсионными силами.
Ориентационные – взаимодействие между молекулами имеет постоянный дипольный момент.
Индукционные – взаимодействие между молекулой с постоянным диполем и молекулой с наведенным диполем.
Дисперсионные – имеют сложную природу- в каждый данный момент электроны в молекуле находятся в движение на некотором расстояние от ядра, т.е. в молекуле есть всегда мгновенная ассиметрия электрического заряда, а значит мгновенный диполь.
Который индуцирует дипольный момент другой молекулы.
2)Взаимодействие вызываемое образованием сольватов и различных донорно-акцепторных комплексов.
Термодинамический параметр состояния растворов.
Для описания термодинамического состояния раствора можно использовать следующие параметры T,P,V,состав.
Состав удобнее всего выражать, через число молей ni или мольную долю.
Как показывает опыт для полного описания состава раствора достаточно 3-х величин T,P,ni.
Парциальные мольные величины.
П.м.в. i-го компонента, это частная производная от любого экстенсивного свойства раствора по числу молей i – го компонента при условии постоянства T,P и числа молей остальных компонентов.
Парциальная мольная энергия Гиббса есть химический потенциал.
Если к раствору большему по массе компонентов при T,P=const добавить 1 моль i – го компонента, то полученные изменения экстенсивного свойства вкладом i- го компонента в изменение общего экстенсивного свойства системы.
Основные свойства п.м.в.
1.Не зависят от мольной массы раствора, а зависит только от его состава т.е. при наращивании массы раствора и постоянстве соотношения между числами молей компонентов п.м.в. остаются постоянными.
2.П.м.в. связаны между собой двумя уравнениями:
Оно показывает, что любое экстенсивное свойство раствора может быть найдено путем аддитивного сложения произведений п.м.в. на состав.
Для п.м.в. компонентов раствора можно применить все термодинамические формулы выведенные для чистых веществ, заменив в них экстенсивные величины но соответствующие парциально – мольные.
Источник
Растворы неэлектролитов.
Неэлектролитами называются вещества, растворы которых не проводят электрический ток. Неэлектролиты – это вещества с неполярной или малополярной ковалентной связью, в растворах они находятся в виде молекул.
Разбавленные растворы неэлектролитов проявляют коллигативные свойства, то есть такие свойства и закономерности, которые зависят только от количества частиц в растворе (концентрации) и не зависят от природы этих частиц.
Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причем коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.
,
где РA 0 – давление пара чистого растворителя, РA – давление пара растворителя над раствором, ХB – мольная доля растворенного вещества.
Этот закон можно выразить в другом виде:
Относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества и не зависит от природы растворенного вещества.
.
Второй закон Рауля. Изменение температуры кристаллизации и температуры кипения раствора
Замерзание растворов можно охарактеризовать величиной понижения температуры замерзания ΔТзам, равной разности между температурой замерзания чистого растворителяи температурой начала кристаллизации раствора Tзам:
ΔTзам. = T 0 зам.–.
Понижение температуры замерзания раствора ΔTзам прямо пропорционально моляльной концентрации раствора:
,
где Kкрио – криоскопическая постоянная растворителя – определяется природой растворителя (для воды Kкрио =1,86), В – растворенное вещество, A ‑ растворитель
Температура кипения растворов нелетучего вещества всегда выше, чем температура кипения чистого растворителя при том же давлении.
Повышение температуры кипения растворов нелетучих веществ ΔTкип = Tкип –пропорционально понижению давления насыщенного пара и, следовательно, прямо пропорционально моляльной концентрации раствора. Коэффициент пропорциональности E есть эбулиоскопическая постоянная растворителя (для воды Е=0,52), не зависящая от природы растворенного вещества.
ΔTкип = ECмл = Е.
В общем виде второй закон Рауля:
Понижение температуры замерзания и повышение температуры кипения разбавленного раствора нелетучего вещества прямо пропорционально моляльной концентрации раствора и не зависит от природы растворенного вещества.
Второй закон Рауля является следствием из первого; данный закон справедлив только для бесконечно разбавленных растворов.
Осмотическое давление разбавленных растворов. Растворенное вещество стремится равномерно распределиться по всему объему раствора. Происходит диффузия – переход молекул растворенного вещества через поверхность раздела в растворитель и одновременно молекул растворителя в раствор. Такая встречная, двухсторонняя диффузия растворенного вещества и растворителя продолжается до тех пор, пока система не придет в состояние равновесия или пока энтропия системы не станет максимальной. Можно сделать диффузию односторонней, разделив некоторый раствор и растворитель полупроницаемой перегородкой (мембраной), проницаемой для молекул растворителя и непроницаемой для молекул растворенного вещества. Если сосуд 1, закрытый внизу полупроницаемой перегородкой 2 и наполненный водным раствором какого-либо вещества, например сахарозы, поместить в сосуд 3 с водой, то вода будет проходить из сосуда 3 в сосуд 1 (рис. 36.). Явление самопроизвольного перехода растворителя через полупроницаемую перегородку в раствор называется осмосом. Через некоторое время объем раствора в сосуде 1 увеличится и его уровень поднимется выше уровня растворителя в сосуде 3 на высоту h. В результате увеличения объема раствора в сосуде 1 возникает гидростатическое давление, называемое осмотическим давлением – π, которое количественно оценивается высотой h подъема жидкости в сосуде 1.
Рис. 36 ‑ Прибор для определения осмотического давления
Осмотическое давление зависит от концентрации растворенного вещества и температуры. Эта зависимость (принцип Вант-Гоффа) выражается уравнением:
π= СМRT = .
Осмотическое давление идеального раствора равно тому давлению, которое оказывало бы растворенное вещество, если бы оно, находясь в газообразном состоянии при той же температуре, занимало бы тот же объем, который занимает раствор.
Источник
II. Коллигативные свойства растворов неэлектролитов
Раствор неэлектролита состоит из растворителя и растворенного вещества в виде недиссоциированных молекул. Коллигативными свойствами раствора неэлектролита являются свойства, которые зависят от концентрации и практически не зависят от природы неэлектролита. К таким свойствам относятся:
Относительное понижение давления насыщенного пара растворителя над раствором (I закон Рауля)
(8)
(8а)
р 0 — давление насыщенного пара над чистым растворителем, Па;
р – давление насыщенного пара над раствором неэлектролита, Па;
х(В) – молярная доля неэлектролита в растворе;
Понижение температуры замерзания (II закон Рауля)
(9)
(9а)
Кк – криоскопическая константа, Kk(H2O)=1,86 К×кг/моль
сm(B) – моляльная концентрация неэлектролита, моль/кг;
Повышение температуры кипения (II закон Рауля)
(10)
(10а)
Кэ–эбуллиоскопическая постоянная, Кэ(Н2О)=0,52 К×кг/моль
Осмотическое давление раствора (закон Вант-Гоффа)
R= 8,314 л×Па/моль×К, Т – температура, К
с(В) – молярная концентрация неэлектролита, моль/л
Пример 5. Давление насыщенного пара воды при 50 0 С равно 12334 Па. Вычислите давление насыщенного пара воды над раствором, содержащим 50г этиленгликоля C2H4(OH)2 в 900г воды. Определите температуру замерзания этого раствора.
Решение. 1.Рассчитаем молярную долю вещества в растворе по формуле (3):
моль;
моль, М(Н2О)= 18 г/моль;
;
2.Рассчитаем понижение давления насыщенного пара:
Па;
3.Рассчитаем давление насыщенного пара над раствором:
Па;
4.Определим Тзам по формуле (9):
моль/кг; 0
Пример 6. Сколько граммов глицерина С3Н8О3 надо растворить в 2 л воды, чтобы получить раствор, закипающий при 100,6 0 С?
- Определим Ткип по формуле (10а):

- Определим сm(В):

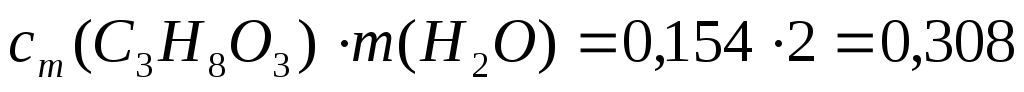





III. Коллигативные свойства растворов электролитов.
Раствор электролита состоит из растворителя и растворенного вещества (электролита), которое частично или полностью диссоциирует на ионы. В растворе число частиц в результате диссоциации увеличивается. Коллигативные свойства растворов электролитов описываются уравнениями с поправочным множителем – изотоническим коэффициентом ( i ), учитывающим процесс диссоциации: 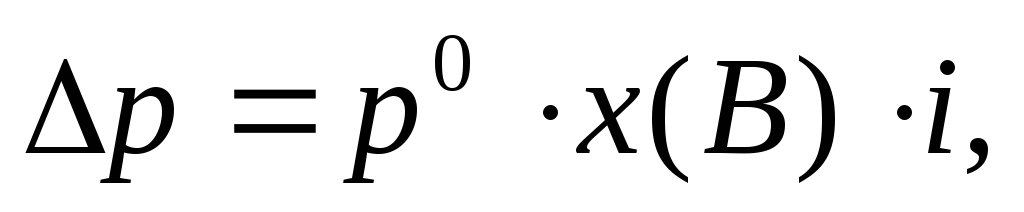





- Определим Ткип по формуле (10):



- Определим x(В)
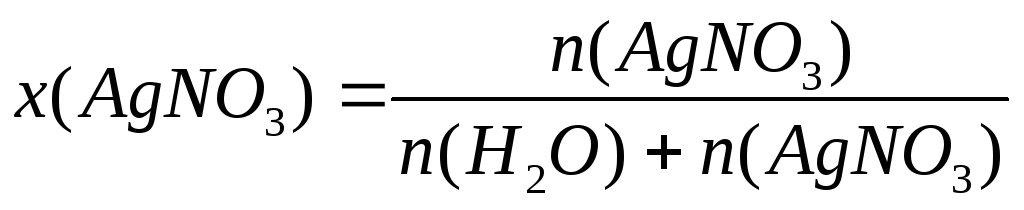


- Определим p по формуле (12):

- Определим p по формуле (8а):

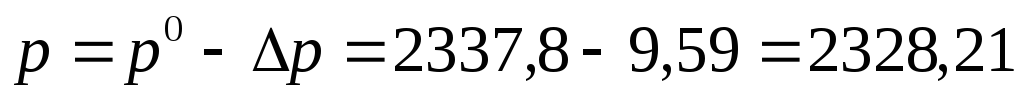
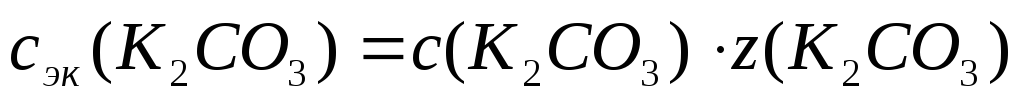


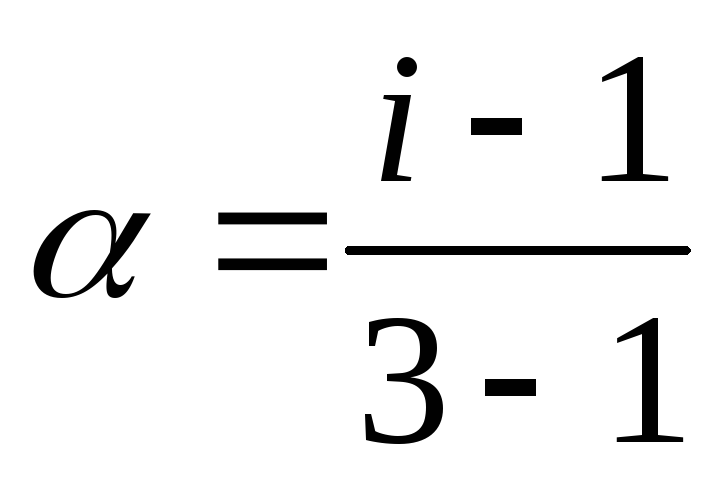
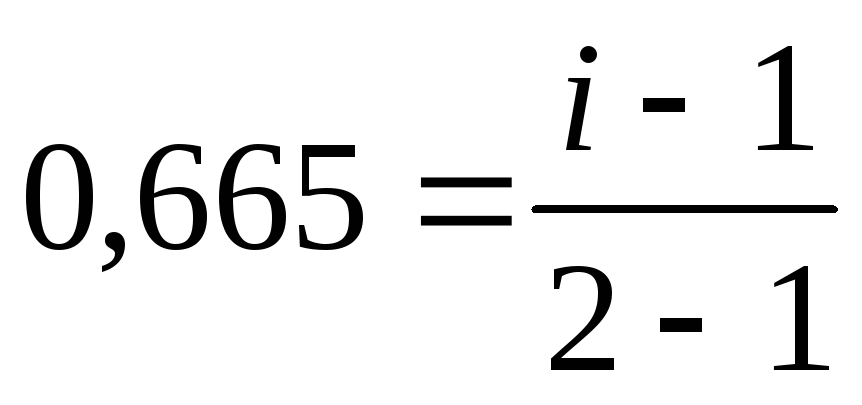

Источник