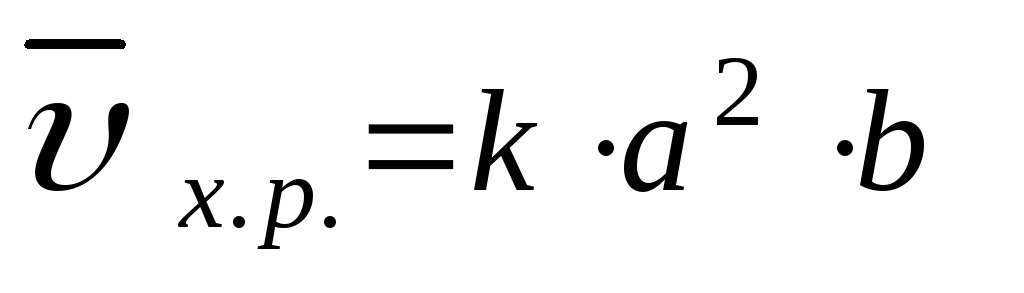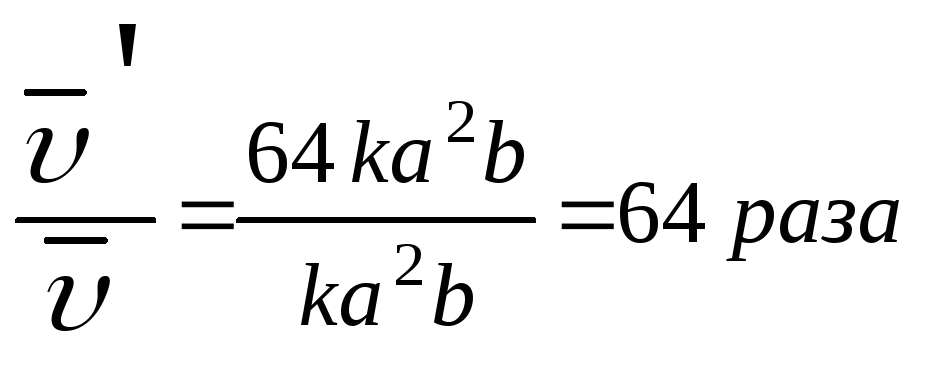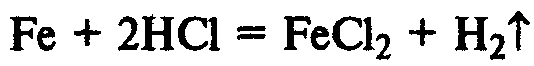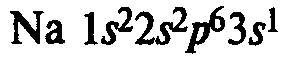Скорость химических реакций. Зависимость скорости химических реакций от природы реагирующих веществ, концентрации, температуры, катализатора
Скорость реакции – это число частиц образованных за единицу времени в единице объема.
Скорость химической реакции равна изменению количества вещества в единицу времени в единице реакционного пространства. Гомогенная реакция протекает в одной фазе. Гетерогенные реакции протекают на границе раздела фаз. [моль*м-3/с] не учитывая газы.
Все реакции можно подразделить на простые и сложные. Простые реакции протекают в одну стадию и называется одностадийными. Сложные реакции идут либо последовательно (многостадийные реакции), либо параллельно, либо последовательно-параллельно. В свою очередь, в каждой стадии реакции может участвовать одна молекула (мономолекулярные реакции), две молекулы (бимолекулярные) и три молекулы (тримолекулярные). Число молекул реагента, принимающих участие в простейшей (элементарной) стадии, называется её молекулярностью.
Порядок реакции — это сумма порядков реакции по реагентам.
Порядок реакции определяется суммой величин показателей степени при значениях концентраций исходных веществ в кинетическом уравнении:
Поэтому обе реакции первого порядка.
Молекулярность реакции определяется числом молекул, одновременным взаимодействием которых осуществляется акт химического взаимодействия. Реакция а) одномолекулярная, б) двухмолекулярная.
Выражение для определения скорости реакции первого порядка
Скорость реакции второго порядка для двух реагентов В и D подчиняется кинетическому уравнению
где С В – концентрация реагента В, а С D – концентрация реагента D.
Наиболее часто встречаются реакции первого и второго порядка. Реакции третьего порядка крайне редки. Реакции более высокого порядка, чем третий, неизвестны, так как в большинстве случаев реакции многостадийны.
Правило Вант-Гоффа. V2 = V1×gDT/ 10
Повышение температуры ускоряет большинство реакций. Согласно правилу Вант-Гоффа при увеличении температуры на 10 К скорость многих реакций увеличивается в 2-4 раза V2 = V1×gDT/ 10
Где V2 и V1 – скорость реакции при температурах Т2 и Т1, γ – коэффициент, значение которого для эндотермической реакции выше, чем для экзотермической реакции. Для многих реакций γ лежит в пределах 2- 4.
Скорость химических реакций зависит:
1. Природа реагирующих веществ
б) 2K+2H2O=2KOH+H2 Скорость реакции» б» больше чем «а», так как калий активнее натрия.
2. Концентрация. Чем выше концентрация, тем больше скорость реакции, Эта зависимость выражается законом действующих масс.
Например, сера горит в чистом кислороде и на воздухе. СКОРОСТЬ ГОРЕНИЯ СЕРЫ В КИСЛОРОДЕ В 5 раз больше, чем на воздухе.
Химические реакции, протекающие в гомогенных системах (смеси газов, жидкие растворы), осуществляется за счет соударения частиц. Однако, не всякое столкновение частиц реагентов ведет к образованию продуктов. Только частицы, обладающие повышенной энергией — активные частицы, способны осуществить акт химической реакции. С повышением температуры увеличивается кинетическая энергия частиц и число активных частиц возрастает, следовательно,
| химические реакции при высоких температурах протекают быстрее, чем при низких температурах |
Возрастание химические реакции при высоких температурах протекают быстрее, чем при низких температурах скорости реакции при нагревании в первом приближении подчиняется следующему правилу:
| при повышении температуры на 10 0С скорость химической реакции возрастает в два — четыре раза. |
3. Катализатор — вещество, изменяющее скорость реакции. Он может как увеличивать скорость реакции так и уменьшать (такой катализатор называется ингибитором).
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник
1. Зависимость скорости химической реакции от природы реагирующих веществ.
Говорить о скорости химической реакции имеет смысл, если природа реагирующих веществ позволяет им вступать в химическое взаимодействие. Например, природа реагирующих веществ позволяет протекать первой и второй реакции, но не позволяет третьей.
1. Mg + O2 2MgО
2. Zn + 2HCl ZnCl2 + H2↑
3. NaOH + KOH ≠
2. Зависимость скорости химической реакции от концентрации реагирующих веществ определяется законом действия масс, который был установлен в 1867г опытным путем Гульдбергом и Вааге.
Скорость химической реакции при данной температуре пропорциональна произведению концентраций реагирующих веществ в степени, равной стехиометрическому коэффициенту, стоящему перед формулой данного вещества в уравнении реакции.
Закон действия масс справедлив только для наиболее простых по своему механизму реакций взаимодействия, протекающих в газах или в разбавленных растворах.
1.aA(Ж) + bB(Ж) ↔ cC(Ж) + dD(Ж) ; (T=const)
2. 3H2(Г) + N2(Г) ↔ 2NH3(Г);
1. aA(т) + bB(Г) = cC(Г) + dD(Г); 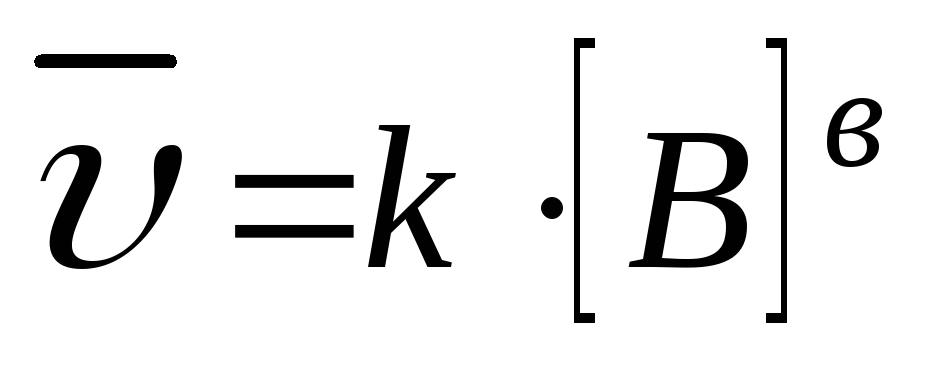
В законе действия масс не учитываются концентрации веществ, находящихся в твердой фазе. Чем больше площадь поверхности твердой фазы, тем выше скорость химической реакции.
k – константа скорости химической реакции определяется природой реагирующих веществ и зависит от температуры, от присутствия в системе катализатора, но не зависит от концентрации реагирующих веществ. Константа скорости представляет собой скорость химической реакции (

3. Зависимость скорости химической реакции от давления. Для газообразных систем увеличение давления или уменьшение объема, равноценно увеличению концентрации и наоборот.
Задача: Как изменится скорость химической реакции 2SO2(г) + O2(г) 2SO3(г), если давление в системе увеличить в 4 раза?
В соответствие с законом действия масс для прямой реакции, записываем выражение:

Уменьшение объема в 4 раза соответствует увеличению концентрации в системе в 4 раза, тогда
;
.
4. Зависимость скорости химической реакции от температуры.
Влияние температуры на скорость химической реакции приближенно определяется правилом Вант-Гоффа. При повышении температуры на 10 0 С скорость химической реакции возрастает в 2-4раза.
Математическая запись правила Вант-Гоффа: γ — температурный коэффициент скорости реакции или коэффициент Вант-Гоффа для большинства реакций лежит в пределах 2-4.
Задача. Во сколько раз изменится скорость химической реакции, протекающей в газовой фазе, если температура изменилась от 80 0 С до 120 0 С (γ = 3)?
В соответствии с правилом Вант-Гоффа записываем:
Увеличение скорости химической реакции при повышении температуры объясняется не только увеличением кинетической энергии взаимодействующих молекул. Например, число столкновений молекул растет пропорционально корню квадратному из абсолютной температуры

Энергия активации (EА)– это тот избыток энергии по сравнению со средним запасом, которым должны обладать молекулы для осуществления химической реакции. Если ЕА< 40 кДж/моль – реакции протекают быстро, если ЕА > 120 кДж/моль – реакции не идут, если ЕА = 40-120 кДж/моль – реакции протекают в обычных условиях. Повышение температуры снижает энергию активации, делает вещества более реакционно-способными, скорость взаимодействия при этом увеличивается.
Более точную зависимость скорости химической реакции от температуры установил C.Аррениус: константа скорости реакции пропорциональна основанию натурального логарифма, возведенного в степень ( –ЕА/RT). ,
А – предэкспоненциальный множитель, определяет число активных
е – экспонента (основание натурального логарифма).
Логарифмируя выражение , получим уравнение:
. Уравнение Аррениуса показывает, что скорость реакции тем выше, чем меньше энергия активации. Для снижения энергии активации используют катализаторы.
Источник
Билет №8.
Скорость химических реакций. Факторы, влияющие на скорость химической реакции (зависимость скорости от природы, концентрации вещества, площади поверхности соприкосновения реагирующих веществ, температуры, катализатора).
Скоростью химической реакции называется изменение количества вещества за единицу времени в единице объема.
Скорость реакции зависит от природы реагирующих веществ.
При реакции металлов с соляной кислотой, чем левее расположен металл в раду напряжений, тем быстрее протекает реакция, а металлы, находящиеся правее водорода, не реагируют вообще:
Скорость реакции увеличивается при увеличении концентрации реагирующих веществ.
Горение веществ в чистом кислороде происходит быстрее, чем в воздухе, содержание кислорода в котором составляет 21%:
Скорость реакции увеличивается при увеличении поверхности соприкосновения реагирующих веществ.
Железные опилки быстрее реагируют с соляной кислотой, чем железные гвозди:
Скорость реакции увеличивается с увеличением темпера-
Железо при обычной температуре реагирует с хлором очень медленно, при высокой же температуре протекает бурная реакция (железо горит в хлоре):
Водород восстанавливает оксиды металлов при нагревании, при комнатной температуре эта реакция не идет, то есть ее скорость равна 0:
Скорость многих реакций увеличивается в присутствии специальных веществ — катализаторов.
Катализаторы увеличивают скорость реакции, но по окончании реакции остаются неизменными.
Примеры каталитических реакций:
(реакция сильно ускоряется в присутствии МnО2).
(реакция протекает только в присутствии катализаторов — платины, оксида ванадия (V), железа и др).
Билет №9.
Общая характеристика металлов главных подгрупп I – III групп (I-A – III-A групп) в связи с их положением в периодической системе химических элементов Д. И. Менделеева и особенности строение их атомов, металлическая химическая связь, химические свойства металлов как восстановителей.
В периодической системе элементов металлы в основном располагаются в главных подгруппах I—Ill групп, а также в побочных подгруппах.
В IA группе у атомов элементов на внешнем энергетическом уровне находится 1 электрон в состоянии s 1 , во IIA группе у атомов на внешнем ЭУ 2 электрона в состоянии s 2 . Эти элементы относятся к s-элементам. В IIIA группе у всех элементов на внешнем ЭУ 3 электрона в состоянии s 2 p 1 . Они относятся к p-элементам.
В IA группу входят щелочные металлы Li, Na, K, Rb, Cs, Fr, активность которых при движении сверху вниз увеличивается вследствие увеличения радиуса атомов, металлические свойства возрастают также, как и у щелочеземельных металлов IIA группы Be, Mg, Ca, Sr, Ba, Ra и металлов IIIA группы Al, Ga, In, Tl.
Оксиды типа R2O характерны только для Li, для всех остальных щелочных металлов характерны пероксиды R2O2, которые являются сильными окислителями.
Все металлы этих групп образуют основные оксиды и гидроксиды, кроме Be и Al, которые проявляют амфотерные свойства.
Химические свойства. Атомы металлов имеют больший радиус, чем атомы неметаллов, поэтому легко теряют валентные электроны. Вследствие этого металлы проявляют восстановительные свойства.
Источник