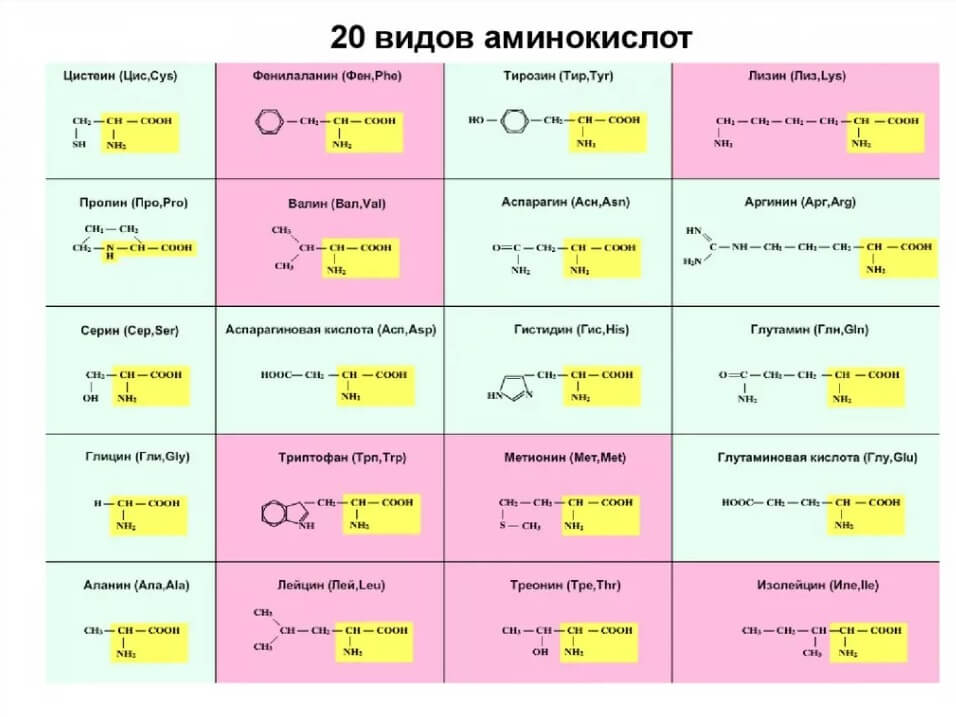
- 20 аминокислот с формулами
- Классификация аминокислот и их назначение
- Структурные формулы и наименования аминокислот
- Избыток и недостаток аминокислот в организме
- Аминокислоты
- Номенклатура аминокислот
- Физические свойства аминокислот
- Получение аминокислот
- Химические свойства аминокислот
- 1.1. Взаимодействие с металлами и щелочами
- 1.2. Взаимодействие с кислотами
- 2. Взаимодействие с азотистой кислотой
- 3. Взаимодействие с аминами
- 4. Этерификация
- 5. Декарбоксилирование
- 6. Межмолекулярное взаимодействие аминокислот
20 аминокислот с формулами
Аминокислоты – это кристаллические вещества с высокой температурой плавления и сладковатым вкусом. Они хорошо растворяются в воде, но плохо растворяются в органических растворителях. Аминогруппа обуславливает основные свойства аминокислот, карбоксильная группа – кислотные свойства.
Аминокислоты являются неотъемлемой частью процесса, связанного с биосинтезом белка.
Характерное свойство белка — это его способность к расщеплению на аминокислоты внутри пищеварительной системы в организме.
Количество основных пептидов в природе насчитывает около 200 наименований. Однако, для правильного построения биологической составляющей организма, необходимо только 20 самых основных из них.
Классификация аминокислот и их назначение
В биологии установлена основная классификация аминокислот, которая подразделяется на две группы:
Аминокислоты, которые можно заменить – это четко выраженная группа аминокислот, которые попадают в организм путем употребления продуктов питания.
Так же они могут образоваться внутри организма человека и любых других веществ.
К заменимым аминокислотам относится следующие показатели:
- Аланин – это измеритель огромного количества белковой составляющей, участвует в процессе гликогенолиза, тем самым преобразовывая в глюкозу в печени человека. Является основным регулятором пищеварительных процессов в организме.
- Аргинин – это аминокислота, особенностью которой является процесс синтеза в организме взрослого человека. В организме ребенка она не образуется. Входит в состав процесса системы синтеза, который связан с гормональным ростом. Является единственным веществом в организме, которое имеет способность взаимодействовать с азотом. Оказывает существенное воздействие на рост мышечной массы, путем снижения массы жира в теле.
- Аспарагин – это составной пептид, который необходим для азотного обмена. Взаимодействуя с основными ферментами имеет способность отщеплять аммониак и преобразовываться в кислоту.
- Аспаргиновая кислота. Дает возможность для восстановления при нарушении работы, связанной с нервной системой и работой сердечно-сосудистой системы.
- Гистидин – необходим для лечения болезней, связанных с кишечником, а также для профилактического лечения при заболевании СПИДом. Является показателем снижения факторов, которые связаны с внешними воздействиями.
- Глицин. Необходим в первую очередь как компонент успокоительного действия. Иными словами, служит как нейромедиатор.
- Глутомин – это аминокислота, которая входит в состав гемоглобина. Активно стимулирует процесс обмена в центральной нервной системе человека.
- Глютаминовая кислота –это кислота, которая оказывает непосредственное воздействие на работу всей нервной системы.
- Пролин –это аминокислота, входящая в состав всех протеинов в организме, максимальное его количество содержится в эластине и коллагенах.
- Серин – это компонент аминокислот, который входит в состав нейронов головного мозга человека и отвечает частично за его работу. Способствует выработке и затрате энергии. Его образование происходит при помощи глицина.
- Тирозин, встречается в тканевых клетках животных и растений. Может преобразовываться из фенилаланина.
- Цистеин, главный компонент, который можно встретить в составе кератина. Включен в состав антиоксидантов, может образовываться из ксилина.
Нет времени решать самому?
Незаменимые аминокислоты — это группа аминокислот, которые не обладают характерной особенностью синтеза в организме человека.
Организм способен получать данные аминокислоты, только через пищу в процессе потребления.
К незаменимым аминокислотам относятся следующие виды ферментов:
- Валин, является кислотой, повышающей координацию при активной работе мышечной части тела. Дает возможность нормализовать активную работу организма. Особенно это характерно для резких смен температуры воздуха.
- Изолейцин. Является естественным компонентом, который обогащает мышцы тела силой и энергией.
- Лейцин. Основной регулятор всех метаболических процессов, которые происходят в организме человека. Его функция заключается в строительстве структуры белка. Как и первые две аминокислоты относится к комплексу BCAA. Данные вещества оказывают существенное воздействие на повышение объема мышечной массы. Контролируют уровень содержания гомеостаза при высоких физических нагрузках.
- Лизин. Повышает скорость процесса регенерации тканей, образует необходимые организму гормоны, ферменты и разного вида антитела. Повышает прочность и надежность работы сосудов. Является составной частью коллагена.
- Метионин. Контролирует уровень жира в организме, тем самым уменьшает его содержание в печени.
- Треонин. Служит укрепляющим эффектом для сухожилий и благоприятно оказывает действие на зубную эмаль.
- Триптофан. Компонент регулирующий за психически-эмоциональное состояние человека. Оказывает значительное воздействие при лечении расстройств психики у человека.
- Фениалалнин. Регулятор правильной деятельности микрочастиц в коже человека. Значительно понижение или сводит до минимума пигментацию. Приводит в норму водно-солевой баланс для самых жизненно важных участков кожи.
Также, в некоторых случаях, возможно выделение третьей группы: условно заменимых аминокислот.
В зависимости от кислотно-основных свойств, которые основаны на строении радикала, аминокислоты принято разделять на четыре основные группы
- Неполярные или гидрофобные.
- Полярные незаряженные.
- Полярные, которые заряжены отражательными частицами, при pH=7.
- Полярные, положительно заряженные частицы при pH=7.
Структурные формулы и наименования аминокислот
Важнейшие аминокислоты, необходимы для правильной жизнедеятельности организма
Избыток и недостаток аминокислот в организме
Большинство видов аминокислот оказывают существенное воздействие на метаболизм в организме человека. Благодаря аминокислотам в организм поступает необходимое количество энергии, позволяющая образовывать химические реакции, которые основаны на дыхательных способностях, психоэмоциональных качествах и многих других. Некоторые аминокислоты содержатся непосредственно только в продуктах питания.
Низкий уровень аминокислот в организме человека, может привести к следующим характерным симптомам:
- плохое самочувствие;
- отставшие аппетита и непереносимость пищи;
- высокий уровень утомляемости и низкая активность;
- нарушение гомеостаза;
- постоянная сонливость;
- нестабильное нервно-психическое состояние.
В случае, когда в организме низкий уровень хотя бы одной аминокислоты, может произойти существенное ухудшение здоровья.
Когда в организме перенасыщение аминокислот, то может произойти сбой работы. И у человека возникают симптомы, которые характерны в большей степени пищевому отравлению.
Для нормальной работы организма следует всегда тщательно следить за своим питание, контролировать уровень белка. Четко составлять и планировать свой рацион питания, включая в него все необходимые продукты, которые содержат важные для организма аминокислоты.
Источник
Аминокислоты
Природные аминокислоты можно разделить на следующие основные группы:
Номенклатура аминокислот
- Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
| 2 – Аминобутановая кислота | 3-Аминобутановая кислота |
 |  |
- Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
| α-Аминомасляная кислота | β-Аминомасляная кислота |
 |  |
Физические свойства аминокислот
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
Получение аминокислот
- Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
- Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):
Химические свойства аминокислот
| При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион: |
1. Кислотно-основные свойства аминокислот
| Аминокислоты — это амфотерные соединения. |
Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
| Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп. |
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин — щелочной (одна группа -СООН, две -NH2).
1.1. Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:
1.2. Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с кислотами:
2. Взаимодействие с азотистой кислотой
Аминокислоты способны реагировать с азотистой кислотой.
| Например, глицин взаимодействует с азотистой кислотой: |
3. Взаимодействие с аминами
Аминокислоты способны реагировать с аминами, образуя соли или амиды.
4. Этерификация
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир:
| Например, глицин взаимодействует с этиловым спиртом: |
5. Декарбоксилирование
Протекает при нагревании аминокислот с щелочами или при нагревании.
| Например, глицин взаимодействует с гидроксидом бария при нагревании: |
| Например, глицин разлагается при нагревании: |
6. Межмолекулярное взаимодействие аминокислот
При взаимодействии аминокислот образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.
| Например, г лицин реагирует с аланином с образованием дипептида (глицилаланин): |
Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH — пептидной связью.
Источник