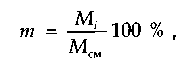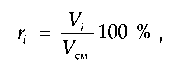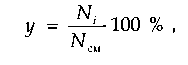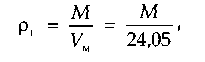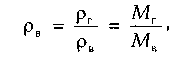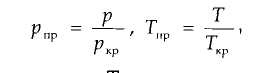Основные законы газового состояния
В основе физических свойств газов и законов газового состояния лежит молекулярно-кинетическая теория газов. Большинство законов газового состояния было выведено для идеального газа, молекулярные силы которого равны нулю, а объем самих молекул бесконечно мал по сравнению с объемом межмолекулярного пространства.
Молекулы реальных газов помимо энергии прямолинейного движения обладают энергией вращения и колебания. Они занимают некоторый объем, то есть имеют конечные размеры. Законы для реальных газов несколько отличаются от законов для идеальных газов. Это отклонение тем больше, чем выше давление газов и ниже их температура, оно учитывается введением в соответствующие уравнения поправочного коэффициента сжимаемости.
При транспортировании газов по трубопроводам под высоким давлением коэффициент сжимаемости имеет большое значение.
При давлениях газа в газовых сетях до 1 МПа законы газового состояния для идеального газа достаточно точно отражают свойства природного газа. При более высоких давлениях или низких температурах применяют уравнения, учитывающие объем, занимаемый молекулами, и силы взаимодействия между ними, или вводят в уравнения для идеального газа поправочные коэффициенты — коэффициенты сжимаемости газа.
Закон Бойля — Мариотта.
Многочисленными опытами установлено, что если взять определенное количество газа и подвергать его различным давлениям, то объем этого газа будет изменяться обратно пропорционально величине давления. Эта зависимость между давлением и объемом газа при постоянной температуре выражается следующей формулой:
где p1 и V1 — первоначальные абсолютное давление и объем газа; p2 и V 2 — давление и объем газа после изменения.
Из этой формулы можно получить следующее математическое выражение:
То есть произведение величины объема газа на величину соответствующего этому объему давления газа будет постоянной величиной при постоянной температуре. Этот закон имеет практическое применение в газовом хозяйстве. Он позволяет определять объем газа при изменении его давления и давление газа при изменении его объема при условии, что температура газа остается постоянной. Чем больше при постоянной температуре увеличивается объем газа, тем меньше становится его плотность.
Зависимость между объемом и плотностью выражается формулой:
Если отношение объемов газа заменить отношением их плотностей, то можно получить:
Можно сделать вывод, что при одной и той же температуре плотности газов прямо пропорциональны давлениям, под которыми находятся эти газы, то есть плотность газа (при постоянной температуре) будет тем больше, чем больше его давление.
Пример. Объем газа при давлении 760 мм рт. ст. и температуре 0 °С составляет 300 м 3 . Какой объем займет этот газ при давлении 1520 мм рт. ст. и при той же температуре?
760 мм рт. ст. = 101329 Па = 101,3 кПа;
1520 мм рт. ст. = 202658 Па = 202,6 кПа.
Подставляя заданные значения V, р1, р2 в формулу, получим, м 3 :
Закон Гей-Люссака.
При постоянном давлении с повышением температуры объем газов увеличивается, а при понижении температуры уменьшается, то есть при постоянном давлении объемы одного и того же количества газа прямо пропорциональны их абсолютным температурам. Математически эта зависимость между объемом и температурой газа при постоянном давлении записывается так:
где V — объем газа; Т — абсолютная температура.
Из формулы следует, что если определенный объем газа нагревать при постоянном давлении, то он изменится во столько раз, во сколько раз изменится его абсолютная температура.
Установлено, что при нагревании газа на 1 °С при постоянном давлении его объем увеличивается на постоянную величину, равную 1 /273,2 первоначального объема. Эта величина называется термическим коэффициентом расширения и обозначается р. С учетом этого закон Гей-Люссака можно сформулировать так: объем данной массы газа при постоянном давлении есть линейная функция температуры:
Закон Шарля.
При постоянном объеме абсолютное давление неизменного количества газа прямо пропорционально его абсолютным температурам. Закон Шарля выражается следующей формулой:
Из формулы можно сделать вывод, что при постоянном объеме давление газа при нагревании увеличивается во столько раз, во сколько раз увеличивается его абсолютная температура.
Источник
1.4. Состав и свойства природного газа
Природный газ представляет собой смесь предельных углеводородов состава СпН2п+2, в которой содержится метан, этан, пропан, бутан и иногда пары более тяжелых углеводородов. Часто в состав природных газов входят азот N2 (до 40 % по объему), углекислота СО2, сероводород H2S и редкие газы.
В газе газовых и газоконденсатных месторождений обычно преобладает метан; его доля достигает 98,8 %; в нефтяном (попутном) газе доля метана намного меньше, однако увеличивается доля более тяжелых углеводородов — этана, пропана и бутана [5, 7, 13, 41].
Состав газовых смесей выражается в виде массовой, объемной или молярной доли компонентов в процентах. Массовая доля в процентах какого-либо компонента газовой смеси представляет собой отношение массы этого компонента к массе всей смеси:
где Мi — масса i-го компонента; Mсм — масса смеси.
Объемная доля (%) какого-либо компонента в смеси газов равна отношению объема компонента к объему всей смеси:
где Vi — объем /-го компонента в смеси; Vсм — объем всей смеси.
Молярная доля компонента определяется аналогично и может быть представлена в виде
где Ni — число молей г-го компонента в смеси; Ncm — суммарное число молей газа в смеси.
Физические свойства природного газа зависят от его состава, но в целом близки к свойствам метана как основного компонента смеси.
Плотность природного газа можно определить взвешиванием или вычислить, зная молекулярную массу смеси М:
где Vm — объем моля газа при стандартных условиях, м 3 .
Обычно рг находится в пределах 0,73— 1,0 кг/м 3 . В расчетах часто используют более удобную величину — относительную плотность Δ так как значение ее практически не зависит от давления и температуры. За величину сравнения принимают плотность воздуха
где МГ — масса газа; Мв — масса воздуха.
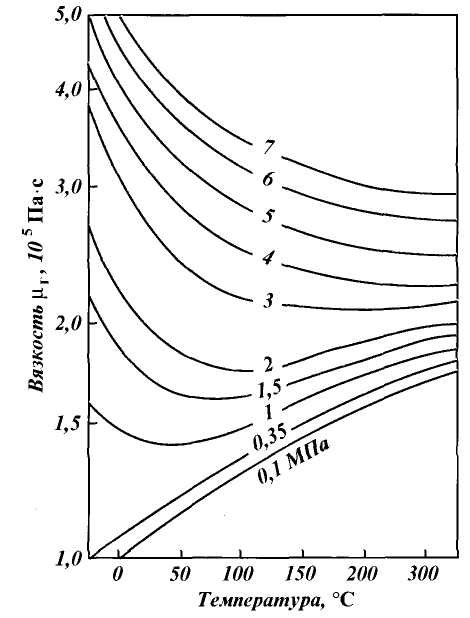
Относительная плотность газа изменяется от 0,50 до 1,0. Плотность индивидуальных компонентов углеводородных газов (и сероводорода), за исключением метана, больше единицы. При всех расчетах, связанных с движением газа, используется вязкость. Аналитические зависимости вязкости смеси от вязкости входящих в смесь компонентов сложны и имеют недостаточную точность. В связи с этим на практике вязкость определяют по экспериментальным графикам, один из которых приведен на рис. 1.2.
Рис. 1.2. Зависимость вязкости природного газа μ (при Δ = 0,6) от температуры
Состояние газа характеризуется давлением р, температурой Т и объемом V. Соотношение между этими параметрами определяется законами идеальных газов (Бойля — Мариотта, Гей-Люссака и др.), которые имеют чрезвычайно большое
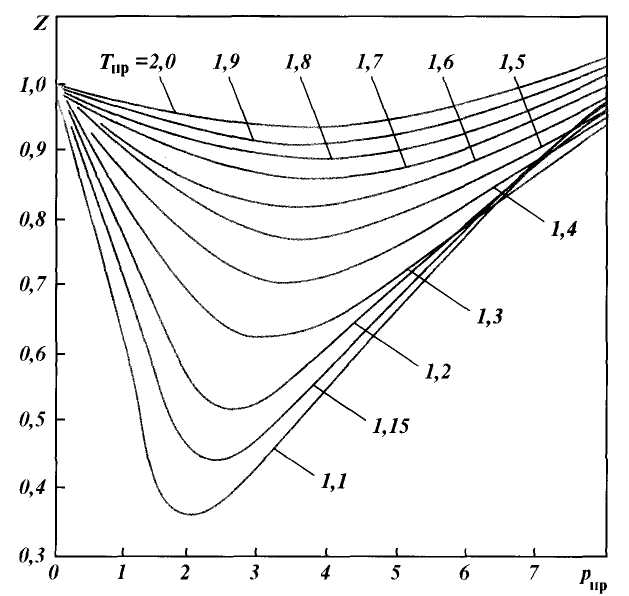
Рис. 1.3. Зависимость коэффициента сжимаемости природного газа от приведенного давления при различных температурах
pV = ZMRT,
где Z — коэффициент сжимаемости; М — масса газа; р — давление; V — объем газа; R — газовая постоянная; Т — абсолютная температура.
Для нефтяных газов значение коэффициента сжимаемости Z можно найти приближенно
Относительная плотность газа
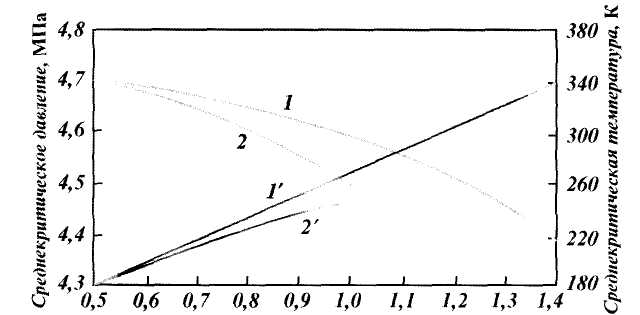
Рис. 1.4. Зависимость среднекритического давления (1, 2) и температуры (1‘ 2′ ) природного газа от относительной плотности:
1, 1‘ — газовое месторождение; 2, 2′ — газоконденсатное месторождение
по графикам Брауна, представленным на рис. 1.3. Коэффициенты сжимаемости Z на этом графике зависят от приведенных давления рпр и температуры Тпр , значения которых можно определить по формулам
где р и Т — соответственно давление и температура газа; ркр и Ткр — критические давления и температура.
Рис. 1.5. Энтальпия природного газа в зависимости от давления и температуры (при относительной плотности газа Δ = 0,6)
газа на конечном участке изменения его давления. Эту величину обычно находят по кривым теплосодержания (рис. 1.5). Зная давление газа и его температуру при одном состоянии, по этим кривым можно найти температуру газа после дросселирования. Для этого от первоначальной точки по линии равного теплосодержания следует переместиться в точку нового значения давления. Температура, соответствующая этой точке, явится искомой величиной. Изменение температуры газа при снижении давления на 0,1 МПа называется коэффициентом Джоуля — Томсона. Эта величина составляет 0,25 — 0,35 °С на 0,1 МПа (1 атм).
Источник