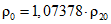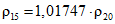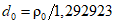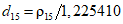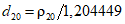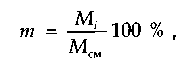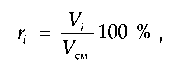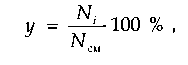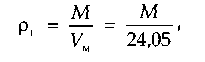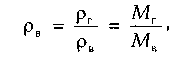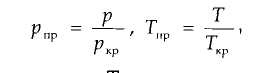- § 7. Плотности природного газа, стабильного и насыщенного углеводородного конденсата
- ПЕРЕСЧЕТ ПЛОТНОСТИ И РАСЧЕТ ОТНОСИТЕЛЬНОЙ ПЛОТНОСТИ ПРИРОДНОГО ГАЗА ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИИ 101,325 кПа
- «ГОСТ 34721-2021. Межгосударственный стандарт. Газ природный. Определение плотности пикнометрическим методом» (введен в действие Приказом Росстандарта от 16.04.2021 N 221-ст)
- 1.4. Состав и свойства природного газа
§ 7. Плотности природного газа, стабильного и насыщенного углеводородного конденсата
где р,t и рoto —плотности газа соответственно при давлении р1 и температуре t и нормальном давлении ро и температуре tо.
Плотность стабильного углеводородного конденсата (C5+) можно определить путем непосредственного измерения, расчета по формулам (по известному составу, по его молекулярной массе Мк или коэффициенту преломления nd).
где tкип—средняя температура кипения конденсата, °С.
Результаты расчетов по этим формулам в зависимости от группового состава конденсата (молярных долей парафиновых, нафтеновых и ароматических углеводородов в его составе) и молекулярной массы получают с определенной погрешностью.
Коэффициент термического расширения стабильного конденсата для большинства газоконденсатных месторождений t = 0,810 -3 1/°С, коэффициент сжимаемости конденсата К= -1,8 ГПа -1 .
Зависимость плотности стабильного конденсата от давления и температуры (при 30
Плотность насыщенного углеводородного конденсата можно определить по графоаналитическому методу Катца и Стендинга [25] и расчетным путем по приведенным параметрам. По методу Катца и Стендинга сначала определяется плотность жидкости при стандартных условиях по формуле (III.46)
где xi, Mi и i — молярная доля, молекулярная масса и плотность i-ro компонента соответственно.
Далее определяются поправки к вычисленной плотности при стандартных условиях на давление p и температуру t.
Плотность насыщенной жидкости при заданных давлении и температуре определяется по формуле = ст + р-рt. (III.46)
Плотность по приведенным параметрам определяется следующим образом:
где пр —приведенная плотность; Vкр i — критический молярный объем i-ro компонента в смеси.
Приведенную плотность определим по формуле Викса
где zкр.см — среднекритический коэффициент сверхсжимаемости жидкой смеси; Tпр — приведенная температура насыщенной жидкости, zкр.см= . (III.49)
Здесь zкpi — критический коэффициент сверхсжимаемости i-ro компонента. Его можно найти по табл. III.5 или определить по формуле Ганна и Ямады
Для ориентировочных расчетов можно воспользоваться формулой Л. П. Филиппова зависимости приведенной плотности от приведенной температуры, справедливой для чистых органических жидкостей в интервале приведенных температур 0.3пр
Порядок расчета плотности насыщенной жидкости:
Приведён пример и номограмма для определения плотности углеводородных газов
Источник
ПЕРЕСЧЕТ ПЛОТНОСТИ И РАСЧЕТ ОТНОСИТЕЛЬНОЙ ПЛОТНОСТИ ПРИРОДНОГО ГАЗА ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИИ 101,325 кПа
«ГОСТ 34721-2021. Межгосударственный стандарт. Газ природный. Определение плотности пикнометрическим методом» (введен в действие Приказом Росстандарта от 16.04.2021 N 221-ст)
ПЕРЕСЧЕТ ПЛОТНОСТИ И РАСЧЕТ ОТНОСИТЕЛЬНОЙ ПЛОТНОСТИ
ПРИРОДНОГО ГАЗА ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ
И ДАВЛЕНИИ 101,325 кПа
Б.1 Плотность природного газа при температурах 0 °C и 15 °C и давлении 101,325 кПа 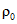
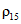
; (Б.1)
, (Б.2)
где 1,07378 и 1,01747 — коэффициенты пересчета в зависимости от температуры.
Б.2 Относительную плотность природного газа вычисляют по следующим формулам:
; (Б.3)
; (Б.4)
, (Б.5)
где d0, d15, d20 — относительная плотность природного газа соответственно при температурах 0 °C, 15 °C, 20 °C и давлении 101,325 кПа,
1,292923; 1,225410 и 1,204449 — плотность сухого воздуха стандартного состава, соответственно при температурах 0 °C, 15 °C и 20 °C и давлении 101,325 кПа, г/дм 3 (кг/м 3 ).
Источник
1.4. Состав и свойства природного газа
Природный газ представляет собой смесь предельных углеводородов состава СпН2п+2, в которой содержится метан, этан, пропан, бутан и иногда пары более тяжелых углеводородов. Часто в состав природных газов входят азот N2 (до 40 % по объему), углекислота СО2, сероводород H2S и редкие газы.
В газе газовых и газоконденсатных месторождений обычно преобладает метан; его доля достигает 98,8 %; в нефтяном (попутном) газе доля метана намного меньше, однако увеличивается доля более тяжелых углеводородов — этана, пропана и бутана [5, 7, 13, 41].
Состав газовых смесей выражается в виде массовой, объемной или молярной доли компонентов в процентах. Массовая доля в процентах какого-либо компонента газовой смеси представляет собой отношение массы этого компонента к массе всей смеси:
где Мi — масса i-го компонента; Mсм — масса смеси.
Объемная доля (%) какого-либо компонента в смеси газов равна отношению объема компонента к объему всей смеси:
где Vi — объем /-го компонента в смеси; Vсм — объем всей смеси.
Молярная доля компонента определяется аналогично и может быть представлена в виде
где Ni — число молей г-го компонента в смеси; Ncm — суммарное число молей газа в смеси.
Физические свойства природного газа зависят от его состава, но в целом близки к свойствам метана как основного компонента смеси.
Плотность природного газа можно определить взвешиванием или вычислить, зная молекулярную массу смеси М:
где Vm — объем моля газа при стандартных условиях, м 3 .
Обычно рг находится в пределах 0,73— 1,0 кг/м 3 . В расчетах часто используют более удобную величину — относительную плотность Δ так как значение ее практически не зависит от давления и температуры. За величину сравнения принимают плотность воздуха
где МГ — масса газа; Мв — масса воздуха.
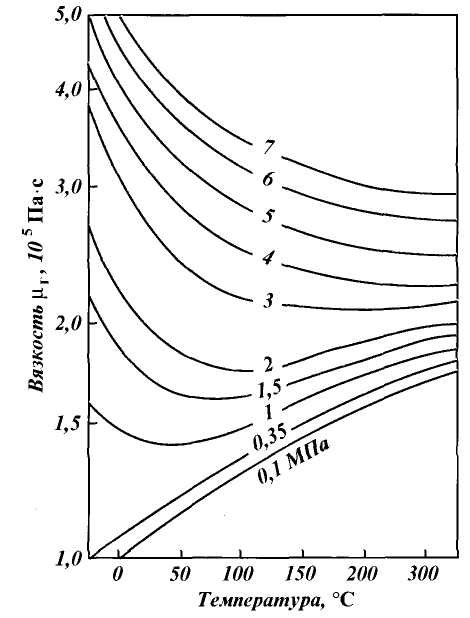
Относительная плотность газа изменяется от 0,50 до 1,0. Плотность индивидуальных компонентов углеводородных газов (и сероводорода), за исключением метана, больше единицы. При всех расчетах, связанных с движением газа, используется вязкость. Аналитические зависимости вязкости смеси от вязкости входящих в смесь компонентов сложны и имеют недостаточную точность. В связи с этим на практике вязкость определяют по экспериментальным графикам, один из которых приведен на рис. 1.2.
Рис. 1.2. Зависимость вязкости природного газа μ (при Δ = 0,6) от температуры
Состояние газа характеризуется давлением р, температурой Т и объемом V. Соотношение между этими параметрами определяется законами идеальных газов (Бойля — Мариотта, Гей-Люссака и др.), которые имеют чрезвычайно большое
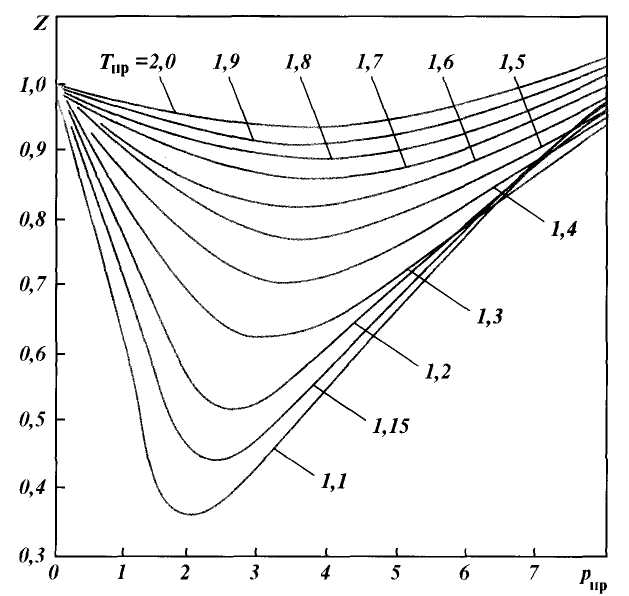
Рис. 1.3. Зависимость коэффициента сжимаемости природного газа от приведенного давления при различных температурах
pV = ZMRT,
где Z — коэффициент сжимаемости; М — масса газа; р — давление; V — объем газа; R — газовая постоянная; Т — абсолютная температура.
Для нефтяных газов значение коэффициента сжимаемости Z можно найти приближенно
Относительная плотность газа
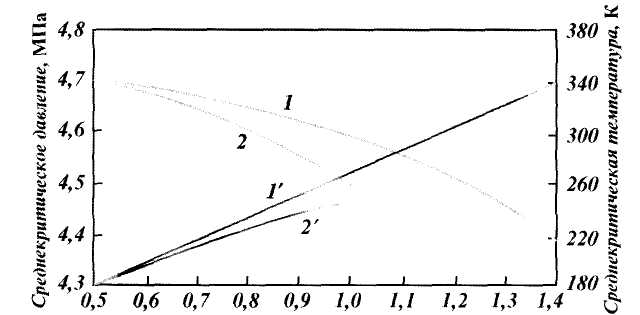
Рис. 1.4. Зависимость среднекритического давления (1, 2) и температуры (1‘ 2′ ) природного газа от относительной плотности:
1, 1‘ — газовое месторождение; 2, 2′ — газоконденсатное месторождение
по графикам Брауна, представленным на рис. 1.3. Коэффициенты сжимаемости Z на этом графике зависят от приведенных давления рпр и температуры Тпр , значения которых можно определить по формулам
где р и Т — соответственно давление и температура газа; ркр и Ткр — критические давления и температура.
Рис. 1.5. Энтальпия природного газа в зависимости от давления и температуры (при относительной плотности газа Δ = 0,6)
газа на конечном участке изменения его давления. Эту величину обычно находят по кривым теплосодержания (рис. 1.5). Зная давление газа и его температуру при одном состоянии, по этим кривым можно найти температуру газа после дросселирования. Для этого от первоначальной точки по линии равного теплосодержания следует переместиться в точку нового значения давления. Температура, соответствующая этой точке, явится искомой величиной. Изменение температуры газа при снижении давления на 0,1 МПа называется коэффициентом Джоуля — Томсона. Эта величина составляет 0,25 — 0,35 °С на 0,1 МПа (1 атм).
Источник